 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Основные виды и характеристики горения
|
|
Коэффициент горючести
Коэффициент горючести К является безразмерным коэффициентом и служит для определения горючести вещества. Рассчитанный коэффициент горючести может быть использован для приближенного вычисления температуры вспышки вещества, а также величины нижнего концентрационного коэффициента распространения пламени.
Коэффициент горючести рассчитывается по следующей формуле:
К = 4 n(C) + 4 n(S) + n(H) + n(N) – 2 n(O) – 2 n(Cl) – 3 n(F) – 5 n(Br), где (1.1)
n(C), n(S), n(H), n(N), n(O), 2 n(Cl), n(F), n(Br) – число атомов углерода, серы, водорода, азота, кислорода, хлора, фтора и брома в молекуле вещества.
Если коэффициент горючести К больше единицы (К ³ 1), то вещество является горючим; при значении К меньше единицы (К < 1) – вещество негорючее.
| Расчет коэффициента горючести веществ | Пример 1.1. Рассчитать коэффициент горючести анилина С6Н5NH2 и хлорной кислоты HClO4. |
1. В молекуле анилина
n(C) = 6; n(Н) = 7; n(N) = 1;
К = 4 × 6 + 7 + 1 = 32 К > 1, следовательно, анилин – горючее вещество.
2. В молекуле хлорной кислоты
n(Н) = 1; n(Cl) = 1; n(О) = 4;
К = 1 – 2 × 4 – 2 × 1 = - 9 К < 1, хлорная кислота – негорючее вещество.
Характер свечения пламени
Характер свечения пламени при горении веществ зависит от процентного содержания элементов в веществе, главным образом, углерода, водорода, кислорода и азота.
Свечение пламени связано с наличием несгоревших раскаленных твердых частиц углерода С, а также трехатомных молекул.
Если в горючем веществе при термическом разложении углерод не образуется, то вещество горит бесцветным пламенем как, например, в случае горения водорода Н2.
При термическом разложении веществ с массовой долей углерода менее 50 % и содержащих в своем составе кислород (более 30 %) несгоревших частиц углерода образуется очень мало, и в момент образования они успевают окислиться до СО.
СН3ОН  СО + 2Н2
СО + 2Н2
Такие вещества имеют голубоватые пламена (пламя угарного газа СО, метанола СН3ОН и этанола С2Н5ОН).
При горении веществ, содержащих более 75 % углерода (ацетилен С2Н2, бензол С6Н6), в зоне горения образуется настолько много частиц С, что поступающего путем диффузии воздуха не хватает для полного окисления всего углерода.
С6Н6  6С + 3Н2
6С + 3Н2
Не окислившийся в пламени углерод выделяется в виде копоти, и пламя при горении таких веществ будет ярким и коптящим.
Если кислород в веществе отсутствует или его содержание не превышает 30 %, но, в свою очередь, и массовая доля углерода не очень велика (менее 75 %), то при термическом разложении будет выделяться значительное количество частиц углерода, но при нормальном доступе воздуха в зону горения они успевают окислиться до СО2.
Возможная реакция при термическом разложении ацетона:
СН3СОСН3  СО + 2С + 3Н2.
СО + 2С + 3Н2.
В подобных случаях пламя будет яркое, но не коптящее.
Сопоставляя значения процентного содержания углерода и кислорода в горючих веществах, можно приблизительно судить о характере свечения пламени (таблица 1.1.).
Таблица 1.1. Характер свечения пламени в зависимости от w (С) и w (Н)
| Содержание углерода в горючем веществе, w (С) % | Содержание кислорода в горючем веществе, w (О) % | Характер свечения пламени |
| < 50 | > 30 | пламя бесцветное или голубоватое |
| < 75 | отсутствует или < 30 | пламя яркое, не коптящее |
| > 75 | отсутствует или < 25 | пламя яркое, коптящее |
| Определение характера свечения пламени | Пример 1.2. Определить характер свечения пламени метаналя НСОН, фенола С6Н5ОН и пентанола С5Н11ОН. |
1. Массовые доли углерода и кислорода в молекуле метаналя составляют:
Мr (НСОН) = 30
w (С) =  = 40 %; w (О) =
= 40 %; w (О) =  = 53 %
= 53 %
Массовая доля углерода < 50 %, а массовая доля кислорода > 30 %, следовательно, при горении метаналя наблюдается голубоватое пламя.
2. Массовые доли углерода и кислорода в молекуле фенола составляют:
Мr (С6Н5ОН) = 94
w (С) =  = 77 %; w (О) =
= 77 %; w (О) =  = 17 %
= 17 %
Массовая доля углерода > 50 %, а массовая доля кислорода < 25 %, следовательно, пламя при горении фенола яркое и коптящее.
2. Массовые доли углерода и кислорода в молекуле пентанола составляют:
Мr (С5Н11ОН) = 88
w (С) =  = 68 %; w (О) =
= 68 %; w (О) = 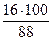 = 18 %
= 18 %
Массовая доля углерода < 75 %, а массовая доля кислорода < 30 %, следовательно, пламя при горении пентанола будет ярким, но не коптящим.
Дата публикования: 2014-10-20; Прочитано: 5686 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
