 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Уравнение Нернста. Влияние активности компонентов, участвующих в процессе, и температуры на величину потенциала описывается уравнением Нернста
|
|
Влияние активности компонентов, участвующих в процессе, и температуры на величину потенциала описывается уравнением Нернста


Если объединить постоянные величины в одну константу, а натуральный логарифм заменить десятичным, то при T = 298 К


Например, для Cr2O72- + 14H+ +  ® 2Cr3+ + 7H2O
® 2Cr3+ + 7H2O

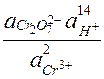
Формальный электродный потенциал  - это потенциал полуреакции, измеренный при условии, что концентрации окисленной и восстановленной формы равны 1 моль/л, а концентрации посторонних ионов известны.
- это потенциал полуреакции, измеренный при условии, что концентрации окисленной и восстановленной формы равны 1 моль/л, а концентрации посторонних ионов известны.


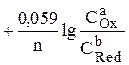
Формальный электродный потенциал является аналогом условной концентрационной константы равновесия в рассмотренных ранее равновесиях. Он равен выделенной полужирным шрифтом сумме первых трех членов в приведенном выше уравнении. Величина формального потенциала зависит от ионной силы раствора, природы и концентрации посторонних электролитов. Например, для Fe3+/Fe2+:

Константа равновесия окислительно-восстановительной реакции
Способность одного вещества отдавать электроны другому веществу можно оценить также с помощью константы равновесия окислительно-восстановительной реакции. Эта константа связана с ЭДС реакции следующим образом. Пусть реакция между окислителем Ox1 и восстановителем Red2 состоит из двух полуреакций (полуреакцию с участием Red2 для удобства запишем как процесс восстановления окисленной его формы):
Ox1 + n1 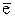 › Red1
› Red1 
Ox2 + n2 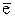 › Red2
› Red2 
Наименьшее общее кратное для n1 и n2 обозначим как m. Суммарное уравнение реакции будет иметь следующий вид
aOx1 + bRed2 › aRed1 + bOx2,
где a = m/n1, b = m/n2.

В состоянии равновесия DG = 0, DЕ = 0 и  =
= 
 =
= 
 -
-  =
= 


 =
= 

Обратите внимание, что в выражение для расчёта константы равновесия окислительно-восстановительной реакции входит не произведение числа электронов n1 и n2, а их наименьшее общее кратное m, которое может быть равно этому произведению, а может быть и не равно.
Если lgK > 0, реакция может самопроизвольно протекать в прямом направлении. Чем больше величина K, тем больше “глубина” протекания окислительно-восстановительной реакции.
Пример 7.3. Рассчитать термодинамическую константу равновесия реакции
 ›
› 
если  ,
, 
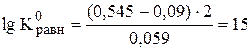

Дата публикования: 2014-10-19; Прочитано: 1094 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
