 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Обработка результатов эксперимента. 1. Рассчитать исходную и равновесные концентрации металла (2+) по уравнению:
|
|
1. Рассчитать исходную и равновесные концентрации металла (2+) по уравнению:
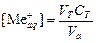 ,
,
где V T и С Т – объем, мл и концентрация, моль/л трилона Б, Va – объем аликвоты, мл.
2. Вычислить концентрацию металла (2+) в органической фазе по уравнению:
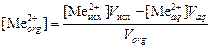 ,
,
где 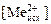 и V исх - концентрация, моль/л, и объем, мл, исходной соли металла, взятой для экстракции; Vaq – объем водной фазы, мл, Vaq = V исх + V NaOH; Vorg – объем органической фазы, мл.
и V исх - концентрация, моль/л, и объем, мл, исходной соли металла, взятой для экстракции; Vaq – объем водной фазы, мл, Vaq = V исх + V NaOH; Vorg – объем органической фазы, мл.
3. Рассчитать коэффициент распределения
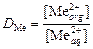 .
.
4. Заполнить таблицу:
| № п/п | V NaOH, мл | рН | V ТрБ, мл (средний) |  , моль/л , моль/л
|  , моль/л , моль/л
| D Me | lg D Me |
5. Построить график зависимости lg D Me = f (pH).
6. Построить линию тренда и вывести уравнение линии тренда на график зависимости. По коэффициентам уравнения линии тренда определить коэффициенты K (константу равновесия) и z: lg D = lg K + z pH
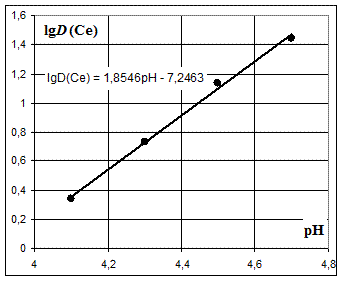
Рис. 12. Пример постоения и обработки зависимости логарифма коэффициента распределения от величины равновесного рН.
7. Сравнить полученную величину z с зарядом иона и сделать вывод о справедливости принятой модели.
8. Сравнить значения lg K для других металлов и сделать вывод о сравнительной экстрагируемости катионов металлов нафтеновыми кислотами.
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Ход эксперимента.
4. Экспериментальные данные (см. протокол к лабораторной работе).
5. Обработка экспериментальных данных.
6. Вывод.
Дата публикования: 2014-11-18; Прочитано: 486 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
