 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Описание технологического процесса и схемы. 1 страница
|
|
Технологический процесс получения сложного азотно-фосфатного удобрения состоит из следующих стадий:
4.1. Прием и слив ЖКУ.
4.2. Нейтрализация азотной кислоты газообразным аммиаком с получением растворов аммиачной селитры.
4.3. Донейтрализация аммиачной селитры с введением ЖКУ.
4.4. Упаривание полученного раствора до состояния высококонцентрированного плава и перекачивание плава наверх грануляционной башни.
4.5. Гранулирование плава с последующим охлаждением гранул.
4.6. Очистка отработанного воздуха, выбрасываемого в атмосферу.
4.7 Упаковка и хранение готового продукта [2].
4.1. Прием и слив ЖКУ.
ЖКУ поступают с ОАО “Аммофос” в железнодорожных цистернах. Из цистерны ЖКУ самотеком сливаются в приемную подземную емкость позиции Е - 30, откуда центробежными насосами позиции Н-32/1,2 подаются в бак раствора ЖКУ позиции Е-34/2,3. В зимнее время ЖКУ насосами Н-32/1,2 подаются на подогреватель Т-33, где подогреваются до температуры 20°С и далее в расходные баки раствора ЖКУ позиции Е-34/2,3 или по линии циркуляции в железнодорожную цистерну. Из расходных баков Е-34/2,3 ЖКУ насосами позиции Н-100/1,2 подаются на подогреватель ЖКУ Т-101/1, где подогреваются до температуры 70-85°С.
Смешанный NP-раствор поступает на выпарной аппарат позиции Т-101, и далее на сепаратор позиции С-102. Из сепаратора раствор САФУ подается на донейтрализатор позиции Р-4, где смешивается с раствором аммиачной селитры (не менее 89% концентрации) из аппаратов ИТН.
Емкости позиций Е-8 и Е-34 используются для перехода с производства аммиачной селитры на САФУ и наоборот.
4.2 Нейтрализация азотной кислоты газообразным аммиаком с получением растворов аммиачной селитры.
Нейтрализация азотной кислоты газообразным аммиаком является простой необратимой реакцией: NН3+НNО3®NН4NО3+Q, которая в обычных условиях протекает почти без образования побочных продуктов и с выделением теплоты (144,936 кДж/моль при взаимодействии 100 %-ных исходных продуктов).
Для процесса нейтрализации применяется азотная кислота с массовой долей не менее 57%, поэтому тепловой эффект реакции соответственно уменьшается на суммарную величину теплоты разбавления азотной кислоты и теплоты растворения твёрдой NН4NО3. Выделяющаяся в процессе нейтрализации теплота используется для испарения большей части воды из образующегося раствора аммиачной селитры, то есть на его концентрацию.
Процесс нейтрализации азотной кислоты газообразным аммиаком осуществ-ляется в двух параллельно работающих аппаратах ИТН, при давлением 20 кПа, с получением раствора аммиачной селитры с массовой долей NН4NО3 не менее 89%.
Температура процесса 148-165°С. Азотная кислота подаётся в агрегат из склада азотной кислоты, распределяется на два подогревателя позиции Т-2, где нагревается до температуры 75-95 °С за счёт теплоты конденсации сокового пара, и далее поступает в два аппарата ИТН.
Газообразный аммиак поступает в агрегат из заводской сети. Жидкий аммиак испаряется за счёт тепла конденсации пара, подаваемого во внутренний змеевик аппарата. Из аппарата Х-37 аммиак направляется в трубное пространство подогревателя Т-1, где нагревается до температуры 120-180°С паровым конденсатом, поступающим в межтрубное пространство теплообменника из пароувлажнителя X-42.
Соковый пар, образующийся при испарении NP-раствора в аппарате ИТН, и имеющий ту же температуру, поступает в сепарационную часть аппарата, где промывается от примесей аммиака и аммиачной селитры на 4-х колпачковых тарелках слабым закисленным NP-раствором и конденсатом сокового пара.
При необходимости переработки NP-раствора из хранилища Е-8 раствор насо-сом через фильтр подаётся в реакционную зону аппарата ИТН. При этом нагрузка по аммиаку на аппарат ИТН должна быть не менее 3600 кг/ч. Из аппаратов ИТН NP-раствор поступает в донейтрализатор Р-4, предназна-ченный для нейтрализации избытка азотной кислоты газообразным аммиаком, введения ЖКУ и поддержания щелочной среды раствора перед подачей его на стадию упаривания.
Для исключения попадания раствора на стадию упаривания перед выпарным аппаратом Т-10 установлен контрольный донейтрализатор Р-97.
4.3. Донейтрализация аммиачной селитры с введением ЖКУ.
NP-раствор с необходимым соотношением количества фосфатов и азота через донейтрализаторы Р-4 и Р-97, в которых газообразным аммиаком нейтрализуется избыточная кислотность раствора, поступает в выпарной аппарат позиции Т-10, где упаривается до состояния высококонцентрированного плава (Н2О£0,5%). После выпарного аппарата Т-10 NP-плав с температурой 180°С по существующей схеме проходит гидрозатвор-донейтрализатор позиции Р-13, бак для плава Е-15/1,2 и насосами подается в напорный бак отделения грануляции.
4.4. Упаривание полученного NP-раствора селитры до состояния
высококонцентрированного NP-плава и перекачивание плава
наверх грануляционной башни.
Упаривание полученного NP-раствора до состояния плава осуществляется под избыточным давление, за счёт использования тепла конденсации насыщенного пара и противоточной продувки горячим воздухом в выпарном аппарате Т-10. Раствор, поступающий в выпарной аппарат из донейтрализатора, равномерно распределяется на верхней трубной решётке и далее стекает по внутренней поверхности трубок в виде плёнки, упариваясь до массовой доли аммиачной селитры 99,0-99,5 %.
После трубчатки NP-плав поступает в нижнюю часть аппарата, и упаривается до массовой доли аммиачной селитры не менее 99,7 % [7].
Образовавшаяся ПВС с температурой не более 185°С поступает в промыватель. Здесь на трёх ситчатых тарелках происходит промывка ПВС закисленным раствором аммиачной селитры.
NP-плав из выпарного аппарата с температурой 175-185°С поступает в гидрозатвор-донейтрализатор Р-13, предназначенный для подщелачивания плава аммиаком перед перекачиванием его на стадию гранулирования.
4.5. Гранулирование NP- плава с последующим охлаждением гранул.
Процесс гранулирования высококонцентрированного NP-плава осуществляется в металлической грануляционной башне. Внизу гранулированной башни имеется встроенный металлический конус с двумя круговыми зазорами для подсоса воздуха из атмосферы. NP-плав с массовой долей аммиачной селитры не менее 99,7% и температурой 175-185°С из напорного бака Е-23 поступает в стояки перед грануляторами и далее через леечные акустические грануляторы Х-26 равномерно в виде капель разбрызгивается по всему сечению полного объёма грануляционной башни. Высота падения гранул в башне составляет 55м. Падающие капли NP-плава охлаждаются встречным потоком воздуха и кристаллизуются в виде гранул. Образовавшиеся гранулы САФУ с температурой 70-120°С через отверстие для выгрузки поступают на конвейер ПТ-30 и, далее, пройдя колосниковую решётку грохота для отделения комков и крупные частиц.
Гранулированные САФУ поступают в аппарат для охлаждения гранул в кипящем слое Х-33, охлаждается до температуры не более 50 °С. Нестандартная фракция поступает на растворение в бак позиции Е-31. Охлаждённые гранулы конвейерами подаются на узел рассева и далее в отделение упаковки и на склад.
Для предотвращения слеживаемости и пылеобразования САФУ при хранении и транспортировке гранулы удобрения обрабатывают антислеживающей добавкой (поверхностно-активным веществом) на пересыпке с конвейера позиции ПТ-61.
4.6. Очистка отработанного воздуха, выбрасываемого в атмосферу.
Загрязнённый примесями NP-смеси и аммиака воздух из грануляционной башни и промывателя паровоздушной смеси Х-98, а также соковый пар из аппаратов ИТН и скруббера Х-86 поступают на очистку в промывной скруббер Х-29.
Очищенный воздух с содержанием аммиачной селитры не более 0,1г/м3 и аммиака не более 0,05г/м3 выбрасывается в атмосферу.
Промывной раствор, пройдя тарелки скруббера, возвращается в бак Е-20, откуда насосом вновь подаётся в скруббер. NP-растворы с пониженной массовой долей аммиачной селитры, которые образуются при налаживании технологического режима в период пуска аппаратов ИТН, при дренировании аппаратов и трубопроводов агрегата, при растворении некондиционного удобрения, собираются в хранилище позиции Е-8 (Е-34). Отсюда они подаются на переработку аппараты ИТН или, при низкой концентрации NP-раствора, - на установку упаривания слабых растворов. Хранилища позиции Е-8, Е-34 для сбора слабых возвратных NP-растворы используются: одно – в качестве рабочей, другое – в качестве резервной емкости. Это обеспечивает возможность проведения чистки хранилищ от накапливающегося шлама без остановки производства.
4.7 Упаковка и хранение готового продукта
САФУ после охлаждения в аппарате кипящего слоя Х-33 подаётся на конвейер ПТ-51. Затем элеватором ПТ-59/2 продукт подаётся на конвейер ПТ-61. Откуда САФУ может подаваться через двухпозиционный шибер с пневмоприводом Х-53 на конвейер ПТ-82 для отгрузки в железнодорожные вагоны насыпью или через ручной шибер Х-54 на конвейер ПТ-71 для упаковки и отгрузки в мешках.
Температура САФУ в бункерах регистрируется, предусмотрена сигнализация максимального и минимального уровней в бункерах. Сигнализация положения переключающих устройств, а также управление ими выведены на щит КИПиА в ДПУ.
Возможные просыпи при упаковке САФУ в мешки убираются в бункеры Е-54, из которых ленточным конвейерам ПТ-79 направляются в элеватор ПТ-81 и далее через переключающее устройство на упаковку.
5. Физико-химические основы технологии
Для выбора оптимальных условий получения САФУ с различным соотношением питательных веществ необходимы данные о температурах кристаллизации (плавления) системы NH4NO3 - NH4H2PO4 при изменении соотноше-ния компонентов в широком интервале. Теоретически значения температур плавления и кристаллизации для одного и того же чистого вещества должны совпадать, но практика показывает, что полученные результаты могут не совпадать. Во-первых, аммиачная селитра в широком температурном интервале – от -300С до 1700С претерпевает ряд полиморфных превращений. Во-вторых, моноаммоний фосфат характеризуется способностью при понижении температуры образовывать переохлажденные расплавы [1].
Кроме определения физических констант САФУ (температур кристаллизации и плавления) в ходе проведения исследований был изучен метод термического анализа о химической природе исследуемого продукта. В выполняемых исследованиях по термографической оценке природы САФУ изучаемый продукт был условно представлен в виде упрощенной модельной схемы, и его состав был рассмотрен по типу сплавляемой бинарной системы состоящей из аммиачной селитры и моноаммоний фосфата.
Таблица 5.1
Результаты ДТА для смесей NH4NO3-NH4H2PO4
| NH4NO3/NH4H2PO4, % масс. | ||||||||||
| Соотношение NH4NO3/ NH4H2PO4 | 10/0 | 95/5 | 85/15 | 80/20 | 60/40 | 50/50 | 30/70 | 10/90 | ||
| Температура кристаллизации и системы | 172,5 | |||||||||
| Содержание PO2 в системе | 3,1 | 9,3 | 12,4 | 24,7 | 30,9 | 43,2 | 55,6 | |||
Причиной значительного расхождения данных по температурам плавления в системе NH4NO3-NH4H2PO4 в области кристаллизации моноаммоний фосфата могут служить такие процессы, протекающие с ним при высоких температурах. При длительном нагревании моноаммоний фосфата в процессе проведения опыта происходит отщепление воды с образованием полифосфата аммония, характеризующегося определенными физико-химическими свойствами. Выступая как индивидуальное химическое соединение, он, в свою очередь, меняет физико-химические свойства системы NH4NO3-NH4H2PO4. Выделение воды при нагревании подтверждается интенсивным вскипанием системы в области повышенных температур, правее эвтектической точки. Следовательно, метод определения температур плавления и полиморфных превращений должен быть экспрессным, характеризоваться высокой прочность и чувствительностью. Поэтому для решения данной задачи как наиболее адекватным признан метод ДТА [12].
Полиморфные превращения аммиачной селитры и минеральных удобрений на ее основе оказывают большое влияние на такие потребительские свойства, как слеживаемость, гигроскопичность, смешиваемость. Изучение двойной системы NH4NO3-NH4H2PO4 методом (ДТА), а также сравнительный анализ кривых ДТА чистой аммиачной селитры и выпускаемой в последние годы аммиачной селитры с магнезиальной добавкой, имеет не только теоретическое, но и практическое значение.
Выделяют четыре типичных эндоэффекта, которые характеризуют:
- IV (ромбическая) ↔ III (ромбическая);
- III (ромбическая) ↔ II (тетрагональная);
- II (тетрагональная) ↔ I (кубическая);
- I (кубическая) ↔ расплав.
Сравнительное определение температуры модификационных переходов в циклах нагрева и охлаждения проводились для следующих типов соединений, выступающих в производственной практике: нитрата аммония «ч», технической аммиачной селитры с магнезиальной добавкой и лабораторных образцов САФУ с содержанием P2O5 0,41 и 5,7% P2O5.
Присутствие магнезиальной добавки на 6 0С снижало температуру плавления аммиачной селитры (1690С и 1360С) и на 30С – температуру начала кристаллизации (1670С и 1640С). Фосфатная добавка в количестве 0,6% P2O5 увеличивает температуру начала перехода IV → III на 11-12 0С (42-430С и 52-550С), для переходов III → II и II → I она остается такой же, как и для аммиачной селитры.
Для проб САФУ с содержанием 0,41-5,7% P2O5 наблюдалась тенденция к понижению температуры плавления на 160С (1530С и 1690С) и увеличение температуры фазовых переходов III → II на 4-80С (92-960С и 880С) и IV → III на 6-140С (49-570С и 42-430С) при практически неизменной температуре фазового перехода II → I (129 0С) по сравнению с чистой аммиачной селитрой.
Таблица 5.2
Температуры фазовых переходов САФУ при нагреве
| Содержание P2O5, % | IV → III | III → II | II → I | I → расплав |
| 5,7 (САФУ) | ||||
| 1,6 | ||||
| 1,0 | ||||
| 0,78 | ||||
| 0,41 | ||||
| 42-43 |
При увеличении содержания в системе NH4NO3-NH4H2PO4 моноаммоний фосфата (от 0 до 5,7% P2O5) наблюдается тенденция снижения температуры плавления с 1690С до 1530С, повышения температуры фазовых переходов IV → III и III → II с 42 0С до 540С и с 880С до 940С соответственно. Температура перехода II → I осталась практически неизменной.
Снижение температуры плавления системы позволит экономить тепловую энергию на технологических стадиях упаривания и грануляции. Особенно важным является повышение температуры фазового перехода IV → III САФУ. В этом случае можно снизить расход холодного воздуха для охлаждения гранул в холодильнике кипящего слоя внизу грануляционной башни перед подачей готового продукта на склад.
6. Технологические расчеты
6.1. Материальный и тепловой балансы производства САФУ
6.1.1 Материальный баланс аппарата ИТН
Исходные данные для расчетов
1. Производительность агрегата…………………………………….450 тыс.т/год
2. Число дней работы установки в год………………………………………330
3. Производительность по 100%-ной NH4NO3, кг/ч.………………………...56800
4. Давление процесса ат. абс ……………………………………………………1,05
8. Концентрация азотной кислоты, % мас…………………………………….….58
6. Концентрация газообразного аммиака, % мас…………………………….....100
7. Потери азотной кислоты с соковым паром, кг…………………………..........7,5
8. Потери нитрата аммония с соковым паром, кг…………………………….....2,5
9. Для промывки сокового пара от аммиачной селитры и азотной кислоты в промывную зону аппарата ИТН подается КСП, кг/ч…………………………....…..3003
в том числе:
воды, кг/ч................……………………………………………………................2979
азотной кислоты, кг/ч……………………………………………………….……...12
нитрата аммония, кг/ч……………………………………………………….……..12
Молярная масса NH4NO3, кг/кмоль………………………………………….……80
Молярная масса HNO3, кг/кмоль…………………………………………….……63
Молярная масса NH3, кг/кмоль……………………………………………….…...17
Молярная масса Н2О, кг/кмоль………………………………………..………......18
1) Нейтрализация азотной кислоты газообразным аммиаком протекает по реакции: NН3+НNО3 ® NН4NО3+Q ∆Н = -146490 кДж
2) Теоретически расход НNО3 по реакции равен на 1 т. NН4NО3:
из 63 кг HNO3 получается 80 кг NH4NO3
из х кг HNO3 получается 1000 кг NH4NO3, отсюда
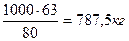
3) Практически расход с учетом потерь: 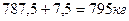
4) Теоретический расход 100%-ного NН3 по реакции равен:
из 17 кг NH3 получается 80 кг NH4NO3
из х кг NH3 получается 1000 кг NH4NO3 , отсюда
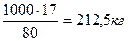 .
.
5) Практический расход NН3: 12,5+2,5 = 215 кг.
6) Часовой расход НNО3 в аппарате ИТН: 795 · 56,8 = 45156 кг/ч
Часовые потери НNО3: 7,5 · 56,8 = 426 кг/ч
7) Часовой расход NН3: 215 · 56,8 =12212 кг/ч
Часовой потери NН3: 2,5 · 56,8 =142 кг/ч
8) Расход 58%-ой кислоты на нейтрализацию:
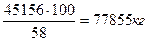 .
.
9) Масса Н2О в растворе: 77855 – 45156 = 32699 кг/ч
10) Общая масса раствора NН3 и НNО3: 77855 + 12212 = 90067 кг/ч
11) Концентрация раствора NН4NО3 без учета испарения Н2О за счет тепла реакции нейтрализации:
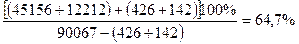
12) С учетом испарения Н2О концентрация раствора NН4NО3 на выходе из аппарата ИТН принимается 90%. Правильность выбранной концентрации проверяется тепловым расчетом. Масса 90%-го раствора NН4NО3:
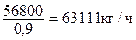
13) Масса Н2О содержащая в этом растворе: 63111 – 56800 = 6311 кг
14) Масса Н2О, испарившейся за счет тепла нейтрализации и перешедшая в СП пар: 32699 – 6311 = 26388кг/ч
Мы рассчитали материальный баланс аппарата ИТН по основным потокам NН3 и раствору НNО3. Однако с 1-й тарелки сепараторной зоны по переливной трубе в реакционную часть поступает 20%-ый раствор NН4NО3. Этот раствор смешивается с основной массой циркуляционного 90%-го раствора NН4NО3 и упарившегося до 90%-го раствора NН4NО3. Объем 20%-го раствора 6,4 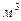 /ч, плотность 1,085 т/
/ч, плотность 1,085 т/ 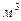 .
.
Уточним материальный баланс с учетом прихода 20%-го раствора NН4NО3.
15) Масса 20%-го раствора NН4NО3: 6,4 · 1,085 = 6,944т/ч = 6944кг/ч.
16) Масса NН4NО3 в 20%-ом растворе: 6944 · 0,2 = 1389кг/ч
17) Масса 90%-го раствора нитрата аммония после упарки 20%-го раствора:
1389/0,9 = 1543 кг
18) Масса испарившейся Н2О: 6944 – 1543 = 5401 кг
19) Общая масса выходящего 90%-го раствора NН4NО3 из ИТН:
63111 + 1543 = 64654кг.
20) Общая масса выходящего сокового пара из аппарата ИТН складывается из массы потерь NН3 и НNО3 и массы дополнительного пара после упарки 20%-го раствора:
26388 + 5401 + 426 + 142 = 32357кг.
21) Общий приход и расход массы.
Приход: 90067 + 6944 = 97011кг
Расход: 64654 + 32357 = 97011кг.
Таблица 6.1
Материальный баланс процесса нейтрализации (на два аппарата ИТН)
| Приход | Кг/ч | % масс | Расход | Кг/ч | % масс |
| Газообразный аммиак (с м. д. NН3 99,6 %), | Раствор аммиачной селитры с м. д. NН4NО3 90% на выходе из аппарата ИТН | ||||
| Азотная кислота с масс. дол. НNО3 80%, в том числе НNО3 Н2О | Соковый пар, в том числе: Н2О NН4NО3 НNО3 | ||||
| Раствор аммиачной селитры с м. д. NН4NО3 20%, том числе NН4NО3 Н2О | |||||
| Всего: | Всего: |
В данном разделе произведен расчет материального баланса на два аппарата ИТН. При этом получается большое количество сокового пара, который используется для подогрева исходных реагентов и воздуха в теплообменниках. Большое количество воды для сокового пара приходит с раствором азотной кислоты (81% от прихода).
6.1.2 Тепловой баланс аппарата ИТН
Исходные данные:
Данные материального баланса аппарата ИТН
Температура аммиака………………………………………….……………..125°С
Температура раствора азотной кислоты ………………………………..……90°С
Температура сокового пара………………………………………………….106 °С
Целью расчета теплового баланса является определение всех потоков прихода и расхода тепла.
Условием теплового баланса является равенство прихода и расхода тепла:
QПРИХ = QРАСХ (6.1)
Запишем уравнение теплового баланса:
Q1 + Q2 + Q3 + Q4 = Q5 + Q6+ Q7+ Q8+ Q9+ Q10, (6.2)
где Q1 – физическое тепло 58%-й НNО3,кДж;
Q2 – физическое тепло газообразного аммиака, кДж;
Q3 – физическое тепло 20%-го раствора, кДж;
Q4 – тепловой эффект реакции нейтрализации, кДж;
Q5–эндотермический эффект разбавления 90%-го раствора NН4NО3 20%-ым раствором NН4NО3, кДж;
Q6 – теплота, затраченная на испарение Н2О из раствора NН4NО3, кДж
Q7 – теплота, затраченная на испарение НNО3 и раствора азотной кислоты, кДж
Q8 – физическое тепло сокового пара, кДж
Q9 – физическое тепло 90%-го раствора NН4NО3, кДж
Q10 – потери тепла в окружающую среду, кДж.
Расчет прихода тепла
1) физическое тепло азотной кислоты рассчитаем по формуле:
Q = m · c · t, (6.3)
где m – масса азотной кислоты, кг;
с – теплоемкость азотной кислоты, кДж/кг·К;
t – температура азотной кислоты, °С.
Q1 = 77855 · 2,780 · 90 = 19479321 кДж.
2) физическое тепло газообразного аммиака рассчитаем по формуле:
Q = n · c · t, (6.4)
где n – количество аммиака, кмоль;
c – теплоемкость аммиака, кДж/кмоль·К;
t – температура аммиака, °С.
Q2 = 12212 · 2,26 · 125 = 3449890 кДж
3) физическое тепло конденсата сокового пара рассчитаем по формуле:
Q = n · c · t, (6.5)
Q3 = 6944 · 3,530 · 108 = 2647331 кДж
4) Q4 тепло реакции нейтрализации является суммой следующих теплот:
- теплота дегидратации азотной кислоты (она численно равна теплоте разбавления HNO3 водой до концентрации 58%), кДж/кг HNO3:
q1 = 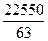 = 357,88
= 357,88
- теплота дегидратации, приходящаяся на 1 кг NH4 NO3, кДж:
q2 = 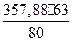 = 281,7
= 281,7
- теплота нейтрализации в соответствии с реакцией на 1 кг NH4 NO3, кДж:
q3 = 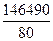 = 1830,2
= 1830,2
- теплота растворения образовавшегося нитрата аммония до концентрации 90% на 1 кг NH4 NO3, кДж/кг: q4 = 76
Удельная теплота нейтрализации равна:
q5 = 1830,2 – 281,7 – 76 = 1472,5 кДж/кг
Вычислим тепло реакции нейтрализации:
Q4 = 1472,5 · 56800 = 83638000 кДж
Общий приход тепла
Qприх = 19479321 + 3449890 + 2647331 + 83638000 = 109214542 кДж
Расчет расхода тепла
5) Масса NН4NО3 в разбавленном растворе: 56800 + 1389 = 58189кг
Общая масса разбавленного раствора: 63111 + 6944 = 70055кг
Концентрация раствора после разбавления: 58189 · 100/70055 = 83%масс
Затраты тепла на растворение NН4NО3 до концентрации 83%:
122кДж/кг · 58189кг = 7099058кДж
Затраты тепла на растворение NН4NО3 до концентрации 90%:
76кДж/кг · 58189кг = 4422364кДж
Q5 = 7099058 – 4422364 = 2676694кДж
6) теплоту, затраченную на испарение воды из раствора аммиачной селитры, рассчитаем по формуле:
Q7 = ΔНисп. · G, (6.6)
где ΔНисп – средняя теплота испарения воды при  и концентрации раствора от 63 до 90%масс,кДж/кг, кДж/кг;
и концентрации раствора от 63 до 90%масс,кДж/кг, кДж/кг;
G – масса испарившейся воды, кг.
 кДж/кг
кДж/кг
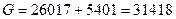 кг
кг
Q6 = 2252 ·31418 = 70753336кДж
7) Тепло, затраченное на испарение HNO3 из раствора азотной кислоты, вычислим следующим образом:
- теплота дегидратации равна 357,88 кДж/кг;
- теплота испарения HNO3 из 100%-го раствора равна 626,3 кДж/кг
- вычислим Q7: Q7 = 426 · (357,88 + 626,3) = 419260,68 кДж
8) 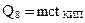 Q8 = 32357 · 1,895 · 155,5 = 9534718 кДж
Q8 = 32357 · 1,895 · 155,5 = 9534718 кДж
Дата публикования: 2014-11-18; Прочитано: 1687 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
