 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задачи для домашних заданий
|
|
Задача 1. Не проводя расчетов, определить и объяснить знак изменения энтропии в следующих реакциях:
| № задачи | Уравнение реакции |
| 1.1 | 2Н2(г)+ О2(г)= 2Н2О(г) |
| 1.2 | 2NO(г)+ O2(г)= 2NO2(г) |
| 1.3 | 2NH3(г)= N2(г) + 3H2(г) |
| 1.4 | 2Mg(к)+ О2(г)= 2MgO(к) |
| 1.5 | С6Н12О6(к)= 2С2Н5ОН(ж)+ 2СО2(г) |
| 1.6 | 2Н2S(г)+ 3О2(г)= 2Н2О(ж)+ 2SO2(г) |
| 1.7 | 2СН3ОН(г)+ 3О2(г)= 4Н2О(г)+ 2СО2(г) |
| 1.8 | 2СН3ОН(г)+ 3О2(г)= 4Н2О(ж)+ 2СО2(г) |
| 1.9 | СН4(г)+ 2О2(г)= СО2(г)+ 2Н2О(ж) |
| 1.10 | С2Н6(г)+ 3,5О2(г)= 2СО2(г)+ 3Н2О(ж) |
| 1.11 | HCl(Г) + NH3 (Г) = NH4Cl (K) |
| 1.12 | 4HCl(г)+ О2(г)= 2Сl2(г)+ 2Н2О(ж) |
| 1.13 | С2Н5ОН(г)+ 3О2(г)= 2СО2(г)+ 3Н2О(г) |
| 1.14 | Fe 2O 3(В) + CO(г) = 2FeO(В) + CO2 (г) |
| 1.15 | FeO(В) + CO(г)«Fe(В) + CO2(г) |
| 1.16 | CO(Г) + ½ O2 (Г) 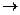 CO2 (Г). CO2 (Г).
|
Задача 2. Рассчитать количество теплоты, выделяющееся при полном сгорании 100л следующего вещества, взятого в газообразном состоянии при н.у., если в результате реакции образуется углекислый газ СО2(Г) и Н2О(Г) :
| № задачи | Вещество |
| 2.1 | метан (СН4) |
| 2.2 | этан (С2Н6) |
| 2.3 | этилен (С2Н4) |
| 2.4 | пентан (С5Н12) |
| 2.5 | н-гептан (С7Н16) |
| 2.7 | ацетилен (С2Н2) |
| 2.8 | пропан (С3Н8) |
| 2.9 | пропилен (С3Н6) |
| 2.10 | бутан (С4Н10) |
| 2.11 | н-гексан (С6Н14) |
| 2.12 | бензол (С6Н6) |
| 2.13 | толуол (С7Н8) |
| 2.14 | циклопентан (С5Н10) |
| 2.15 | н-октан (С8Н18) |
| 2.16 | циклогексан (С6 Н18) |
Задача 3. Установить возможность протекания следующей реакции при стандартных условиях и при температуре Т (зависимостью  и
и 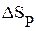 от температуры пренебречь):
от температуры пренебречь):
| № задачи | Уравнение реакции | Т,К |
| 3.1 | Fe 2O 3(тв) + 3 H2 (г) = 2Fe (тв) + 3Н2О (г) | |
| 3.2 | SO3 (г) + CO (г) = SO2(г) + CO 2(г) | |
| 3.3 | 2NО (Г) + Cl2 (Г) = 2NOCl (Г) | |
| 3.4 | 4HCl(г)+ О2(г)= 2Сl2(г)+ 2Н2О(г) | |
| 3.5 | Cl2 (Г) + H2(Г) = 2HCl (Г) | |
| 3.6 | СаСО3(ТВ) = СаО(тв) + CO 2(г) | |
| 3.7 | С2 Н4(г) + Н2О(Г) = С2Н5ОН(Г) | |
| 3.8 | СН4(г)+ 2О2(г)= СО2(г)+ 2Н2О(г) | |
| 3.9 | Fe 2O 3(тв) + CO(г) = 2FeO(тв) + CO2 (г) | |
| 3.10 | CO(г) + H2O(г) = CO2(г) + H2(г) | |
| 3.11 | FeO(тв) + CO(г) = Fe(тв) + CO2(г) | |
| 3.12 | 2CuO (тв) + CO (г) = Cu 2O (тв) + CO 2 (г) | |
| 3.13 | Fe 3O 4(тв) + 2C (ТВ) = 3Fe (тв) + 2CO2 (г) | |
| 3.14 | Fe 3O 4(тв) + CO (г) = 3FeО (тв) + CO2 (г) | |
| 3.15 | 3СаСО3(ТВ) + 2Al(тв) = Ca(ТВ) + Al2O3(ТВ) | |
| 3.16 | 2NО 2 (г) = N2O4(Г) |
Задача 4. Рассчитать концентрационную константу равновесия для приведенной реакции при температуре Т и указать, какая реакция, прямая или обратная, преобладает в системе в данных условиях:
| № задачи | Уравнение реакции | Т,К |
| 4.1 | 2Сl2(г)+ 2Н2О(г) 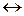 4HCl(г)+ О2(г) 4HCl(г)+ О2(г)
| |
| 4.2 | CН4(Г) 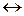 2H 2 (г) + C (ТВ) 2H 2 (г) + C (ТВ)
| |
| 4.3 | Cl2 (Г) + H2(Г) 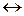 2HCl (Г) 2HCl (Г)
| |
| 4.4 | 2NО (Г) + Cl2 (Г) 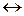 2NOCl (Г) 2NOCl (Г)
| |
| 4.5 | РCl3 (Г) + Cl2 (Г) 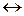 РCl5 (Г) РCl5 (Г)
| |
| 4.6 | 2Н2(Г) + Br2(Г) 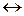 2НBr(Г) 2НBr(Г)
| |
| 4.7 | 2CO(Г) + О2(Г) 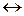 2CO2 (г) 2CO2 (г)
| |
| 4.8 | CO(Г) + Cl2 (Г) 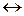 COCl2 (г) COCl2 (г)
| |
| 4.9 | CO(г) + H2O(г) 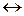 CO2(г) + H2(г) CO2(г) + H2(г)
| |
| 4.10 | 2Н2(Г) + S2(Г) 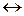 2Н2S(Г) 2Н2S(Г)
| |
| 4.11 | 2NO (г) + O 2 (г) 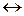 2NО 2 (г) 2NО 2 (г)
| |
| 4.12 | 2NO (г) 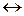 O 2 (г) + N 2 (г) O 2 (г) + N 2 (г)
| |
| 4.13 | CO(г) + 2H2 (г) 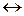 CН3OН (г) CН3OН (г)
| |
| 4.14 | CН4(Г) + H 2O (г) 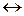 CО(г) + 3H 2O (г) CО(г) + 3H 2O (г)
| |
| 4.15 | С2 Н4(г) + Н2О(Г) 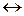 С2Н5ОН(Г) С2Н5ОН(Г)
| |
| 4.16 | СН4(г)+ 2О2(г) 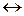 СО2(г)+ 2Н2О(г) СО2(г)+ 2Н2О(г)
|
Варианты домашних заданий
Дата публикования: 2014-11-18; Прочитано: 648 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
