 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Термохимические расчеты
|
|
Так как изменение энтальпии не зависит от пути протекания, то и тепловой эффект реакции не зависит от того, по какому пути протекает реакция. Это положение было экспериментально установлено Г.И. Гессом в 1840 году и известно как закон Гесса.
Закон Гесса. Тепловой эффект химической реакции зависит от природы и состояния исходных веществ и конечных продуктов, но не зависит от пути реакции, т.е. от числа и характера промежуточных стадий.
Например, процесс окисления углерода Ств до СО2(Г) можно осуществить как через стадию непосредственного сгорания углерода до углекислого газа с тепловым эффектом Н (путь I), так и через стадию
+ О2(Г)
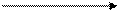   C(тв) СО2(Г), Н (путь I)
+ ½ О2(Г), + ½ О2(Г),
Н1 Н2, (путь II) C(тв) СО2(Г), Н (путь I)
+ ½ О2(Г), + ½ О2(Г),
Н1 Н2, (путь II)
|
СО(Г)
образования промежуточного продукта – окиси углерода – СО(Г) с тепловым эффектом Н1, с последующим окислением СО(Г) до СО2(Г) с тепловым эффектом Н2 (путь II) в соответствии с уравнениями реакций:
СТВ. + О2(Г) 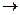 СО2(Г), Н (I)
СТВ. + ½ О2(Г) СО2(Г), Н (I)
СТВ. + ½ О2(Г) 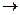 СО(Г), Н1
СО(Г) + ½ О2(Г) СО(Г), Н1
СО(Г) + ½ О2(Г) 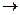 СО(Г), Н2 (II)
-------------------------------------------
СТВ. + О2(Г) СО(Г), Н2 (II)
-------------------------------------------
СТВ. + О2(Г) 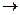 СО2(Г), Н1+ Н2.
Из сопоставления тепловых эффектов реакций следует, что Н = Н1 + Н2, т.е. каким бы путем не осуществлялась реакция, ее тепловой эффект будет одинаков, если не меняется конечное и исходное состояния системы.
Уравнения реакций, записанные с соответствующим тепловым эффектом, называются термохимическими. В термохимических уравнениях указывается агрегатное состояние вещества. Термохимические уравнения допускают наличие дробных коэффициентов, поскольку они указывают не количество молекул, а количество молей вещества. Согласно закону Гесса с термохимическими уравнениями можно оперировать как с алгебраическими.
Закон Гесса позволяет рассчитать энтальпию химических реакций.
Энтальпия химической реакции Но298, реакции равна разнице суммы стандартных энтальпий образования продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов
Но298, реакции = СО2(Г), Н1+ Н2.
Из сопоставления тепловых эффектов реакций следует, что Н = Н1 + Н2, т.е. каким бы путем не осуществлялась реакция, ее тепловой эффект будет одинаков, если не меняется конечное и исходное состояния системы.
Уравнения реакций, записанные с соответствующим тепловым эффектом, называются термохимическими. В термохимических уравнениях указывается агрегатное состояние вещества. Термохимические уравнения допускают наличие дробных коэффициентов, поскольку они указывают не количество молекул, а количество молей вещества. Согласно закону Гесса с термохимическими уравнениями можно оперировать как с алгебраическими.
Закон Гесса позволяет рассчитать энтальпию химических реакций.
Энтальпия химической реакции Но298, реакции равна разнице суммы стандартных энтальпий образования продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов
Но298, реакции = 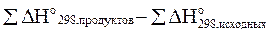 . .
| |
В общем случае, для реакции в стандартных условиях
аА(Г) + bВ(Г) 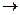 сС(Г) + dD(Г)
Но298, реакции = [(cНоC + dНоD) – (аНоА + bНоВ)], кДж,
где Но298, реакции – энтальпия химической реакции, кДж;
НоА, НоB, НоC, НоD – стандартные значения энтальпий
образования веществ, участвующих в реакции, кДж/моль;
а, b, с, d – стехиометрические коэффициенты в уравнении
реакции.
Можно также рассчитать значение стандартной энтальпии образования одного из исходных веществ или продуктов, если известны энтальпии образования остальных реагентов и энтальпия химической реакции.
Например, для реакции
аА(Г) + bВ(Г) сС(Г) + dD(Г)
Но298, реакции = [(cНоC + dНоD) – (аНоА + bНоВ)], кДж,
где Но298, реакции – энтальпия химической реакции, кДж;
НоА, НоB, НоC, НоD – стандартные значения энтальпий
образования веществ, участвующих в реакции, кДж/моль;
а, b, с, d – стехиометрические коэффициенты в уравнении
реакции.
Можно также рассчитать значение стандартной энтальпии образования одного из исходных веществ или продуктов, если известны энтальпии образования остальных реагентов и энтальпия химической реакции.
Например, для реакции
аА(Г) + bВ(Г) 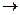 сС(Г) + dD(Г), Но298, реакции > 0.
НоА(Г) = cНоC(Г) + dНоD(Г) – bНоВ(Г) - Но298, реакции , кДж/моль А(Г). сС(Г) + dD(Г), Но298, реакции > 0.
НоА(Г) = cНоC(Г) + dНоD(Г) – bНоВ(Г) - Но298, реакции , кДж/моль А(Г).
| |
| Зная теплоты образования веществ, можно определить и их теплоты разложения по закону Лавуазье – Лапласа: При разложении сложного вещества на простые поглощается (или выделяется) столько же теплоты, сколько выделяется (или поглощается) при его образовании из простых веществ в тех же условиях. Так, если Н2(Г) +½ О2(Г) Н2О(Г), Нореакции = - 241,8 кДж, то Н2О(Г) Н2(Г) +½О 2(Г), Нореакции = 241,8 кДж. |
Понятие об энтропии и второй закон термодинамики
Первый закон термодинамики позволяет определить тепловые эффекты химических реакций (но не направление реакций в данных условиях). В 1854 г. датский химик Ю. Томсен, а затем французский химик М. Бертло высказали предположение о том, что химические процессы самопроизвольно идут только с выделением теплоты, т.е. с уменьшением энтальпии системы (с экзотермическим эффектом, ∆Н< 0).
Однако известно много примеров, когда химические реакции самопроизвольно протекают с поглощением теплоты (например, при растворении в воде некоторых солей аммония, таких как NH4Cl, NH4CNS) и, более того, одни и те же реакции в зависимости от условий могут идти как в прямом, так и в обратном направлениях. Решить вопрос о направлении химической реакции в данных условиях можно на основании закономерностей, вытекающих из второго закона термодинамики (и, в первую очередь, представления о термодинамической функции состояния, называемой энтропией).
Дата публикования: 2014-11-18; Прочитано: 1056 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
