 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Оксипроизводные: спирты, карбонильные соединения, карбоновые кислоты
|
|
Спирты – оксопроизводные углеводородов, в молекулах которых один атом водорода замещен на гидроксильную группу. Общая формула одноатомных спиртов R – OH:
С2Н5ОН – этанол.
Гликоли – спирты с двумя и более гидроксильными группами при разных углеродных атомах. Общая формула таких спиртов CnH2n(OH)m:
НO – CH2 – CH2 – OH – этиленгликоль,
НО – СН2 – СН(ОН) – СН2 – ОН – глицерин.
Глицерин легко образует глицераты с гидроксидами тяжелых металлов. Однако способность его образовывать металлические производные (глицераты) с многовалентными металлами объясняется не столько его повышенной кислотностью, сколько тем, что при этом образуются внутрикомплексные соединения, обладающие особой устойчивостью. Соединения такого типа часто называют хелатными (от греческого слова «хела» - клешня).
Фенолами называются соединения, содержащие гидроксильную группу, связанную непосредственно с бензольным ядром. В зависимости от числа гидроксильных групп в ядре различают одно-, двух- и трехатомные фенолы:

Фенол пирокатехин резорцин гидрохинон
По своим физическим и химическим свойствам алифатичесие спирты и фенолы заметно отличаются друг от друга.
Общим способом получения спиртов, имеющим промышленное значение, является гидратация алкенов. Реакция идет при пропускании алкена с парами воды над фосфорнокислым катализатором:
СН2 ═ СН2 + Н2О → СН3 – СН – ОН.
Спирты получают гидролизом алкилгалогенидов под действием водных растворов щелочей:
R – Br + NaOH → R – OH + NaBr.
Спирты получают восстановлением карбонильных соединений (при восстановлении альдегидов образуются первичные спирты, при восстановлении кетонов – вторичные):
R – CH = O + H2 → R – CH2 – OH,
R – CO – R' + H2 → R – CH(OH) – R'.
Химические свойства спиртов определяются присутствием в их молекулах гидроксильной группы (ОН). Связи С – О и О – Н сильнополярны и способны к разрыву.
Реакции с разрывом связи О – Н.
1. Низшие спирты бурно реагируют со щелочными металлами:
2С2Н5ОН + 2К → 2С2Н5ОК + Н2.
2. При действии на спирты минеральных и органических кислот образуются сложные эфиры (реакция этерификации):
С2Н5ОН + СН3СООН → СН3СООС2Н5 + Н2О,
С2Н5ОН + HONO2 → C2H5ONO2 + H2O.
3. Спирты окисляются под действием дихромата или перманганата калия до карбонильных соединений. Первичные спирты окисляются до альдегидов, а вторичные – до кетонов:
R – CH2 – OH → R – CH ═ O → R – COOH,
CH3 – CH(OH) – CH3 → CH3 – C(O) – CH3.
Реакции с разрывом связи С – О.
1. Реакции дегидратации протекают при нагревании спиртов с водоотнимающими средствами. При сильном нагревании происходит внутримолекулярная дегидратация с образованием алкенов, при более слабом нагревании происходит межмолекулярная дегидратация с образованием простых эфиров:
t, H2SO4
CH3 – CH2 – CH2 – OH → CH3 – CH ═ CH2 + H2O,
t, H2SO4
2CH3 – CH2 – OH → C2H5 – O – C2H5 + H2O.
2. Спирты реагируют с галогеноводородными кислотами:
ROH + HCl → RCl + H2O.
Альдегиды и кетоны – производные углеводородов, в которых содержится одна и более карбонильных групп.
Если карбонильная группа соединена с одним радикалом и водородом, то такие соединения называются альдегидами:
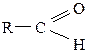
Соединения, в которых карбонильная группа соединена с двумя одинаковыми или разными радикалами, называются кетонами:
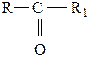
В зависимости от характера радикалов, связанных с карбонильной группой, альдегиды и кетоны могут быть насыщенными, ненасыщенными, алифатическими или ароматическими
Насыщенные:
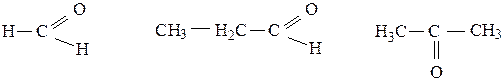
метаналь пропаналь ацетон
Ненасыщенные:

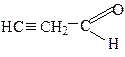
пропеналь пропиналь
Ароматические:

бензойный альдегид
Карбонильные соединения относятся к числу весьма реакционноспособных органических веществ. Их химические свойства связаны с особенностями электронного строения карбонильной группы. Связь между атомом углерода и атомом кислорода вследствие большой электротрицательности кислорода по сравнению с углеродом сильно поляризована за счет смещения электронной плотности π – связи к кислороду:
С ═ О.
Сильная поляризация связи С ═ О в карбонильных соединениях ведет к тому, что на кислороде сосредотачивается отрицательный заряд, а на карбонильном углероде – положительный. Полярность карбонильной группы определяет и ее реакции. Большинство реакций карбонильных соединений – это реакции, в которых положительно заряженный карбонильный углерод – электрофильный центр молекулы взаимодействует с нуклеофильными реагентами.
1. СН3 – СН = О + HCN → CH3 – CH(CN) – OH
2. R – CH = O + NaHSO3 → R – CH(OH) – SO3Na


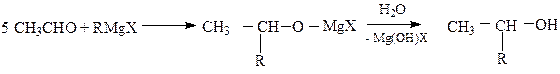

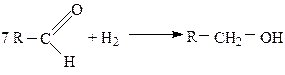

Карбоновыми кислотами называют производные углеводородов, которые содержат в молекуле одну или несколько карбоксильных групп - СООН. Карбоксильную группу можно рассматривать как формальное сочетание карбонильной группы и гидроксила («карб–оксил»).
В зависимости от природы радикала, связанного с карбоксильной группой, карбоновые кислоты делят на предельные и непредельные, алифатические и ароматические.
Число карбоновых групп определяет основность кислот: кислоты с одной карбоксильной группой являются одноосновными, с двумя – двухосновными и т.д. Кроме того по количеству углеродных атомов в радикале различают кислоты низшие (низкомолекулярные) и высшие (высокомолекулярные).
Карбоновые кислоты с числом атомов углерода выше 6 называют высшими (жирными) кислотами.
Алифатические предельные одноосновные карбоновые кислоты имеют общую формулу СnH2nO2 или CmH2m+1COOH.
СН3СООН – уксусная кислота (этановая),
СН3(СН2)16СООН – стеариновая кислота (октадециловая)
Получение. 1 Общий способ получения карбоновых кислот – окисление альдегидов и первичных спиртов, в качестве окислителей применяют KMnO4 и K2Cr2O7:
R – CH2 – OH → R – CH ═ O → R – COOH.
2 Гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода. Образуются спирты, содержащие группы ОН у одного атома, эти вещества неустойчивы и отщепляют с образованием карбоновой кислоты:
R – CCl3 → [R – C(OH)3] → R – COOH.
3 Получение карбоновых кислот из цианидов – способ, позволяющий наращивать углеродную цепь при получении исходного цианида:
CH3 – Br + NaCN → CH3 – CN + NaBr;
CH3 – CN + 2H2O → CH3COONH4;
CH3CONH4 + HCl → CH3COOH + NH4Cl.
4 Для отдельных кислот существуют специфические способы получения. Муравьиную кислоту получают нагреванием оксида углерода (II) с порошкообразным гидроксидом натрия:

Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
2C4H10 + 5O2 → 4CH3COOH + 2H2O
Химические свойства. Карбоновые кислоты – более сильные кислоты, чем спирты, так как атом водорода в карбоксильной группе обладает повышенной подвижностью благодаря влиянию группы СО. В водном растворе карбоновые кислоты диссоциируют:
RCOOH → RCOO- + H+.
Сила карбоновых кислот зависит от электронного эффекта группы, связанной с группой СООН. Электроноакцепторные заместители (ССl3) оттягивают электронную плотность от карбоксильной группы и способствуют диссоциации кислоты. Электронодонорные заместители (углеводородные заместители) увеличивают электронную плотность на карбоксильной группе и затрудняют диссоциацию кислоты.
1 Карбоновые кислоты реагируют с активными металлами, основными кислотами, основаниями и солями более слабой кислоты:
2RCOOH + Mg → (RCOO)2Mg + H2;
2RCOOH + CaO → (RCOO)2Ca + H2O;
RCOOH + NaOH → RCOONa + H2O;
RCOOH + NaHCO3 → RCOONa + H2O + CO2↑.
2 Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала:

Дата публикования: 2014-11-03; Прочитано: 1662 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
