 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Сущность каталитического действия
|
|
Катализ обусловлен промежуточным химическим взаимодействием реагирующих веществ с катализатором, в результате которого открывается новый реакционный путь. Ускорение процессов с помощью катализаторов достигается за счет того, что появляются новые механизмы, при которых медленные стадии заменяются более быстрыми.
Реакция превращения веществ А и В в вещество АВ с участием катализатора К осуществляется по следующей схеме:
A + K® AK
АК + В ® АВ + К
-------------------------------------
А + В ® АВ.
Независимо от механизма действия роль катализатора с точки зрения энергетики реакции сводится, как показано на рис. 9, к снижению энергии активации (Е акат < Е а ), за счет чего увеличивается константа скорости реакции.
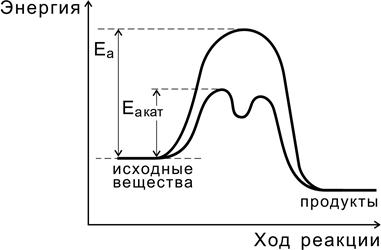
Рис.9. Реакция с участием катализатора
Катализатор может также способствовать необходимой для взаимодействия молекул ориентации.
Катализатор не влияет на константу химического равновесия и не смещает положение химического равновесия.
Энергия активации прямой и обратной реакций при введении катализатора уменьшается на одинаковую величину.
Катализатор ускоряет прямую и обратную реакции, т.е. сокращает время достижения равновесия при подходе к нему как со стороны исходных веществ, так и со стороны продуктов.
Дата публикования: 2014-11-02; Прочитано: 1292 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
