 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Фазовые переходы. Уравнение Клапейрона-Клаузиуса
|
|
В системе, состоящей из нескольких фаз чистого вещества, находящихся в равновесии, возможны переходы вещества из одной фазы в другую. Такие переходы называются фазовыми переходами.
Рассмотрим равновесный переход одного моля вещества из одной фазы (1) в другую (2), совершающийся при постоянных давлении и температуре. Энергии Гиббса (G 1и G 2) моля вещества в фазах 1 и 2 равны (условие равновесия). Следовательно:
G 2 = G 1 (IV, 1)
Напишем уравнения (III,31) полных дифференциалов для энергии Гиббса одного моля чистого вещества в двух равновесных фазах 1 и 2:
dG 1 = V 1 dP – S 1 dT
dG 2 = V 2 dP – S 2 dT (IV, 2)
Вычитая верхнее уравнение из нижнего, получим:
dG 2 – dG 1 = (V 2 – V 1) dP – (S 2 – S 1) dT
Изменения P и Т здесь были не независимыми, а такими, при которых сохранялось равновесие между фазами 1 и 2. Таким образом, между P и Т сохранялась функциональная связь, соответствующая фазовому равновесию. Поэтому, если G 1 = G 2(равновесие при давлении P и температуре Т), то G 1 + dG 1 = G 2 + dG 2(равновесие при давлении P + dP и температуре T + dT), значит, dG l = dG 2 или dG 2 — dG 1 = 0. Следовательно
(V 2 – V 1) dP – (S 2 – S 1) dT = 0
или
 (IV, 3)
(IV, 3)
Взаимное превращение фаз рассматривалось как равновесное и изотермическое, поэтому:
 (IV, 4)
(IV, 4)
Здесь  — теплота фазового превращения, поглощаемая или выделяемая при переходе моля вещества из фазы 1 в фазу 2; V 2 – V 1 — разность мольных объёмов двух фаз.
— теплота фазового превращения, поглощаемая или выделяемая при переходе моля вещества из фазы 1 в фазу 2; V 2 – V 1 — разность мольных объёмов двух фаз.
Из уравнений (IV, 3) и (IV, 4) получим:
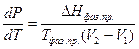 (IV, 5)
(IV, 5)
Уравнение (IV, 5) называется уравнением Клапейрона - Клаузиуса и является общим термодинамическим уравнением, приложимым ко всем фазовым переходам чистых веществ.
Дата публикования: 2014-11-04; Прочитано: 642 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
