 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Раздел 5. Факторы, влияющие на токсичность 8 страница
|
|
2.3.2. Псевдоаллергические реакции
Различные химические вещества, действуя на организм, порой вызывают состояния, чрезвычайно напоминающие аллергические реакции и проявляющиеся широким спектром нарушений от кожной сыпи до астмы и анафилаксии. При этом лабораторными методами не удаётся выявит участие в процессе иммунологических механизмов. Молекулярные механизмы таких феноменов в полной мере не ясны. Не исключено, что некоторые ксенобиотики обходят обычный двухстадийный процесс активации тучных клеток (фиксация на поверхности клеток антител; взаимодействие антигена с фиксированными антителами). В этом случае дегрануляция и высвобождение биологически активных веществ происходит вследствие непосредственного разрушения тучных клеток (цитотоксическое действие).
2.3.3. Иммуногены и аллергены
Молекулы, вызывающие иммунный ответ организма, называются иммуногенами. Идентификация иммуногена может быть осуществлена с помощью моноклональных антител. Как правило, аллергия развивается при действии именно иммуногенов, то есть высокомолекулярных соединений, естественных полных антигенов. Однако становится все более очевидным, что многие низкомолекулярные вещества (производственные токсиканты, лекарства, косметика, экополлютанты и т.д.) также могут вызвать состояние гиперреактивности, т.е. выступить в качестве аллергенов.
Еще со времен Ландштейнера известно, что при определенных условиях возможно формирование иммунной реакции на введение низкомолекулярного вещества, однако при условии, что оно вступит во взаимодействие с высокомолекулярным носителем с образованием так называемого комплексного антигена. Таким образом, важными моментами, определяющими вероятность развития аллергии, являются химические свойства, сенсибилизирующая доза вещества и продолжительность контакта. Для того чтобы вызвать иммунный ответ низкомолекулярное вещество должно обладать свойствами гаптенов, т.е., с одной стороны, иметь возможность взаимодействовать с эндогенными структурами организма, обладающими антигенными свойствами, а с другой, так модифицировать их, чтобы сенсибилизированные этим комплексным антигеном лимфоциты вырабатывали антитела, способные распознавать именно токсикант. Не редко аллергенами являются не сами вещества, а продукты их метаболизма. По-видимому, существует прямая связь между химической реакционной способностью и сенсибилизирующей активностью вещества. Токсиканты, образующие обратимые связи с белками крови не являются аллергенами.
В настоящее время установлено, что в иммунном ответе на комплексный антиген принимают участие как Т-, так и В-лимфоциты. При этом В-клетки распознают гаптен, а Т-клетки - макромолекулярный носитель. Этот принцип реализуется и при формировании реакции на естественные антигены. Антигены, активирующие иммунную реакцию только через взаимодействие с Т-клетками, называются Т-зависимыми антигенами. Антигены, активирующие иммунолгический процесс путем взаимодействия только с В-клетками, называются В-зависимыми антигенами. Количество веществ, действующих исключительно через Т- и В- лимфоциты, крайне мало.
Как указывалось выше, в качестве носителя гаптена могут выступать различные макромолекулы: белки, полипептиды, полисахариды. Особой реакционной активностью при образовании связей с носителем обладают соединения, имеющие в структуре амно-, нитро-, азо-, карбаминовые и некоторые другие группы. Как уже указывалось, во взаимодействие с носителем может вступать не исходный ксенобиотик, а продукт его метаболизма. Таков механизм формирования комплексного антигена, в частности, при действии на организм производных р-аминобензола. Предположительно в ходе метаболических превращений происходит гидроксилирование или окисление NH2-группы вещества. Образующиеся активные радикалы легко вступают во взаимодействие с сульфгидрильными и другими функциональными группами молекул-носителей с образованием ковалентных связей (рисунок 4).
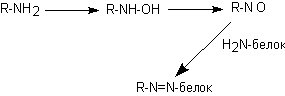
Рисунок 4. Взаимодействие лиганда с белком
Подобные вещества вызывают аллергические реакции на целую группу соединений, что объясняется близостью их строения (рисунок 5).
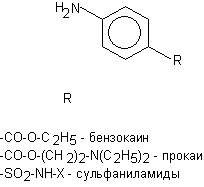
Рисунок 5. р-аминобензол и его производные
Совокупность близких по строению аллергенов образует "парагруппу". К "парагруппе" производных аминобензола относятся, в частности, сульфаниламиды, производные фенотиазина, ацетанилиды, азокрасители, пикриновая кислота и др.
Другими хорошо известными аллергенами являются вещества, также способные образовывать прочные ковалентные связи с белками. Это цианаты, тиоцианаты, изотиоцианаты, альдегиды, галоген-содержащие вещества, тиогликолаты (таблица 6). К числу аллергенов принадлежат также ионы металлов Ni, Co, Zn, Hg, Ag, Cr и др.
Таблица 6. Строение некоторых низкомолекулярных аллергенов
| Название | Строение |
| цианаты тиоцианаты изотиоцианаты альдегиды тиогликолаты | R-OCN R-SCN R-CNS R-CH=O R-C-SH |
Особый вид аллергии, вызываемый ксенобиотиками, представляет фотоаллергия. В данном случае образование прочной связи между молекулой белка и гаптеном, накопившемся в коже, активируется в результате фотохимического превращения последнего, как правило, при действии ультрафиолетовых лучей. В клинической практике нередко встречаются с фотоаллергическими реакциями на хлорпромазин, псорален, сульфаниламидные препараты и др. (см. раздел "Дерматотоксичность").
Сенсибилизирующие свойства вещества могут быть оценены с помощью "индекса сенсибилизации", который представляет собой выраженную в процентах вероятность развития аллергии у лиц, контактирующих с веществом. Индекс сенсибилизации некоторых лекарственных веществ представлен в таблице 7.
Способность сенсибилизировать организм у разных веществ выражена не одинаково. Некоторые соединения (например фенилэтилгидантион, см. рисунок 6) в 90% случаев вызывают аллергизацию (появление экзантемы, отек кожи лица и слизистых оболочек, лихорадка), другие дают осложнение менее чем в 1% случаев.
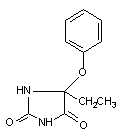
Рисунок 6. Структура фенилэтилгидантиона. Снотворное средство
Важен способ аппликации вещества. Так, пенициллин при приёме через рот вызывает аллергические реакции менее чем в 1% случаев, при парентеральных способах введения - в 3%, а при аппликации на слизистые - до 15%.
Таблица 7. Индекс сенсибилизации некоторых лекарственных веществ
| Вещество | Аппликация | Индекс сенсибилизации (%) | Замечания |
| Пенициллин Стрептомицин Тетрациклин Сульфаниламдные препараты Барбитураты Фенотиазины Аспирин Фенилэтилгидан-тион Фенилметилги-дантион | Местно слизистые местно кожа парентерально через рот местно - - местно через рот, парентерально местно через рот - местно через рот - - | до 9 до 30 до 20 до 5 до 3 до 50 0,2 - 3,5 80 - 90 5 -10 | у больных - - - у больных на производстве обслуживающий персонал на производстве - - - у больных обслуживающий персонал у больных - - |
По частоте аллергических реакций, вызываемых медикаментами, на первом месте стоит пенициллин. Механизм формирования реакции в основном изучен. Антитела формируются на метаболиты пенициллина, в частности пеницилловую кислоту, пеницилленовую кислоту, пеницилламин. Эти соединения взаимодействуют с белками с образованием прочных амидных связей. Возможна перекрестная аллергия к другим препаратам группы пенициллина. Высокой иммуногенностью обладает цефалоспорин. При расщеплении 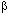 -лактамного кольца препарата выявляются реактивные группы, обеспечивающие взаимодействие их с белками.
-лактамного кольца препарата выявляются реактивные группы, обеспечивающие взаимодействие их с белками.
Свойствами аллергенов обладают производные салициловой кислоты, встречающиеся в виде примесей в лекарственных формах препарата (ангидрид ацетилсалициловой кислоты, цис-дисалицилид и др.).
Примерно у 3%, принимающих барбитураты, развиваются аллергические реакции. Как правило, отмечаются кожные проявления (экзантемы, эритема). Производные фенотиазина вызывают контактную сенсибилизацию кожи, аутоиммунный агранулоцитоз, отек Квинке. Наиболее часто реакция развивается у работающих на производствах по выпуску препаратов. Аллергенами также являются некоторые анестетики (новокаин, прокаин, бензокаин), рентгеноконтрастные вещества, вызывающие кожные реакции (эритема, уртикарная сыпь, буллезные изменения кожи, лихорадку), блокаторы адренорецепторов (поражение глаз, серозных оболочек).
У большинства людей при действии иммуногенов происходит сенсибилизация клеток, вырабатываются антитела. Однако далеко не у всех развиваются гиперреактивные реакции. Склонность к развитию гиперреактивных состояний, выявляемая у некоторой части популяции людей, объясняется генетически обусловленными особенностями человека (см. выше). Это еще более усложняет работу по контролю за качеством среды и обеспечению здоровья населения, поскольку у высоко чувствительных сенсибилизированных лиц неблагоприятные эффекты могут развиваться от доз токсикантов значительно ниже допустимых.
Механизмы действия аллергенов суммированы в таблице 8.
Таблица 8. Механизмы действия токсикантов, вызывающих аллергизацию организма и активацию аутоиммунных процессов
| - вещество или его метаболиты являются полными антигенами; - вещество или его метаболиты являются гаптенами, способными образовывать с белками крови иммуногены и аутоантигены; - вещество или его метаболиты ковалентно связываются с макромолекулами легких, кожи, желудочно-кишечного тракта и т.д.; - вещество непосредственно повреждает иммунную систему, активируя В-лимфоциты, Т-лимфоциты, увеличивая соотношение хелперов/ супрессоров; - повреждение органа химическим веществом с высвобождением "скрытых" антигенов, превращающихся таким образом в аутоантигены; - ксенобиотик и макромолекулы тканей организма имеют общие антигенные детерминанты; |
2.4. Аутоиммунные процессы
Распознавание "чужеродного" и формирование биологической реакции на него - основная функция иммунной системы. Для того, чтобы реагировать на чужое, иммунная система должна распознавать и "своё". Поломки в механизмах, позволяющих иммунокомпетентным структурам отличать своё от чужого лежат в основе аутоиммунных процессов. Количество болезней и синдромов, в основе которых лежат аутоиммунные процессы неуклонно возрастает. Ранее в качестве пускового механизма рассматривали действие, прежде всего, инфекционного фактора. В настоящее время не меньшее значение придаётся химическим агентам.
Имеющиеся данные свидетельствуют, что аутоиммунные заболевания являются следствием количественных нарушений отдельных сторон и в норме протекающих процессов: увеличения количества пролиферирующих стволовых клеток, продуцируемых антител, образующихся комплексов антиген-антитело (иммунные комплексы). Полагают, что заболевания являются следствием сочетанного действия ряда причин, включая генетически обусловленную индивидуальную предрасположенность, сопутствующие воздействия среды, благоприобретённые дефекты механизмов регуляции иммунной системы. Так, у животных, с вызванным в эксперименте аутоиммунным процессом выявляется дефект клеток-супрессоров.
Аутоиммунные заболевания подразделяются на орган-специфичные и орган-неспецифичные. Оба процесса запускаются нормальными антигенами собственного организма, либо антигенами, модифицированными действием экзогенных факторов. Поскольку химические вещества могут с одной стороны, вступая во взаимодействие с макромолекулами организма изменять их антигенные свойства (см. выше), а с другой - существенно изменять процессы активации лимфоцитов, синтеза антител, продукцию цитокинов, не удивительно, что результатом взаимодействия организма и ксенобиотика могут стать аутоиммунные заболевания (таблица 9). Ртуть, диэлдрин, метилхолантрен - известные стимуляторы аутоиммунных реакций.
Таблица 9. Аутоиммунные болезни. Патология, обусловленная антителами
| Синдромы | Соответствующие ассоциированные антигены |
| Системная красная волчанка | однонитевая и двунитевая ДНК, ядерные и цитоплазматические ассоциированные антигены |
| Миастения гравис | рецепторный белок к ацетилхолину |
| Аутоиммунный тиреоидит | Тириоглобулин |
| Аутоиммунная эндокринопатия | отдельные гормоны |
| Аутоиммунная гемолитическая анемия | ксенобиотик, присоединенный к мембране клетки крови |
| Иммунная гранулоцитопения | - |
| Иммунная тромбоцитопения | - |
| Пузырчатка | внутриядерные ассоциированные антигены |
| Сывороточная болезнь | модифицированные белки крови |
| Анафилаксия | - |
Можно выделить три механизма, пока гипотетичных, инициации химическими веществами аутоиммунных заболеваний:
1. Прямое действие токсиканта на иммунную систему. Ксенобиотики могут оказывать действие на лимфоциты и макрофаги. В итоге, возможно, показанное в эксперименте, угнетение активности Т-супрессоров, усиление активности Т-хелперов, активация поликлональных В-лимфоцитов. Так, метилдофа, взаимодействуя с Т-супрессорами, провоцирует развитие аутоиммунной анемии у человека. Некоторые металлы, например, ртуть, вызывают стимуляцию поликлональных В-лимфоцитов.
2. Высвобождение аутоантигенов. Многие ксенобиотики могут нарушать целостность биологических структур и способствовать выходу в кровь тканевых антигенов, с которыми в норме иммунокомпетентные клетки не сталкиваются. Возможно простое увеличение количества антигенов, в норме циркулирующих в крови. Хроническое воздействие некоторых металлов (ртути, золота, марганца, кобальта и т.д.) вызывая хронический воспалительный процесс в тканях, провоцируют развитие аутоиммунных реакций.
3. Модификация собственных антигенов. Ксенобиотики, взаимодействуя с макромолекулами тканей, могут изменять их конформацию, формировать в них новые детерминанты, вызывать экспрессию "спрятанных" детерминантных групп. В итоге эти структуры перестают восприниматься иммунной системой как "свои". Примером такого взаимодействия является действие дигидролазина (рисунок 7) на нуклеопротеины.
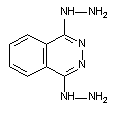
Рисунок 6. Структура дигидролазина. Мочегонное средство
Наиболее вероятно возникновение аутоиммунных заболеваний при длительном, хроническом действии токсикантов на организм. Эту возможность следует иметь в виду при обеспечении здоровья лиц, контактирующих с вредными факторами на производствах, проживающих в экологически неблагоприятных регионах.
3. Краткая характеристика токсикантов
3.1. Бериллий.
Хотя бериллий был открыт еще в 18 веке, его токсическое действие обнаружилось лишь в ХХ.
В 1945-50 годах в США регистрировались эпидемические вспышки острых и хронических интоксикаций бериллием на предприятиях по его производству, выплавке сплавов, изготовлению неоновых ламп, а также среди населения, проживающего близ этих производств. Первоначально патологию, вызванную металлом, принимали за саркоидоз, легочное и мультисистемное заболевание неизвестной этиологии. В настоящее время заболевания острым бериллиозом на предприятиях полностью ликвидированы. Однако экологи полагают, что в связи с увеличением объемов используемого в производстве бериллия возможен рост числа лиц, подвергающихся хроническому воздействию. Коварство бериллия, его способность вызывать реакцию сенситизации заставляют исследователей и практических врачей рекомендовать строгий контроль за состоянием здоровья всех людей, работающих с бериллием.
Заболевание, возникающее в результате длительно воздействия бериллием, называется хроническим бериллиозом и представляет собой гранулематозный процесс, проявляющийся преимущественно в легких, реже в других органах. В отличие от острого поражения, интенсивность хронического воздействия, по-видимому, не является важным фактором, определяющим тяжесть поражения. Дело в том, что в основе патологии лежит реакция гиперчувствительности к бериллию, выступающему в качестве антигена или гаптена. Недавние исследования показали, что сенситизация может развиться даже при кратковременном действии металла в очень малых концентрациях. Скрытый период между моментом первого воздействия бериллием и развитием клиники заболевания продолжается от нескольких месяцев до 30 лет. Средняя продолжительность латентного периода 6-10 лет.
Нарушения функций легких при хроническом бериллиозе могут протекать в нескольких формах:
1. преимущественно обструктивный тип (примерно у трети отравленных);
2. рестриктивный тип (у одной четверти пострадавших);
3. снижение диффуззионной способность легких (в тесте с СО) при неизмененных легочных объемах и проходимости бронхов (у одной трети пострадавших).
Наиболее ранний симптом √ одышка при физической нагрузке. Часто присоединяются боли за грудиной, кашель, артралгии, повышенная утомляемость, потеря веса. При исследовании выявляются двухсторонние хрипы, цианоз, пальцы в форме барабанных палочек, лимфоаденопатия, поражения кожи. В запущенных случаях √ правосердечная недостаточность, cor pulmonale. У небольшой части отравленных отмечаются нарушения, выявляющиеся лишь при физических нагрузках в форме увеличения альвеолярно-артериального градиента рО2; процесс без нарушения функций на фоне гранулемы в легких и бериллий-специфических иммунологических реакций лимфоцитов легочного лаважа.
При исследовании биоптатов легких у больных выявляются нераспадающиеся гранулемы, мононуклеарные клеточные инфильтраты в интерстиции легких и различной степенью выраженности фиброз легких. В бронхоальвеолярном лаваже обнаруживается большое количество лейкоцитов, увеличенное число лимфоцитов, повышенное соотношение Т-хелперов к Т-супрессорам.
Помимо легких, гранулемы обнаруживаются в печени, селезенке, региональных лимфатических узлах, миокарде, скелетных мышцах, почках, слюнных железах, костях, коже.
Хроническая интоксикация бериллием часто сопровождается гранулематозными изменениями кожных покровов даже в тех случаях, когда прямого действия металла на покровную ткань не было.
У 10% больных выявляется гепатомегалия. Реже в патологический процесс вовлекается ЦНС.
В литературе имеются данные о выздоровлении, наступившем без лечения. Однако на такой исход всегда мало надежды. У большинства больных постепенно прогрессирует дыхательная недостаточность и правожелудочковая недостаточность сердца. В запущенных случаях бериллиоза летальность может составить до 30%.
4. Определение иммунотоксичности ксенобиотиков
Стратегия определения иммунотоксичности состоит в последовательном изучении в эксперименте состояния элементов иммунной системы (от клетки до целостного организма), в условиях воздействия испытуемого токсиканта. Ни одна отдельно взятая методика не является в полной мере надежной и достаточной для оценки потенциальной опасности ксенобиотика. Содержание одного из пакетов тестов представлено в таблице 10.
Таблица 10. Двухэтапный пакет тестов оценки иммунотоксичности ксенобиотика
| Этап | Параметры | Методы исследования |
| 1. Этап скрининга | Иммуноморфология Гуморальный иммунитет Клеточный иммунитет Неспецифическая резистентность | Гематологические: общий анализ крови, формула крови; Вес тела, селезенки, тимуса, почек, печени, легких; Гистология: селезенки, тимуса, лимфатических узлов Подсчет колоний клеток, образующих IgM к Т-зависимым и Т-независимым антигенам и ответ на митогены Ответ на действие митогена и смешанный лейкоцитарный ответ на аллогенные лейкоциты Фагоцитарная активность клеток |
| 2. Этап изучения механизмов | Морфология Гуморальный иммунитет Клеточный иммунитет Неспецифический иммунитет Оценка резистентности организма | Подсчет числа В- и Т-лимфоцитов в селезенке Подсчет колоний клеток, образующих IgG к Т-зависимым антигенам Функции цитотоксических лимфоцитов; Количество перитонеальных макрофагов и анализ их функциональной активности Прививка опухолевых тканей: саркома PYB6 меланома B6F10 Бактериальные модели: Listeria monocytogenes Streptococcus spp Паразитарные модели: Trypanosoma musculi Plasmodium yoellii Вирусные модели: вирус гриппа |
Исследования первого этапа предназначены для выявления потенциальных иммунотоксикантов. Тесты второго этапа позволяют установить механизм иммунотоксичности и потенциальную способность вещества нарушать общую резистентность организма. Обычно токсикант вводится мышам в течение 14 дней, хотя в случае неясных результатов введение может быть продолжено до 30 и даже 90 суток.
Для изучения иммуносупрессорных свойств токсикантов в лабораторных условиях могут быть применены животные, зараженные патогенными микроорганизмами. С целью инфецирования используют: Listeria monocytogenes, Streptococcus pneumonia, Trypanosoma musculi, Plasmodium yoellii, вирус гриппа, вирус герпеса простого и т.д. В подобного рода исследованиях удаётся оценить состояние отдельных элементов иммунной системы. Продолжительность анализа - 2 - 3 недели.
Примером хорошо отработанного теста на иммунотоксичность ксенобиотика, является метод введения мышам, подвергшимся действию токсиканта, культуры трипаносом (trypanosoma musculi). Эти трипаносомы являются непаразитическими, экстрацеллюлярными микроорганизмами. Поражение мышей этими организмами на ранних этапах заражения контролируется врожденными механизмами резистентности, в частности фагоцитозом. В поздние стадии (10 дней инфекционного процесса) паразитемия контролируется механизмами антителообразования. Конечный этап (18 - 20 день) инфекционного процесса проходит под контролем как клеточного, так и гуморального иммунитета. Таким образом, в одном эксперименте можно определить влияние ксенобиотика на несколько элементов иммунной реакции (фагоцитоз, выработку антител, клеточный иммунитет). Вызванные токсикантом повреждения фагоцитоза, либо антителообразования, либо механизмов клеточного иммунитета, проявляются паразитемией в соответствующем периоде развития инфекции. Эта модель достаточно чувствительна и эффективна при оценке иммуносупрессорных свойств ксенобиотиков.
Оценка потенциальной способности веществ сенсибилизировать организм проводится в опытах на лабораторных животных, как правило, на морских свинках. В настоящее время используются три группы тестов: Draize; Buehler; Magnusson-Kligman. Тесты различаются способами введения токсикантов: внутрикожное, накожное и подкожное, соответственно; используемыми в исследовании адъювантами, промежутками времени между сенситизацией и провокацией реакции. В настоящее время как наиболее специфичный и точный рассматривается тест Magnusson-Kligman. С методикой проведения исследований можно познакомиться в специальной литературе.
5. Выявления иммунотоксических эффектов
Не смотря на многочисленные данные об иммунотоксических свойствах веществ, получаемых на экспериментальных животных, в силу сложности экстраполяции, сведения о влиянии веществ на человека порой противоречивы. Кроме того далеко не у всех лиц, с признаками иммунотоксического поражения органов (гломерулонефрит, пневмониты, астма, аллергические дерматиты, гепатиты и т.д.) удается легко выявить химическую природу этиологического фактора, определить источник воздействия. Достаточно сложно отличить дисфункцию системы, как следствие какого либо заболевания или недостаточности питания, от химически обусловленной патологии. Поэтому для выявления иммунотоксичности вслед за этапом оценки иммунного статуса обследуемых лиц, должен следовать этап поиска доказательства причинно-следственных связей между выявленными нарушениями и действием токсиканта.
Исследования должны начинаться с тщательного обследования и сбора анамнеза. Необходимо особое внимание уделять выявлению классических проявлений и симптомов иммунных нарушений. Сложные лабораторные тесты могут обеспечить детальную информацию о состоянии гуморального и клеточного компонентов иммунитета, комплемента, фагоцитарных функциях, однако проведение этих тестов в подавляющем большинстве случаев совершенно излишне. Для оценки состояния иммунной системы часто вполне достаточно использовать простые скрининговые методы. Необходимо иметь в виду, что вследствие высокой лабильности иммунной системы, получаемые в ходе обследования результаты, характеризуют её состояние только в данный момент времени.
5.1. Оценка иммунологического статуса
Для оценки статуса человека с предполагаемой иммунной патологией Иммунологическая секция ВОЗ рекомендует использовать тесты, представленные на таблице 11.
Таблица 11. Тесты клинического иммунологического скрининга
| - Подсчет числа форменных элементов крови. Формула крови - Количественный электрофорез плазмы крови |
| Гуморальный иммунитет: - Количество иммуноглобулинов (IgG, IgM, IgA, IgE) - Титры изоантител |
| Клеточный иммунитет: - Кожные тесты на отсроченную гиперреактивность |
| Аутоиммунный процесс: - Титр аутоантител |
Эти исследования следует проводить перед тем, как переходить к более сложным и дорогим диагностическим процедурам (таблицы 12, 13).
Талица 12. Методы оценка состояния гуморального иммунитета
| Функция иммуноглобулинов: - электрофорез белков - количество иммуноглобулинов в плазме крови - титр специфических антител (изогаммаглобулины, антистрептолизин О, антитела к возбудителям свинки, кори, полиомиелиту) - антигенный ответ: - первичное антителообразование - вторичное антителообразование Функция В-лимфоцитов: - количество В-лимфоцитов с поверхностными иммуноглобулинами (нормальное содержание 4 -10%) - активация В-лимфоцитов (реакция на митогены, инактивированные антигены, индукцию клеточного деления) - пролиферация В-лимфоцитов (измерение интенсивности пролиферации путём изучения скорости инкорпорации тимидина, меченого тритием) - дифференциация В-лимфоцитов (определение колоний антителосекретирующих клеток или определение количества антител в супернатанте культуры клеток; определение продукции иммуноглобулинов индуцированной митогенами Т- и В-лимфоцитов) |
Таблица 13. Методы оценка состояния клеточного иммунитета
| Подсчёт лимфоцитов Тесты на трансформацию лимфоцитов: - стимуляция митогенами - воздействие антигенов - смешанная культура лимфоцитов Определение лимфокинов: - фактор ингибирования макрофагов - фактор угнетения миграции лимфоцитов - лимфоцитарный хемотаксический фактор Кожные тесты на отсроченную гиперчувствительность (антигены: свинка, трихофитон, тетанотоксоид и др.) Лимфоцитарная цитотоксичность, активность естественных киллеров Субпопуляции Т-клеток: соотношение хелперы/супрессоры |
Электрофорез белков позволяет быстро установить нормально ли у обследуемого содержание иммуноглобулинов, нет ли дисгаммаглобулинемии. Гипогаммаглобулинемия обычно является следствием вторичного иммунного дефицита. Определение иммуноглобулинов даёт прямую информацию о наличии или отсутствии моноклональной или поликлональной гаммаглобулиноапатии. Основными типами иммуноглобулинов являются IgG, IgM, IgA, IgE их определение оправдано в тех случаях, когда частью клинического синдрома является аллергический компонент. Определение специфичных антител методологически сложно (методы энзимсвязанной иммуносорбции). Наиболее часто развивается дефицит IgA, причем в 50% случаев при этом отсутствуют признаки патологии. Функция этого иммуноглобулина - защита слизистых барьеров организма от инфекции.
Нарушение клеточного иммунитета можно выявить, ориентируясь на симптомы заболеваний, ассоциирующихся с функциями этого механизма резистентности. Как известно, к числу таких функций относятся: уничтожение внутриклеточных патогенных организмов, отторжение опухолевых клеток, отсроченные реакции гиперреактивности, в том числе контактные дерматиты, аутоиммунное повреждение органов и тканей. Наиболее часто дефицит клеточного иммунитета проявляется учащением инфекционных заболеваний вирусной и грибковой этиологии.
Любое уменьшение числа Т-лимфоцитов, выявляемое при подсчете формулы крови, до уровня 75 - 85% от нормального значения, называется лимфопенией. Определение числа Т-лимфоцитов различных типов производится путем подсчета розеток, образуемых с эритроцитами барана и с помощью флюоресцирующих моноклональных антител к зрелым Т-лимфоцитам.
Тест на трансформацию лимфоцитов можно провести in vitro с использованием митогенов (фитогемагглютинин и др.) и растворимых антигенов, добавляя их к культуре клеток.
Дата публикования: 2014-11-04; Прочитано: 304 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
