 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Классификация совмещенных процессов
|
|
Совмещенные процессы [7] можно разделить[*] на:
- однородные совмещенные процессы;
- неоднородные совмещенные процессы.
К однородным относятся сложные процессы, базирующиеся на совмещении двух или более процессов, принадлежащих к одному классу. Например, направленное совмещение в одном аппарате двух и более реакций; двух или более массообменных процессов и т.д.
К неоднородным относятся сложные процессы, базирующиеся на совмещении двух или более процессов, принадлежащих к разным классам. К этой группе относятся реакционно-массообменные, совмещенные гидромеханические и механические процессы и другие.
Отметим, что совмещенные процессы могут быть направленно совмещенными и самопроизвольно совмещенными.
К направленно совмещенным будут относиться те процессы, где совмещение организуется целенаправленно специальными приемами и методами. Самопроизвольно совмещенные процессы характеризуются тем, что какой-либо из составных процессов протекает спонтанно в условиях проведения другого процесса.
Определяя пространственно-временной контур, соответствующий границе одного аппарата и количеству потоков в единицу времени, составим в общем виде уравнение материального баланса для компонента i(продукт реакции):
Пi - Уi + Ui - Ci = Hi [кмоль/с], (6)
где Пi - количество компонентаi, поступающего в систему (приход);
Уi - количество компонентаi, уходящего из системы (уход);
Ui - количество компонентаi, образующегося в системе (источник);
Ci - количество компонентаi, расходуемого в системе (сток);
Hi – накопление компонентаiв системе.
Для продукта реакции в стационарном режиме работы аппарата соблюдается условие:
Пi = Ci = Hi = 0. (7)
Следовательно Ui - Уi = 0. (8)
Если в выводимом потоке мольная доля компонента i близка к единице (селективность системы высока), то
Уi» У,(9)
где У - суммарное количество (расход) отводимого потока.
Для случая нескольких продуктов реакции:
å Уi» У. (10)
Таким образом, в совмещенном реакционно-массообменном процессе количество компонентаi, образующегося в системе в единицу времени (мощность источникаi), должно быть равным количеству этого компонента, выводимому из системы в единицу времени. С учетом избирательного обмена через границу системы компонент i удаляется из системы в практически чистом виде. Уравнение (7) относится к случаю, когда принцип совмещения позволяет преодолеть термодинамические ограничения по химической составляющей с помощью избирательного массообмена рассматриваемой системы с окружающей средой.
Возможен и другой случай, которому соответствует система уравнений:
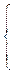 Пi = Hi = Уi = 0
Пi = Hi = Уi = 0
Ui- Ci =0(11)
В этом случае компонент i не пересекает границ системы (Ui = Ci). Т.е. термодинамические ограничения целевой химической составляющей преодолеваются за счет стока компонента i путем организации другой химической реакции, в которой он расходуется. Здесь сток должен обладать избирательностью относительно компонента i. Система уравнений (11) соответствует сложному реакционно-реакционному процессу, в котором возможен селективный вывод нескольких продуктов реакции через границы системы.
Наконец, возможен случай, который характеризуется следующей системой уравнений:
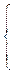 Уi = Ui = Hi = 0
Уi = Ui = Hi = 0
Пi - Ci =0(12)
Здесь количество компонентаi, поступающего в систему в единицу времени равно стоку этого вещества внутри системы. Например, такой случай характерен для задачи выделения из многокомпонентной смеси одного из компонентов. Причем в результате термодинамических ограничений выделение такого компонента затруднительно (фазовое равновесие характеризуется малыми относительными летучестями или образованием азеотропов). Одним из возможных путей решения проблемы является добавление в разделяемую смесь вещества, образующего с целевым продуктом химическое соединение, сравнительно легко выделяемое из многокомпонентной смеси. Выделение полученного при этом продукта может быть осуществлено в режиме реакционно-массообменного процесса, т.е. химическое превращение будет сопровождаться одновременным выделением реакционной смеси. Вместе с тем для выделения целевого продукта потребуется вторая ступень, на которой будет осуществлена обратная реакция с получением целевого продукта и реагента, который будет возвращен в первый массообменный аппарат. Таким образом, оба аппарата образуют некоторый комплекс с обратной связью, в котором осуществляется в две ступени совмещенный реакционно-массообменный процесс, позволяющий преодолеть термодинамические ограничения как по химической составляющей, так и по массообменной. В качестве примеров рассмотрим несколько реакционно-массообменных процессов.
Дата публикования: 2015-11-01; Прочитано: 1287 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
