 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Основи молекулярно-кінетичної теорії речовини
|
|
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
ЧЕРКАСЬКИЙ ДЕРЖАВНИЙ ТЕХНОЛОГІЧНИЙ УНІВЕРСИТЕТ
„Затверджено”
на засіданні кафедри фізики
протокол №___ від „____” __________ 2009 р.
Тираж ____ примірників
Вимогам, що ставляться до
навчально-методичних видань, відповідає
Зав. кафедри фізики Ващенко В.А. ___________
ПРАКТИКУМ З ФІЗИКИ
Для студентів інженерних спеціальностей
Частина ІІ. Молекулярна фізика.
Весь цифровий і фактичний матеріал та бібліографічні
відомості перевірено. Зауваження рецензента враховано
Зав. кафедри фізики ________________ Ващенко В.А., д.т.н., професор
Укладачі: ________________ Ващенко В.А., д.т.н., професор
________________ Колінько С.О., к.ф-м.н., доцент
________________ Рудь М.П.
________________ Нетребчук Л.К.
________________ Бутенко Т.І., к.т.н., доцент
________________ Бондаренко М.О., к.т.н., доцент
Відповідальний редактор ____________ Ващенко В.А., д.т.н., професор
Рецензент: ________________ Прямухін В.Є., к.ф-м.н, доцент
Відповідальний за випуск ____________ Колінько С.О., к.ф-м.н., доцент
Черкаси ЧДТУ 2009
УДК 539.1
ББК 22.36
П 69
Укладачі: Ващенко В‘ячеслав Андрійович, д.т.н, професор,
Колінько Сергій Олександрович, к.ф-м.н., доцент,
Рудь Максим Петрович,
Нетребчук Лідія Кузьмівна,
Бутенко Тетяна Іванівна, к.т.н., доцент,
Бондаренко Максим Олексійович, к.т.н., доцент
Рецензент: Прямухін В.Є., к.ф-м.н, доцент
Практикум з фізики для студентів інженерних спеціальностей. Частина ІІ "Молекулярна фізика" / Укл. В.А.Ващенко, С.О.Колінько, М.П. Рудь, Л.К.Нетребчук, Бутенко Т.І., Бондаренко М.О. – Черкаси, ЧДТУ, 2009. – 70 с.
Практикум призначений для самостійного оволодіння студентами практичними навичками шляхом розв’язування задач з фізики із розділу „Молекулярна фізика”. Кількість запропонованих задач (498) така, що дозволяє скласти різні варіанти завдань різної складності для академічної групи студентів. Всі задачі оцінені за рівнем складності (А, В, С). У виданні міститься достатній теоретичний і довідковий матеріал, що позбавляє необхідності звертатися до різних довідників.
Видання призначене для студентів інженерних спеціальностей.
УДК 539.1
ББК 22.36
ПЕРЕДМОВА
В останній час все більше уваги приділяється самостійній роботі студентів, а також посиленню індивідуального підходу до навчання студентів. Такі тенденції вимагають відповідного методичного забезпечення. Зокрема, вивчення фізики неможливе без розв'язування задач. Фізичні задачі сприяють закріпленню теоретичного матеріалу курсу, допомагають зрозуміти зміст фізичних законів, закріпити в пам'яті формули, прищеплюють навички практичного застосування теоретичних знань, розвивають творчі здібності і формують фізичне мислення.
Пропонований практикум з фізики є другою частиною запланованого кафедрою фізики ЧДТУ комплексу практикумів з усіх розділів загальної фізики для студентів інженерно-технічних спеціальностей вищих навчальних закладів. Практикум призначений для самостійного оволодіння студентами практичними навичками шляхом розв'язування задач по фізиці із розділу "Молекулярна фізика". Кількість запропонованих задач (498) така, що дозволяє скласти різні варіанти завдань різної складності для академічної групи студентів. Всі задачі оцінені по рівню складності:
А (прості) - розрахункові задачі, які вимагають знання основних формул і одиниць вимірювання фізичних величин;
В (середні) - тематичні задачі і вправи, які потребують розуміння суті фізичних явищ;
С (середні) - комбіновані і аналітичні задачі, які вимагають поєднання знань із різних тем і уміння аналізувати умову і отриманий розв'язок задачі.
Видання, окрім тексту задач, містить достатній теоретичний і довідковий матеріал, що позбавляє необхідності звертатися до різних довідників. Безпосередньо після умови кожної задачі приводиться відповідь до неї, що дозволяє студенту самостійно оцінювати правильність розв'язання свого завдання.
Література, яка використана для укладання практикуму, наведена в кінці видання.
Основи молекулярно-кінетичної теорії речовини
Кількість речовини однорідного газу (в молях):
n= 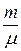 ,
,
де m – маса газу; m - молярна маса газу.
Один моль різних речовин містить однакову кількість молекул (стала Авогадро):
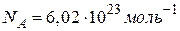
Рівняння Клапейрона-Менделєєва (рівняння стану ідеального газу):
pV = 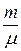 RT = nRT,
RT = nRT,
де Р – тиск газу; V – об’єм газу; R – універсальна газова стала, 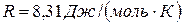 ; Т – термодинамічна температура.
; Т – термодинамічна температура.
Дослідні газові закони, які є частковими випадками рівняння Клапейрона-Менделєєва для ізопроцесів:
а) закон Бойля-Маріотта (ізотермічний процес: Т = const; m = const):
pV = const,
або для двох станів газу: p1V1 = p2V 2, де p1 і V1 – і об’єм в початковому стані; p2 і V2 – ті ж величини в кінцевому стані;
б) закон Гей – Люссака (ізобаричний процес: p=const, m=const):
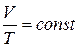 ,
,
або для двох станів:
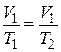 ,
,
де V1 і T1 об’єм і температура газу в початковому стані;
V2 і T2 – в кінцевому стані;
в) закон Шарля (ізохоричний процес: V = const, m = const);
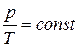 ,
,
або для двох станів, 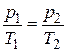 , де р1 і Т1 – тиск і температура газу в початковому стані; р2 і Т2 – ті ж величини в кінцевому стані;
, де р1 і Т1 – тиск і температура газу в початковому стані; р2 і Т2 – ті ж величини в кінцевому стані;
г) об’єднаний газовий закон (m = const):
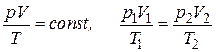 ,
,
де р1, V1, Т1 – тиск, об’єм і температура газу в початковому стані.
Тиск суміш газів (закон Дальтона):
p = р1 + р2 + …рn,
де рі – парціальні тиски компонентів суміші; n – число компонентів суміші.
Концентрація молекул (число молекул в одиниці об’єму):
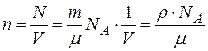 ,
,
де N – число молекул речовини,
r – густина речовини, V – об’єм речовини.
Основне рівняння кінетичної теорії газів:
Р = 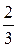 n
n 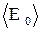 ,
,
де 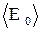 середня кінетична енергія молекули.
середня кінетична енергія молекули.
Середня кінетична енергія молекули:
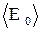 =
= 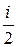 kT,
kT,
де і – число ступенів вільності молекули, k – стала Больцмана.
Залежність тиску газу від концентрації молекул і температури:
p = nkT.
Швидкості молекул:
середня квадратична 
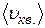 =
= 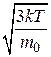 =
= 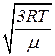 ;
;
середня арифметична 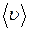 =
= 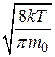 =
= 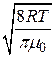 ;
;
найбільш імовірна 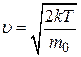 =
= 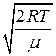 ,
,
де m0 - маса однієї молекули.
Барометрична формула визначає залежність тиску газу від висоти в полі сили тяжіння
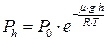
де 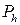 – тиск газу на висоті h,
– тиск газу на висоті h, 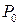 – тиск на висті h=0, g – прискорення вільного падіння.
– тиск на висті h=0, g – прискорення вільного падіння.
5.1. (A) Яку температуру мають 2 г азоту, що займає, об'єм 820 см3 при тиску в 2∙105 Па?
Відповідь: T = 280 К = 7 °С
5.2. (A) Який об'єм займають 10 г кисню при тиску 105 Па і температурі 20° С?
Відповідь: V =7,6∙10-3 м3.
5.3. (A) Балон місткістю 12 л наповнений азотом при тиску 8,1·106 Па і температурі 17° С. Яка кількість азоту знаходиться в балоні?
Відповідь: m=1,13 кг.
5.4. (A) Який тиск на стінки посудини чинять 0,02 кг кисню, що займає об'єм 0,2 м3 при температурі 40° С? Як зміниться результат, якщо замість кисню (О2) в тій же посудині буде водень (Н2)?
Відповідь: 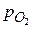 = 0,814∙104 Па.
= 0,814∙104 Па.
5.5. (A) Скільки метану (СН4) знаходиться в балоні об’ємом 15 дм3 при тиску 106 Па і температурі 27°С?
Відповідь: 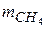 = 0,0963 кг.
= 0,0963 кг.
5.6. (A) При якій температурі кисень (О2), знаходячись під тиском 0,2∙106 Па, має густину 1,2 кг/м3?
Відповідь: Т ≈ 642 К.
5.7. (В) В зварювальному цеху стоїть 40 балонів ацетилену (С2Н2) об’ємом по 40 дм3 кожний. Всі балони включені в загальну магістраль. Після 12 год безперервної роботи тиск у всіх балонах впав з 1,3∙107 Падо 0,7∙107 Па. Визначити витрату ацетилену за 1 хв, якщо температура в цеху залишалася незмінною і дорівнювала 32° С.
Відповідь: m = 0,139 кг/хв.
5.8. (В) При нагріванні ідеального газу на ΔT = 1 К при постійному тиску об'єм його збільшився на 1/350 початкового об'єму. Знайти початкову температуру Т газу.
Відповідь:350 К.
5.9. (A) Тиск повітря всередині щільно закупореної пляшки при температурі 7° С дорівнював 105 Па. При нагріванні пляшки пробка вилетіла. Знайти, до якої температури нагріли пляшку, якщо відомо, що пробка вилетіла при тиску повітря в пляшці, рівному 1,3∙105 Па.
Відповідь: T = 364 К = 91°С.
5.10. (A) Яким може бути найменший об'єм балона, що містить 6,4 кг кисню, якщо його стінки при температурі 20° С витримують тиск в 1600 Н /см2?
Відповідь: V = 3,1∙10-2 м3 .
5.11. (A) В балоні знаходилося 10 кг газу при тиску 107 Па. Знайти, яку кількість газу узяли з балона, якщо тиск став рівний 2,5·106 Па. Температуру газу вважати постійною.
Відповідь: 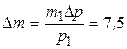 кг.
кг.
5.12. (A) Знайти масу сірчистого газу (SO2), що займає об'єм 25 л при температурі 27° С і тиску 105 Па.
Відповідь: m = 0,065 кг.
5.13. (A) Знайти масу повітря, яке заповнює аудиторію заввишки 5 м і з площею підлоги 200 м2. Тиск повітря 105 Па, температура приміщення 17° С. (Масу одного кіломоля повітря прийняти рівною 29 кг/моль.)
Відповідь: m = 1200 кг.
5.14. (A) В скільки разів маса повітря, що заповнює приміщення взимку (7° С), більше його маси влітку (37° С)? Тиск однаковий.
Відповідь: в 1,1 раза.
5.15. (A) Накреслити ізотерми 0,5 г водню для температур: 1) 0° С, 2) 100° С.
Відповідь: 1) 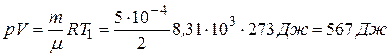 . (1)
. (1)
2) 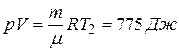 . (2)
. (2)
Задаючи різні значення V по рівняннях (1) і (2), отримаємо відповідні значення р.
5.16. (В) Циліндр розділено рухомим поршнем на дві частини, об'єми яких відносяться, як 1:2. Обидві частини циліндра заповнено газом при однаковій температурі. Знайти рівноважне положення поршня, якщо газ в першій частині циліндра нагрівається до температури 127° C, а інша частина має температуру –73° C.
Відповідь: Поршень на середині.
5.17. (В) Дві кулі об’ємом 1 л кожна сполучено трубкою завдовжки 1 м і діаметром 6 мм. При температурі 0°С крапля ртуті знаходиться в рівновазі посередині трубки. На скільки зміститься крапля ртуті, якщо праву кулю нагріти на 2°, а ліву охолодити на 3°?
Відповідь: l = 33,0 см.
5.18. (С) В деякому об'ємі міститься 18 кг суміші газів: 5 кг водню, 7 кг вуглецю, 2 кг вуглекислого газу, а інше азот. Температура суміші 18° С і тиск 98420 Па. Визначити густину суміші і парціальні тиски газів.
Відповідь: ρ = 0,246 кг/м3; 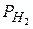 = 8430 Па.
= 8430 Па.
5.19. (С) Куля об’ємом 1000 л наповнена воднем при температурі 27° С і тиску 117,72 МПа. Визначити висоту, на яку може піднятися куля, якщо її оболонка важить 0,3 кг і при піднятті на 100 м тиск падає на 1330 Па, а температура знижується на 0,4° C.
Відповідь: Н = 5,5 км.
5.20. (A) Накреслити ізотерми 15,5 г кисню для температур: 1) 29° С і 2) 180° С.
Відповідь: 1) 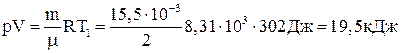 . (1)
. (1)
2) 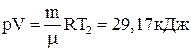 . (2)
. (2)
Задаючи різні значення V по рівняннях (1) і (2), отримаємо відповідні значення р.
5.21. (С) Зобразити для ідеального газу приблизні графіки ізохорного, ізобарного, ізотермічного та. адіабатного процесів на діаграмах: а) р, V; б) V, Т.
5.22. (С) На площині V, Т зображено процес, який відбувся з газом при постійному тиску і постійному об'ємі. Як при цьому змінилася маса газу.
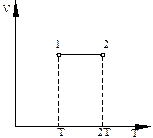
Відповідь: Зменшилась вдвічі.
5.23. (С) На р, Т-діаграмі показаний процес, над ідеальним газом. Об'єм газу постійний. Знайдіть точки, де маса газу максимальна, а де мінімальна.
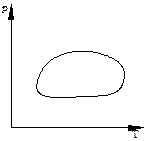
5.24. (С) На V, Т-діаграмі показаний замкнутий процес над газом. Зобразіть цей процес в координатах р, V.

5.25. (A) Яка кількість кіломолей газу знаходиться в балоні об'ємом 10 м3 при тиску 9,6∙104 Па і температурі 17° С?
Відповідь: 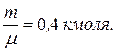
5.26. (С) Скільки накачувань треба зробити, щоб за допомогою насоса, захоплюючого при кожному накачуванні 40 см3 повітря, наповнити порожню камеру шини велосипеда настільки, щоб площа її дотику з дорогою була рівна 60 см2. Навантаження на колесо рівне 35 кг. Об'єм камери рівний 2000 см3. Тиск атмосфери прийняти рівним 0,98 ∙105 Па. Жорсткістю покришки камери знехтувати.
Відповідь: 79.
5.27. (A) Газ при тиску 99,085 ∙103 Па і при температурі 20° С має об'єм 164 см3. Який об'єм тієї ж маси газу за нормальних умов?
Відповідь: 150 см3.
5.28. (В) Балон ємністю 20 л наповнений стиснутим повітрям. При температурі 20° С манометр показує тиск 117,72 ∙105 Па. Який об'єм води можна витіснити з цистерни підводного човна повітрям цього балона, якщо витіснення проводиться на глибині 30 м і температурі 5° С?
Відповідь: 554 л.
5.29. (В) З балона із стислим воднем об’ємом 10 л унаслідок несправності вентиля витікає газ. При температурі 7° С манометр показував 49 ∙105 Па. Через деякий час при температурі 17° С манометр показав такий же тиск. Скільки витекло газу?
Відповідь: 1,48 г.
5.30. (С) По газопровідній трубі йде вуглекислий газ при тиску р = 3,9 ∙105 Па і температурі t=7° С. Яка швидкість руху газу в трубі, якщо за τ =10 хвпротікає т = 2 кг вуглекислого газу і якщо площа перерізу каналу труби S = 5 см2?
Відповідь: 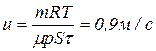 .
.
5.31. (A) 5 г азоту, що знаходиться в закритій посудині об'ємом 4 л при температурі 20° С, нагріваються до температури 40° С. Найти тиск газу до і після нагрівання.
Відповідь: p1 = 1,08∙105 Па; р2 = 1,16∙105 Па.
5.32. (С) Посередині відкачаного і запаяного з обох кінців горизонтального капіляра знаходиться стовпчик ртуті завдовжки l=20 см. Якщо капіляр поставити вертикально, то стовпчик ртуті переміститься на відстань l= 10 см. До якого тиску був відкачаний капіляр? Довжина капіляра L=1 м.
Відповідь: p 0 =49875 Па.
5.33. (С) Загальновідоме жартівливе питання: "Що важче: тонна свинцю чи тонна пробки?" Підрахувати, наскільки маса пробки, яка в повітрі важить 9,8 кН, більша маси свинцю, який в повітрі важить також 9,8 кН. Температураповітря 17° С, тиск 105 Па, ρ св=11300 кг/м3, ρ пр=200 кг/м3.
Відповідь: ΔP = 58,6 Н.
5.34. (С) Якою повинна бути маса оболонки дитячої повітряної кульки діаметром 25 см, наповненої воднем, щоб результуюча підйомна сила кульки була рівна нулю, тобто, щоб кулька знаходилася в підвішеному стані? Повітря і водень знаходяться за нормальних умов. Тиск усередині кульки дорівнює зовнішньому тиску.
Відповідь: m = 9,8∙10-3 кг.
5.35. (A) Знайти густину водню при температурі 15° С і тиску в 9,7∙104 Па.
Відповідь: ρ = 0,081 кг/м3.
5.36. (A) Густина деякого газу при температурі 10° С і тиску в 2∙105 Па дорівнює 0,34 кг/м3. Чому дорівнює маса одного кіломоля цього газу?
Відповідь: μ = 4 кг/кмоль.
5.37. (А) Чому дорівнює густина повітря в посудині, якщо посудина відкачана до найвищого розрідження, яке досягнуте сучасними лабораторними способами (р= 10-9 Па)? Температура повітря 15° С.
Відповідь: ρ = 1,6∙10-14 кг/м3.
5.38. (В) 12 г газу займають об'єм 4·10-3 м3 при температурі 7° С. Після нагрівання газу при постійному тиску його густина стала рівна 6·10-4 г/см3. До якої температури нагріли газ?
Відповідь: до температури 1400 К.
5.39. (С) Об'єм повітряної бульбашки по мірі її спливання з дна озера на поверхню збільшується в n раз. Яка глибина озера? Зміною температури з глибиною можна нехтувати.
Відповідь: 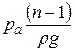 , де
, де 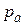 - атмосферний тиск, ρ – густина води.
- атмосферний тиск, ρ – густина води.
5.40. (С) Відкрита з двох кінців трубка завдовжки 0,76 м до половини занурена в ртуть. Скільки ртуті залишиться в трубці, якщо, щільно закривши верхній отвір, вийняти трубку з ртуті?
Відповідь: 30 см.
5.41. (В) У вертикально розташованому циліндрі під невагомим рухомим поршнем знаходиться повітря. На поршень ставлять гирю масою 10 кг. На скільки переміститься поршень, якщо температура повітря в циліндрі підтримується постійною? Атмосферний тиск 105 Па, площа перерізу поршня 100 см2, відстань від ненавантаженого поршня до дна циліндра 100 см.
Відповідь: 8,9 см.
5.42. (С) Циліндричний стакан опущений отвором вниз у воду і плаває в ній так, що внутрішня поверхня дна знаходиться на одному рівні з поверхнею води в посудині. Маса стакана 400 г, площа його дна 10 см2, тиск повітря в стакані перед зануренням 101,08 кПа. Яку частину стакана займатиме повітря після занурення?
Відповідь: 0,96.
5.43. (С) Посудина розділена рухомим поршнем на об'єми V/3 і 2V/3, що містять газ з температурою Т. До якої температури потрібно нагрівати газ зліва від поршня, щоб відношення об'ємів змінилося на зворотне? Справа температура газу підтримується постійною.
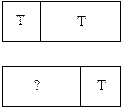
Відповідь: 4Т.
5.44. (В) До якої температури слід нагріти ізобарично газ, щоб його густина зменшилася в 2 рази порівняно з густиною при 0 °С?
Відповідь: 546 К.
5.45. (С) Повітря знаходиться у відкритій зверху вертикальній циліндричній посудині під поршнем масою 20 кг і перерізом 20 см2. Після того, як посудину стали рухати вгору з прискоренням 5 м/с2, висота стовпа, повітря між поршнем і дном посудини зменшилася на 20 %. Вважаючи температуру постійною, знайдіть за цими даними атмосферний тиск. Тертям між поршнем і стінками посудина можна знехтувати.
Відповідь: 105 Па.
5.46. (В) В посудині знаходиться озон при температурі 527 °С. Через якийсь час він повністю перетворився на кисень, а температура в посудині впала до 127° С. На скільки відсотків змінився при цьому тиск газу?
Відповідь: зменшився на 25%.
5.47. (В) Гумова куля містить 2 л кисню при температурі 20 °С і атмосферному тиску 100 кПа. Визначте масу кисню в кулі. Який об'єм займе кисень, якщо кулю опустити у воду на глибину 10 м і охолодити до температури води 4 °С? Тиск усередині кулі вважайте рівним тиску зовні кулі.
Відповідь: 2,6 г.
5.48. (С) В чашковий ртутний барометр потрапило повітря, в результаті чого за нормальних умов барометр показує 98,42 кПа, а відстань від рівня ртуті в трубці до запаяного кінця складає 10 см. Чому дорівнює істинне значення атмосферного тиску, якщо при температурі 20 °С барометр показує 97,09 кПа? Тепловим розширенням ртуті, і трубки можна знехтувати.
Відповідь: 99,75 кПа.
5.49. (С) Тонкостінна гумова куля масою 50 г наповнена азотом і занурена в озеро на глибину 100 м. Знайдіть масу азоту, якщо куля знаходиться в рівновазі. Атмосферний тиск 101,08 кПа, температура в глибині озера 4 °С. Натягом гуми можна знехтувати.
Відповідь: 0,67 г.
5.50. (С) Визначте підйомну силу повітряної кулі об'ємом 100 м3, наповненої гарячим повітрям при температурі 147 °С. Куля сполучається з атмосферою. Температура зовнішнього повітря 27 °С, його тиск 93,1 кПа.
Відповідь: 300 Н.
5.51. (С) Чи зможе повітряна куля, наповнена гелієм, утримувати вантаж масою 100 кг, якщо об'єм кулі 150 м3, а маса оболонки 8 кг? Тиск і температура гелію усередині кулі і повітря зовні однакові і рівні відповідно 105 Па і 15 °С.
Відповідь: так.
5.52. (С) В балоні об'ємом 10 л міститься водень при температурі 20 °С під тиском 107 Па. Яку масу водню випустили з балона, якщо при повному згоранні газу, що залишився, утворилося 50 г води?
Відповідь: 77 г.
5.53. (С) В циліндричну посудину, що лежить на боку на горизонтальній поверхні, починають поволі всувати з відкритого кінця гладкий поршень. Знайдіть тиск повітря в посудині в той момент, коли посудина зсунеться з місця. Маса посудини разом з поршнем 2 кг, площа поршня 6 см2, атмосферний тиск 100 кПа, коефіцієнт тертя між горизонтальною поверхнею і посудиною 0,3.
Відповідь: 110 кПа.
5.54. (С) Електрична газонаповнена лампа розжарювання, об'єм якої V = 500 см3, наповнена азотом під тиском р = 9∙104 Па. Яка маса води m увійде в лампу, якщо у ній зробити отвір під водою при нормальному атмосферному тиску?
Відповідь: 0,46 кг.
5.55. (В) Аеростат об'ємом V наповнений воднем при температурі Т1 = 288 К. При сталому атмосферному тиску під впливом сонячної радіації його температура підвищилась до Т2 = 310 К, і надлишок газу вийшов з нього через отвір, внаслідок чого маса аеростата з газом зменшилась на Δm = 6,05 кг. Знайти об’єм аеростата.
Відповідь: 69,7 м3.
5.56. (В) В циліндр завдовжки l = 1,6 м, заповнений повітрям при нормальному атмосферному тиску р0, почали повільно всувати поршень площею S = 200 см2. Визначити силу F, яка діятиме на поршень, якщо його зупинити на відстані l1 = 10 см від дна циліндра.
Відповідь: 32,3 кН.
5.57. (С) Колба об'ємом V = 300 см3, закрита пробкою з краном, містить розріджене повітря. Для вимірювання тиску в колбі шийку колби сполучили з водою на незначну глибину і відкрили кран, внаслідок чого до колби увійшла вода масою т = 292 г. Визначити початковий тиск р в колбі, якщо атмосферний тиск р0 = 100 кПа.
Відповідь:2,66 кПа.
5.58. (A) В балоні міститься газ при температурі t1 = 100° С. До якої температури t2 потрібно нагріти газ, щоб його тиск збільшився в два рази?
Відповідь: 473° С.
5.59. (С) Порожнисту кулю об'ємом V = 10 см3, заповнену повітрям при температурі T1 = 573 К, з'єднали трубкою з чашкою, заповненою ртуттю. Визначити масу m ртуті, що увійшла до кулі при охолодженні повітря в ній до температури Т2 = 293 К. Зміною об'єму кулі знехтувати.
Відповідь: 66,4 г.
5.60. (С) Оболонка повітряної кулі об'ємом V = 800 м3 цілком заповнена воднем при температурі T1 = 273 К. На скільки зміниться підйомна сила кулі при підвищенні температури до Т2 = 293 К? Вважати об'єм V оболонки незмінним і зовнішній тиск нормальним. В нижній частині оболонки є отвір, через який водень може виходити в оточуючий простір.
Відповідь: зменшиться на 642 Н.
5.61. (С) Газовий термометр складається з кулі з припаяною до нього горизонтальною скляною трубкою. Крапелька ртуті, поміщена в трубку, відділяє об'єм кулі від зовнішнього простору. Площа S поперечного перерізу трубки рівна 0,1 см2. При температурі Т1 = 273 К крапелька знаходилася на відстані l1 = 30 см від поверхні кулі, при температурі Т2 = 278 К – на відстані l2 = 50 см. Знайти об'єм V кулі.

Відповідь:106 см3.
5.62. (С) Оболонка повітряної кулі має об'єм V = 1600 м3. Знайти підйомну силу F водню, що наповнює оболонку, на висоті, де тиск р = 60 кПа і температура Т = 280 К. При підйомі кулі водень може виходити через отвір в нижній частині кулі.
Відповідь:10,9 кН.
5.63. (В) В балоні об'ємом V = 25 л знаходиться водень при температурі Т = 290 К. Після того як частину водню витратили, тиск в балоні знизився на Δр = 0,4 МПа. Визначити масу m витраченого водню.
Відповідь: 8,3 г.
5.64. (С) Суміш газів, що перебуває під тиском р = 1,02∙105 Па, містить m1 = 16 г кисню та m2 = 4 г гелію. Температура суміші T = 280 К. Знайти концентрацію молекул суміші та її густину.
Відповідь: 2,6∙1025 м-3; 0,584 кг/м3.
5.65. (С) У посудині об'ємом V = 20 л міститься m1 = 5 г водню та m2 = 10 г азоту при температурі T = 290 К. Визначити тиск у посудині, молярну масу та густину суміші газів.
Відповідь: 3,44∙105 Па; 5,25∙10-3 кг/моль; 0,75 кг/м3.
5.66. (В) В закритій посудині ємністю 2 м3 знаходяться 1,4 кг азоту (N2) і 2 кг кисню (О2). Знайти тиск газової суміші в посудині, якщо температура суміші t = 27° С.
Відповідь: рсм = 1,4∙105 Па.
5.67. (В) В балоні ємністю 2 м3 міститься суміш азоту (N2) і окислу азоту (NO). Визначити масу окислу азоту, якщо маса суміші рівна 14 кг, температура 300К і тиск 0,6∙106 Па.
Відповідь: m = 13,5 кг.
5.68. (С) В посудині при температурі t = 100 ° С і тиску р = 4∙105 Па знаходиться 2 м3 суміші кисню О2 і сірчистого газу SO2. Визначити парціальний тиск компонентів, якщо маса сірчистого газу 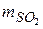 = 8 кг.
= 8 кг.
Відповідь: 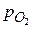 = 2,1∙105 Па;
= 2,1∙105 Па; 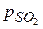 = 1,9∙105 Па.
= 1,9∙105 Па.
5.69. (В) Який об'єм V займає суміш газів – азоту масою m1= 1 кг і гелію масою m2= 1 кг – за нормальних умов?
Відповідь: 6,4 м3.
5.70. (В) В посудині об'ємом V = 0,01 м3 міститься суміш газів – азоту масою m1 = 7 г і водню масою т2 = 1 г – при температурі Т = 280 К. Визначити тиск р суміші газів.
Відповідь: 175 кПа.
5.71. (С) Знайти густину ρ газової суміші водню і кисню, якщо їх масові частки ω1 і ω 2 рівні відповідно 1/9 і 8/9. Тиск р суміші рівний 100 кПа, температура Т = 300 К.
Відповідь: 0,402 кг/м3.
5.72. (С) Газова суміш, що складається з кисню і азоту, знаходиться в балоні під тиском р = 1 МПа. Визначити парціальні тиски р1 кисню і р2 азоту, якщо масова частка ω 1 кисню в суміші дорівнює 0,2.
Відповідь: 0,18 МПа; 0,82 МПа.
5.73. (С) В 1 кг сухого повітря міститься m1= 232 г кисню і m2= 768 г азоту (масами інших газів нехтуємо) Визначити молярну масу повітря.
Відповідь: 0,0288 кг/моль.
5.74. (С) Балон об'ємом V = 30 л містить суміш водню і гелію при температурі Т = 300 К і тиску р = 828 кПа. Маса m суміші рівна 24 г. Визначити масу m1 водню і масу m2 гелію.
Відповідь: 16 г; 8 г.
5.75. (С) В посудині об'ємом V = 15 л знаходиться суміш азоту і водню при температурі t = 23° С і тиску р = 200 кПа. Визначити маси суміші і її компонентів, якщо масова частка ω 1 азоту в суміші дорівнює 0,7.
Відповідь: 6,87 г; 4,81 г.
5.76. (С) Балон ємністю V = 5 л містить суміш гелію і водню при тиску р = 600 кПа. Маса m суміші рівна 4 г, масова частка ω 1 гелію рівна 0,6. Визначити температуру Т суміші.
Відповідь: 258 К.
5.77. (С) В закритій посудині ємністю 20 л знаходиться водень масою 6 г і гелій масою 12 г. Визначити: 1) тиск; 2) молярну масу газової суміші в посудині, якщо температура суміші Т = 300 К.
Відповідь: 1) p = 0,75 кПа; 2) μ = 3 ∙10-3 кг/моль.
5.78. (В) Визначити густину суміші газів водню масою m1 = 8 г та кисню масою m2 = 64 г при температурі Т = 290 К і при тиску 0,1 МПа.
Відповідь: 0,498 кг/м3.
5.79. (С) Балон ємністю V = 20 л містить суміш водню і азоту при температурі 290 К і тиску 1 МПа. Визначити масу водню, якщо маса суміші рівна 150 г.
Відповідь: 6,3 г.
5.80. (В) 10 г кисню знаходяться під тиском 3∙105 Па при температурі 10° С. Після розширення унаслідок нагрівання при постійному тиску кисень зайняв об'єм 10 л. Знайти: 1) об'єм газу до розширення, 2) температуру газу після розширення, 3) густину газу до розширення, 4) густину газу після озширення.
Відповідь: 1) 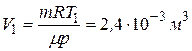 ;
;
2) 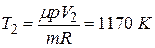 ;
;
3) 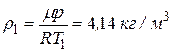 ;
;
4) 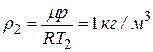 .
.
5.81. (В) В запаяній посудині знаходиться вода, що займає об'єм, рівний половині об'єму посудини. Знайти тиск і густину водяної пари при температурі 400° С, знаючи, що при цій температурі вся вода перетворюється в пару.
Відповідь: p = 1,55∙108 Па; ρ = 500 кг/м3.
5.82. (В) Накреслити графік залежності густини кисню: 1) від тиску при температурі Т= const=390 К (0≤ р ≤4∙105 Пачерез 5∙104 Па ) і 2) від температури при р= const= 4∙105 Па(200 К≤Т≤300 К через 20 К).
Відповідь: 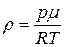 . При Т = const величина
. При Т = const величина 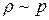 , и при p = const величина
, и при p = const величина 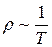 .
.
5.83. (В) В закритій посудині місткістю в 1 м3 знаходиться 0,9 кг води і 1,6 кг кисню. Знайти тиск в посудині при температурі 500° С, знаючи, що при цій температурі вся вода перетворюється на пару.
Відповідь: p = 6,4∙105 Па.
5.84. (В) 6 г вуглекислого газу (СО2) і 5 г закису азоту (N2O) заповнюють посудину об'ємом в 2∙10-3 м3. Який загальний тиск в посудині при температурі 127° С?
Відповідь: p = 4,15∙105 Па.
5.85. (С) В посудині знаходиться 14 г азоту і 9 г водню при температурі 10° С і тиску 106 Па. Знайти: 1 ) масу одного кіломоля суміші, 2) об'єм посудини.
Відповідь: 1) μ = 4,6 кг/кмоль;
2) V = 11,7∙10-3 м3.
5.86. (С) В закриту посудину, наповнену повітрям, вводиться диетиловий ефір (С2Н5ОС2Н5). Повітря знаходиться за нормальних умов. Після того, як весь ефір випарувався, тиск в посудині став рівний 1,4∙105 Па. Яка кількість ефіру була введена в посудину? Об'єм посудини V = 2 л.
Відповідь: m = 2,5∙10-3 кг.
5.87. (С) В посудині місткістю 0,5 л знаходиться 1 г парів йоду. При температурі 1000° С тиск в посудині виявився рівним 9,31∙104 Па. Знайти ступінь дисоціації молекул йоду J2 на атоми J за цих умов. Маса одного моля J2 дорівнює 0,254 кг/моль.
Відповідь: α = 0,12.
5.88. (С) В посудині знаходиться вуглекислий газ. При деякій температурі ступінь дисоціації молекул вуглекислого газу на кисень і окис вуглецю рівний 25%. В скільки разів тиск в посудині за цих умов буде більшим того тиску, який мав би місце, якби молекули вуглекислого газу не були дисоційовані?
Відповідь: 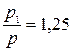 .
.
5.89. (С) Вважаючи, що повітря складається по масі з 23,6% кисню і 76,4% азоту, знайти густину повітря при тиску 105 Па і температурі 13° С. Знайти парціальні тиски кисню і азоту за цих умов.
Відповідь: ρ = 1,2 кг/м3, p1 = 0,236∙105 Па, p2 = 0,764∙105 Па.
5.90. (С) В посудині знаходиться суміш 10 г вуглекислого газу і 15 г азоту. Знайти густину цієї суміші при температурі 27° С і тиску 1,5∙105 Па.
Відповідь: ρ = 1,98 кг/м3.
5.91. (В) Знайти масу атома: 1) водню, 2) гелію.
Відповідь: 1) 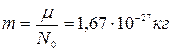 ; 2)
; 2) 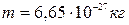 .
.
5.92. (A) Молекула азоту, що летить із швидкістю 600 м/с, ударяється нормально об стінку посудини і пружно відскакує від неї без втрати швидкості. Знайти імпульс сили, отриманий стінкою посудини за час удару.
Відповідь: 5,6∙10-23 Н∙с.
5.93. (A) Молекула аргону, що летить із швидкістю 500 м/с, пружно ударяється об стінку посудини. Напрям швидкості молекули і нормаль до стінки посудини складають кут 60°. Знайти імпульс сили, отриманий стінкою посудини за час удару.
Відповідь: 3,3∙10-23 Н∙с.
5.94. (A) Молекула азоту летить із швидкістю 430 м/с. Знайти імпульс цієї молекули.
Відповідь: 2∙10-23 кг∙м/с.
5.95. (В) Яка кількість молекул міститься в 1 г водяної пари?
Відповідь: 3,3∙1022.
5.96. (В) В посудині місткістю 4 л знаходиться 1 г водню. Яке число молекул міститься в 1 см3 цієї посудини?
Відповідь: 7,5∙1019 см-3.
5.97. (В) Яка кількість молекул знаходиться в кімнаті об'ємом 80 м3 при температурі 17°С і тиску 105 Па?
Відповідь: 2∙1027.
5.98. (В) Колба ємністю V = 0,5 л містить газ за нормальних умов. Визначити число N молекул газу, що знаходяться в колбі.
Відповідь: 1,34∙1022.
5.99. (В) В балоні ємністю V = 5 л міститься кисень масою т = 20 г. Визначити концентрацію п молекул в балоні.
Відповідь: 7,52∙1019 см-3.
5.100. (С) Одна третина молекул азоту масою т = 10 г розпалася на атоми. Визначити повне число N частинок, що знаходяться в такому газі.
Відповідь: 2,86∙1020.
5.101. (A) В балоні ємністю V = 3 л знаходиться кисень масою т = 4 г. Визначити кількість речовини ν газу.
Відповідь: 0,125 моль.
5.102. (A) В посудині ємністю V = 2,24 л за нормальних умов знаходиться кисень. Визначити кількість речовини ν в посудині.
Відповідь: 0,1 моль.
5.103. (В) В посудині ємністю 1 л знаходиться кисень масою 1 г. Визначити концентрацію молекул кисню в посудині.
Відповідь: 1,88 ∙1025 м-3.
5.104. (В) В посудині ємністю 5 л при нормальних умовах знаходиться азот. Визначити: 1) кількість речовини ν; 2) масу азота; 3) концентрацію n його молекул в посудині.
Відповідь: 1) ν = 0,223 моль; 2) m = 6,24 г; 3) n = 2,69 ∙1025 м-3.
5.105. (В) Визначити кількість речовини ν і число N молекул газу, що міститься в колбі ємністю V = 240 см3 при температурі Т = 290 К і тиску р = 50 кПа.
Відповідь:4,98 ммоль; 3∙1022.
5.106. (С) В колбі ємністю V = 100 см3 міститься деякий газ при температурі Т = 300 К. На скільки знизиться тиск р газу в колбі, якщо унаслідок витоку з колби вийде N = 1020 молекул?
Відповідь: 4,14 кПа.
5.107. (В) В колбі ємністю V = 240 см3 знаходиться газ при температурі Т = 290 К і тиску р = 50 кПа. Визначити кількість речовини ν газу і число N його молекул.
Відповідь:4,97 ммоль; 2,99∙1021.
5.108. (В) Скільки молекул знаходитиметься в 1 см3 посудини при 10° С, якщо посудина відкачана до щонайвищого розрідження, яке досягнуте сучасними лабораторними способами (р=10-9 Па)?
Відповідь: 3,4∙105 см-3.
5.109. (С) Для отримання високого вакууму в скляній посудині необхідно прогрівати стінки посудини при відкачуванні з метою видалення адсорбованого газу. Обчислити, на скільки може підвищитися тиск в сферичній посудині радіусом r = 10 см, якщо адсорбовані молекули перейдуть із стінок в посудину. Площу поперечного перерізу молекули вважати рівною 10-15 см2, шар мономолекулярний. Температура t= 300° С.
Відповідь: ΔP = 2,4 Па.
5.110. (С) Яка кількість частинок знаходиться в 1 г парів йоду, якщо ступінь дисоціації його рівний 50%? Маса одного моля йоду J2 дорівнює 0,254 кг/мoль.
Відповідь: 3,56∙1021.
5.111. (С) Яка кількість частинок знаходиться в 16 г наполовину диссоційованого кисню?
Відповідь: 4,5∙1023.
5.112. (С) В посудині знаходиться 10-13 молів кисню і 10-6 г азоту. Температура суміші дорівнює 100° С. При цьому тиск в посудині 0,133 Па. Знайти: 1) об'єм посудини, 2) парціальний тиск кисню і азоту, 3) число молекул в 1 см3 цієї посудини.
Відповідь: 1) V = 3,2∙10-3 м3; 2) p1 = 0,098 Па, p2 = 0,035 Па; 3) n = 2,6∙1013 см-3.
5.113. (A) Знайти середню квадратичну швидкість молекул повітря при температурі 17° С, вважаючи повітря однорідним газом, маса одного моля якого дорівнює μ = 0,029 кг/моль.
Відповідь: 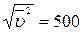 м/с.
м/с.
5.114. (В) Середня квадратична швидкість деякого газу при нормальних умовах дорівнює 480 м/с. Скільки молекул містить 1 г цього газу.
Відповідь: 2,04 ∙1022.
5.115. (С) В посудині ємністю V = 0,3 л при температурі 290 К знаходиться деякий газ. На скільки понизиться тиск p газу в посудині, якщо з нього вийде N = 1019 молекул.
Відповідь: 133 Па.
5.116. (A) Знайти відношення середніх квадратичних швидкостей молекул гелію і азоту при однакових температурах.
Відповідь: 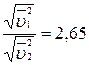 .
.
5.117. (A) У момент вибуху атомної бомби розвивається температура, що дорівнює приблизно 10 млн °С. Вважаючи, що при такій температурі всі молекули повністю диссоційовані на атоми, а атоми іонізовані, знайти середню квадратичну швидкість іона водню.
Відповідь: 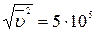 м/с.
м/с.
5.118. (С) Знайти число молекул водню в 1 см3, якщо тиск дорівнює 2,66∙104 Па, а середня квадратична швидкість його молекул за даних умов дорівнює 2400 м/с.
Відповідь: N = 4,2∙1018 см-3.
5.119. (С) Густина деякого газу дорівнює 6·10-2 кг/м3, середня квадратична швидкість молекул цього газу дорівнює 500 м/с. Знайти тиск, який газ чинить на стінки посудини.
Відповідь: p = 5∙103 Па.
5.120. (С) Визначити тиск, який чинить газ на стінки посудини, якщо його густина дорівнює 0,01 кг/м3, а середня квадратична швидкість молекул газу складає 480 м/с.
Відповідь: 768 Па.
5.121. (В) В скільки разів середня квадратична швидкість порошинки в повітрі, менша за середню квадратичну швидкість молекул повітря? Маса порошинки 10-8 г. Повітря вважати однорідним газом, маса одного моля якого дорівнює 0,029 кг/моль.
Відповідь: В 1,44∙107 раза.
5.122. (В) Знайти імпульс молекули водню при температурі 20° С. Швидкість молекули вважати рівною середній квадратичній швидкості.
Відповідь: 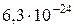 кг∙м/с.
кг∙м/с.
5.123. (С) В посудині об'ємом 2 л знаходиться 10 г кисню під тиском 9∙104 Па. Знайти: 1) середню квадратичну швидкість молекул газу, 2) число молекул, що знаходяться в посудині, 3) густину газу.
Відповідь: 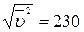 м/с; 2) N= 1,9∙1023; 3) ρ = 5,0 кг/м3.
м/с; 2) N= 1,9∙1023; 3) ρ = 5,0 кг/м3.
5.124. (В) Частинки гуммігута діаметром D = 1 мк беруть участь в броунівському русі. Густина гуммігута ρ = 1 г/см3. Знайти середню квадратичну швидкість частинок гуммігута при t = 0°C.
Відповідь: 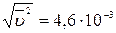 м/с.
м/с.
5.125. (В) Середня квадратична швидкість молекул деякого газу дорівнює 450 м/с. Тиск газу дорівнює 0,5 ∙105 Па. Знайти густину газу за цих умов.
Відповідь: ρ = 0,74 кг/м3.
5.126. (В) Знайти середню квадратичну швидкість молекул газу, густина якого при тиску 105 Па дорівнює 8,2·10-5 г/см3. 2) Чому дорівнює маса одного кіломоля цього газу, якщо значення густини дано для температури 17° С?
Відповідь: 1) 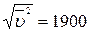 м/с. 2) μ = 2 кг/кмоль.
м/с. 2) μ = 2 кг/кмоль.
5.127. (В) Середня квадратична швидкість молекул деякого газу за нормальних умов дорівнює 461 м/с. Яка кількість молекул міститься в 1 г цього газу?
Відповідь: N = 1,88∙1022.
5.128. (В) Визначити найбільш імовірну швидкість молекул газу густина якого при тиску 40 кПа складає 0,35 кг/м3.
Відповідь: 478 м/с.
5.129. (С) Визначити середню енергію 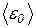 поступального руху молекул газу, який знаходиться під тиском 0,1 Па. Концентрація молекул газу дорівнює 1013 см-3.
поступального руху молекул газу, який знаходиться під тиском 0,1 Па. Концентрація молекул газу дорівнює 1013 см-3.
Відповідь: 1,5 ∙10-19 Дж.
5.130. (В) Визначити: 1) найбільш імовірну υім; 2) середню арифметичну <υ>; 3) середню квадратичну <υкв> швидкості молекул азоту (N2) при 27° С.
Відповідь: 1) 422 м/с; 2) 476 м/с; 3) 517 м/с.
5.131. (В) При якій температурі середня квадратична швидкість молекул кисню більша їх найбільш імовірної швидкості на 100 м/с?
Відповідь: 381 К.
5.132. (A) Знайти середню квадратичну <υкв>, середню арифметичну <υ> і найвірогіднішу υ в швидкості молекул водню. Обчислення виконати для трьох значень температури: 1) Т = 20 К; 2) Т = 300 К; 3) Т = 5000 К.
Відповідь: 1) 500 м/с, 462 м/с, 407 м/с; 2) 1940 м/с, 1790 м/с, 1580 м/с; 3) 7900 м/с, 7300 м/с, 6480 м/с;
5.133. (В) При якій температурі Т середня квадратична швидкість атомів гелію стане рівною другій космічній швидкості υ2 = 11,2 км/с?
Відповідь: 20100 К.
5.134. (В) При якій температурі Т молекули кисню мають таку ж середню квадратичну швидкість <υкв>, як молекули водню при температурі Т1 = 100 К?
Відповідь: 1600 К.
5.135. (В) Колба ємністю V = 4 л містить деякий газ масою m = 0,6 г під тиском р = 200 кПа. Визначити середню квадратичну швидкість <υкв> молекул газу.
Відповідь: 2000 м/с.
5.136. (С) Суміш гелію і аргону знаходиться при температурі Т = 1200 К. Визначити середню квадратичну швидкість <υкв> і середню кінетичну енергію атомів гелію і аргону.
Відповідь: гелій: 2730 м/с та 2,48∙10-20 Дж; аргон: 864 м/с, 2,48∙10-20 Дж.
5.137. (В) Знайти середню арифметичну, середню квадратичну і найвірогіднішу швидкості молекул газу, густина якого при тиску 4∙104 Па дорівнює 0,3 кг/м3.
Відповідь: 1) 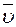 = 579 м/с; 2)
= 579 м/с; 2) 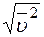 = 1,57×103 м/с; 3)
= 1,57×103 м/с; 3) 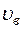 = 513 м/с.
= 513 м/с.
5.138. (A) При якій температурі середня квадратична швидкість молекул азоту більша за їх найвірогіднішу швидкість на 50 м/с?
Відповідь: Т = 83 К.
5.139. (В) В скільки разів середня квадратична швидкість <υкв> молекул кисню більша за середню квадратичну швидкість порошинки масою m = 10-8 г, що знаходиться серед молекул кисню?
Відповідь: 1,37∙107 раз.
5.140. (A) Визначити середню арифметичну швидкість <υ> молекул газу, якщо їх середня квадратична швидкість <υкв>= 1 км/с.
Відповідь: 920 м/с.
5.141. (A) Визначити найвірогіднішу швидкість υв молекул водню при температурі Т = 400 К.
Відповідь: 1820 м/с.
5.142. (В) Найбільш імовірна швидкість молекул азоту υiм, що розглядається як ідеальний газ, зменшилась вдвічі. Як змінився при цьому тиск р, якщо процес, що супроводжується зміною υiм, адіабатний?
Відповідь: 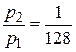 .
.
5.143. (В) Підрахувати найбільш імовірну υiм, середню 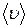 та середню квадратичну
та середню квадратичну 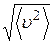 швидкості молекул ідеального газу, у якого при нормальному тиску густина ρ= 1,2 кг/м3.
швидкості молекул ідеального газу, у якого при нормальному тиску густина ρ= 1,2 кг/м3.
Відповідь: υiм = 411 м/с; 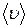 = 463 м/с;
= 463 м/с; 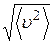 = 502 м/с.
= 502 м/с.
5.144. (A) При якій температурі Т2 середня квадратична швидкість молекул водню дорівнює такій самій швидкості молекул азоту при температурі Т1 = 390 К?
Відповідь: 27,85 К.
5.145. (В) Знайти кінетичну енергію ε поступального руху молекул газу, якій відповідає швидкість, що дорівнює її найбільш імовірній швидкості. Температура газу T=300 К.
Відповідь: 4,144∙10-21 Дж.
5.146. (A) Висотна космічна станція розташована на горі Алагез у Вірменії на висоті 3250 м над рівнем моря. Знайти тиск повітря на цій висоті. Температуру повітря вважати постійною і рівною 5° С. Массу одного моля повітря прийняти рівною 0,029 к г/моль. Тиск повітря на рівні моря 1,01∙105 Па.
Відповідь: р = 68 кПа.
5.147. (В) На якій висоті тиск повітря складає 75% від тиску на рівні моря? Температуру вважати постійною і рівною 0° С.
Відповідь: h = 2,3 км.
5.148. (В) Пасажирський літак здійснює польоти на висоті 8300 м. Щоб не забезпечувати пасажирів кисневими масками, в кабінах за допомогою компресора підтримується постійний тиск, що відповідає висоті 2700 м. Знайти різницю тисків всередині і ззовні кабіни. Середню температуру зовнішнього повітря вважати рівною 0° С.
Відповідь: р1 = 0,354 ат., р2 = 0,713 ат., Δр = 0,36 ат.
5.149. (В) Яка маса 1 м3 повітря: 1) біля поверхні Землі, 2) на висоті 4 км від поверхні Землі? Температуру повітря вважати постійною і рівною 0° С. Тиск повітря біля поверхні Землі дорівнює 105 Па.
Відповідь: 1) 1,28 кг; 2) 0,78 кг.
5.150. (В) Знайти відношення тиску повітря на висоті h1 = 2 км до тиску на дні шахти завглибшки h2 = 2 км. Поле тяжіння однорідне, атмосфера є ідеальним газом, який перебуває в стані термодинамічної рівноваги при Т = 300 К.
Відповідь: 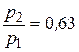 .
.
5.151. (В) На якій висоті h відношення концентрації водню до концентрації кисню у земній атмосфері при Т = 300 К більша за відношення цих концентрацій поблизу поверхні Землі у η = 4,22 раза?
Відповідь: 12 км.
5.152. (В) Порошинки, завислі в повітрі, мають масу т = 10-18 г. В скільки разів зменшиться їх концентрація n призбільшенні висоти на Δh = 10 м? Температура повітря Т = 300 К.
Відповідь: В е23,6 раза.
5.153. (A) На скільки зменшиться атмосферний тиск р = 100 кПа при підйомі спостерігача над поверхнею Землі на висоту h = 100 м? Вважати, що температура Т повітря рівна 290 К і не змінюється з висотою.
Відповідь: 1,18 кПа.
5.154. (A) На якій висоті h над поверхнею Землі атмосферний тиск удвічі менший ніж на її поверхні? Вважати, що температура Т повітря рівна 290 К і не змінюється з висотою.
Відповідь: 5,88 км.
5.155. (A) Барометр в кабіні вертольота, що летить, показує тиск р = 90 кПа. На якій висоті h летить вертоліт, якщо на злітному майданчику барометр показував тиск р0 = 100 кПа? Вважати, що температура Т повітря рівна 290 К і не змінюється з висотою.
Відповідь: 885 м.
5.156. (В) Барометр в кабіні літака, що летить, весь час показує однаковий тиск р = 80 кПа, завдяки чому льотчик вважає висоту h польоту незмінною. Проте температура повітря змінилася на ΔТ = 1 К. Яку помилку Δ h у визначенні висоти допустив льотчик? Вважати, що температура не залежить від висоти і що біля поверхні Землі тиск р0 = 100 кПа.
Відповідь: 6,5 м.
5.157. (A) На якій висоті тиск повітря складає 60 % від тиску на рівні моря? Вважати, що температура повітря скрізь однакова і рівна 10° С.
Відповідь: 4,22 км.
5.158. (В) Який тиск повітря в шахті на глибині 1 км, якщо вважати, що температура по всій висоті постійна і рівна 22° С, а прискорення вільного падіння не залежить від висоти? Тиск повітря біля поверхні Землі прийняти рівним р0.
Відповідь: 1,12 р0.
5.159. (В) Визначити відношення тиску повітря на висоті 1 км до тиску на дні свердловини глибиною 1 км. Повітря біля поверхні Землі знаходиться за нормальних умов, і його температура не залежить від висоти.
Відповідь: 0,78.
5.160. (В) На якій висоті густина повітря в е раз (е – основа натуральних логарифмів) менша в порівнянні з його густиною на рівні моря? Температуру повітря і прискорення вільного падіння вважати не залежною від висоти.
Відповідь: 7,98 км.
5.161. (В) На якій висоті густина газу складає 50% від густини його на рівні моря? Температуру вважати постійною і рівною 0° С. Задачу розв’язати для: 1) повітря і 2) водню.
Відповідь: 1) h = 5,5 км; 2) h = 80 км.
5.162. (A) Тиск повітря на рівні моря р0 = 99,75 кПа, а на вершині гори 78,47 кПа. Яка висота гори, якщо температура повітря рівна t = 5° С?
Відповідь: 1950 м.
5.163. (С) Трубка завдовжки 22 см обертається навколо вертикальної осі, що проходить через її середину, з частотою оборотів, рівною 30 с-1. Температура повітря 16° С. Приймаючи тиск повітря усередині трубки поблизу її відкритих кінців рівним атмосферному (101,08 кПа ), визначити тиск в середині трубки.
Відповідь: 100,8 кПа.
Дата публикования: 2015-11-01; Прочитано: 9982 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
