 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Получение азота и водорода для синтеза аммиака
|
|
Источником азота, а также кислорода является атмосферный воздух. Разделение его можно вести переводом в жидкое состояние с последующей ректификацией. Для этого необходимо глубокое охлаждение воздуха до температуры ниже критической, которая для азота составляет –147 о С при давлении 0,34 МПа. Такие условия могут быть созданы лишь при многократном цикле «сжатие – расширение – совершение работы» с помощью турбокомпрессоров и значительных затратах энергии.
Практическое получение водорода обычно осуществляют конверсией метана, входящего в состав природного газа в количестве до 98 %. Сущность конверсии состоит в окислении метана и его гомологов по одной из следую-щих реакций:

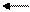 СН4 + Н2О СО + 3Н2 – 206 кДж/моль; (10.4)
СН4 + Н2О СО + 3Н2 – 206 кДж/моль; (10.4)

 СН4 + 0,5О2 СО + 2Н2 + 35 кДж/моль; (10.5)
СН4 + 0,5О2 СО + 2Н2 + 35 кДж/моль; (10.5)

 СН4 + СО2 2СО + 2Н2 – 248 кДж/моль. (10.6)
СН4 + СО2 2СО + 2Н2 – 248 кДж/моль. (10.6)
Для производства водорода применяют реакции (10.4) и (10.5). Полу-чаемый в этих реакциях синтез-газ (смесь СО и Н2) используют также для синтеза метанола, высших спиртов, синтетической олифы, моющих средств, восстановления ряда металлов из руд.
Для получения азотоводородной смеси или водорода из синтез-газа его подвергают вторичной обработке водяным паром с целью конверсии СО:

 СО + Н2О СО2 + Н2 + 41 кДж/моль. (10.7)
СО + Н2О СО2 + Н2 + 41 кДж/моль. (10.7)
Если суммировать реакции 10.4 и 10.7, то получим:
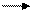
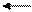 СН4 +2Н2О СО2 + 4Н2 – 165 кДж/моль (10.8)
СН4 +2Н2О СО2 + 4Н2 – 165 кДж/моль (10.8)
и реакция требует подвода энергии.
Для смещения равновесия вправо применяют избыток водяного пара и повышенную температуру. При соотношении СН 4: Н2О = 1:2 и температуре 800 о С уже достигаются условия синтеза аммиака, когда в исходном сырье содержится не более 0,5 % СН 4. Но скорость реакции мала даже при 1000 о С. Поэтому процесс ведут на никельсодержащем катализаторе, с применением которого скорость конверсии СН 4 резко возрастает. Равновесие на нем достигается уже при 800–850 о С. Процесс ведут при 1–4 МПа, причем давление создается природным газом, подаваемым на завод под давлением.
По характеру применяемого окислителя различают парокислородную и паровоздушную конверсии.
10.2.1. В парокислородной конверсии компенсацию потерь теплоты в эндотермической реакции (10.4) проводят одновременной реализациeй в одном каталитическом реакторе экзотермической реакции (10.5) и частичного сгорания метана до СО 2 и Н 2 О. Для этого в реактор шахтного типа подают смесь природного газа, водяного пара и воздуха, обогащенного кислородом до 40–50 % об. За счет выделившегося тепла по реакции (10.5) температуру в верхних слоях катализатора поддерживают в пределах 1050–1100 о С, а на выходе из реактора – 800–900 о С.
10.2.2. Паровоздушную конверсию ведут в две стадии с целью полной утилизации тепла конвертируемого и дымовых газов. Первую стадию (реакцию 10.4) проводят в каталитическом реакторе трубчатого типа идеального вытеснения, в трубках которого помещают катализатор. При этом компенсацию потерь тепла достигают путем сжигания природного газа в межтрубном пространстве реактора. Температура в реакторе 800–850 о С. Выходящий газ содержит 8–10 % СН 4 (об.). Вторую стадию (конверсию непревращенного метана) ведут по реакции 10.8 в шахтном каталитическом реакторе при 900– 1000 о С. Эту температуру выдерживают за счет тепла самой реакции.
9.2.3. Конверсия СО – обратимая экзотермическая реакция, протекаю-щая без изменения объема. Снижение температуры смещает равновесие вправо, но даже при Т = 500 о С скорость реакции очень мала даже в присутствии катализатора. Константа скорости реакции описывается уравнением:
K = 4,92 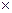 104
104 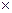 е– Е/RT , (10.8)
е– Е/RT , (10.8)
где Е = 77,5 кДж/моль.
Конверсию СО ведут на высокотемпературном железохромовом ката-лизаторе, промотированном оксидами алюминия, кобальта и калия при температуре не менее 450 о С. При этом в газе конверсии содержится 2–4 % непревращенного СО. На низкотемпературном цинк-хром-медном катализаторе процесс ведут при 200–300 о С, причем остаточное количество СО составляет всего 0,2–0,4 % и очистка газа конверсии от СО упрощается. Однако второй катализатор менее устойчив, чем первый. В промышленности осуществляют комбинированную технологию в две стадии, причем первую стадию ведут на высокотемпературном катализаторе, а вторую – на низкотемпературном. Такая технология позволяет приблизить температуру процесса к оптимальной и повысить срок службы низкотемпературного катализатора. Тепло реакции после первой стадии утилизируется и температура газа перед второй стадией понижается с увеличением выхода водорода.
Технологическое оформление процесса представлено на рис. 10.2.
 дымовой газ Н2 2 3
дымовой газ Н2 2 3





















































































































































































































 воздух
воздух



 6 8 10
6 8 10
 |  | ||||
 | |||||
 | |||
 | |||



 вода
вода







 4
4







 9
9




 воздух конвертиро-
воздух конвертиро-










 ванный газ
ванный газ













 СН4
СН4





 5 7 пар вода пар
5 7 пар вода пар
Рис. 10.2. Схема установки паровоздушной конверсии метана
На схеме обозначено: 1 – подогреватель природного газа; 2 – реактор гидрирования сернистых соединений; 3 – адсорбер сероводорода; 4 – теплообменник; 5 – трубчатый реактор-конвертор; 6 – шахтный реактор-конвер-тор; 7,9 – котел-утилизатор; 8 – реактор конверсии СО первой ступени; 10 – реактор конверсии СО второй ступени.
10.2.4. Описание технологической схемы. Согласно данной схеме, природный газ после нагрева в теплообменнике 1 и очистки от серосодержащих соединений в аппаратах 2 и 3 смешивают с парами воды в соотношении 1:3,5. Парогазовая смесь, нагретая дымовыми газами, отходящими из трубчатого реактора, до 380 о С в теплообменнике 4, поступает на первую ступень конверсии в трубчатый реактор-конвертер 5. Конвертированный на первой ступени газ, смешивают с воздухом и направляют на вторую ступень конверсии в шахтный реактор-конвертер 6 при температуре 900–1000 о С и далее в котел-утилизатор 7, где за счет тепла процесса получают пар с температурой 480 о С и давлением 10 МПа. После охлаждения в котле-утилизаторе 7 конвертированный газ поступает на двухступенчатую конверсию СО последовательно в реакторы 8 и 10. Окончательно конвертированный газ поступает в отделение очистки от остатков СО, СО 2, О 2 и серосодержащих веществ.
Очистка природного и конвертированного газа необходима для за-щиты катализаторов конверсии метана СО и синтеза аммиака от действия ядов, которыми являются соединения серы, СО, СО 2, и О 2.
Очистку газов от серосодержащих соединений мокрым (абсорбционным) или/и сухим (адсорбционным) методами. На первой стадии (мокрой) очистку ведут путем поглощения СО 2 водой или растворами моноэтаноламина, гидроксидов натрия или калия. Если доля СО в газе выше 0,4 %, то абсорбцию проводят медноаммиачным раствором, жидким азотом. Затем остаточные количества СО и СО 2 метанируют каталитическим гидрированием на цинксодержащем или алюмоникелевом катализаторе.
Очистку газа от СО 2 водой ведут при повышенном давлении в соответствии с реакцией:

 СО2 + Н2О Н2СО3. (9.9)
СО2 + Н2О Н2СО3. (9.9)
Действие щелочей основано на следующих реакциях:

 Н2S + 2OH– 2H2O + S2– ; (9.10)
Н2S + 2OH– 2H2O + S2– ; (9.10)

 СО2 + 2ОН– Н2О + СО32–. (9.11)
СО2 + 2ОН– Н2О + СО32–. (9.11)
Этаноламин поглощает сероводород и углекислый газ по следующей схеме

 Н2S + CH2OH – CH2NH2
Н2S + CH2OH – CH2NH2  +HS –; (9.12)
+HS –; (9.12)

 CO2 + H2O + CH2OH – CH2NH2
CO2 + H2O + CH2OH – CH2NH2  +НСО
+НСО 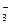 . (9.13)
. (9.13)
Очистку от угарного газа ведут при давлении 10–32 МПа и температуре 10 о С аммиачным раствором ацетата меди:


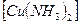 + + СH3COOH + CO + NH3
+ + СH3COOH + CO + NH3  + + CH3COONH4. (9.14)
+ + CH3COONH4. (9.14)
Окончательное удаление вредных примесей из газа ведут каталитическим гидрированием на никель-алюминиевом катализаторе при 250–300 о С и давлении 30 МПа. При этом протекают следующие реакции

 СО + 3Н2 СН4 + Н2О; (10.15)
СО + 3Н2 СН4 + Н2О; (10.15)

 СО2 + 4Н2 СН4 + 2Н2О; (10.16)
СО2 + 4Н2 СН4 + 2Н2О; (10.16)
О2 + 2Н2 = 2Н2О. (10.17)
Поcле всех ступеней очистки получают азотоводородную смесь (АВС), поступающую на синтез аммиака, следующего состава, oб %: N 2 – 24,75; Ar – 0,25; H 2 – 71,25; CH 4 – 0,25.
Дата публикования: 2015-10-09; Прочитано: 1151 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
