 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Зависимость доли аммиака в газовой смеси от параметров процесса
|
|
| Температура, оС | Доля аммиака в газовой смеси, % об. | |
| при 30 МПа | при 100 МПа | |
| 89,9 | 98,3 | |
| 71,0 | 92,5 | |
| 47,0 | 79,8 | |
| 26,4 | 57,5 | |
| 13,3 | 31,4 | |
| 7,3 | 12,8 |
Из таблицы следует, что даже при 100 МПа достаточно высокий выход NH 3 может быть достигнут при температуре менее 400 о С. Но при этой температуре мала скорость процесса и велико время достижения равновесия.
Промышленный синтез аммиака удалось осуществить при температуре 450–500 о С и высоком давлении с участием катализаторов и цикличностью процесса. Эта реакция катализируется металлами Fe, W, Re, Rh, Os, Pt, U.
Наиболее активны Os и U, но они очень дороги и высокочувствительны к ядам. Кроме того, уран радиоактивен. В российской азотной промышленности применяют катализатор ГИАП (государственный институт азотной промышленности) состава: [ Fe + Al2O3 + K2O + CaO + SiO2 ]. В этой каталитической системе железо является главным компонентом композиции, оксид алюминия и диоксид кремния имеют функцию носителей-промоторов, оксиды калия и кальция – только промоторов.
 Катализатор готовят плавлением в кислородной среде смеси оксидов Fe3O4, K 2 O, CaO и SiO 2 с последующим восстановлением водородом или азотоводородной смеси магнетита (Fe 3 O 4) до металла. Промоторы создают высокоразвитую поверхность катализатора, препятствуют его рекристаллизации и повышают активность основного компонента катализатора – железа. Железный катализатор быстро и необратимо отравляется сернистыми соединениями, образуя сульфиды. СО и СО 2 отравляют железо обратимо, т.е. его можно в этом случае восстановить.
Катализатор готовят плавлением в кислородной среде смеси оксидов Fe3O4, K 2 O, CaO и SiO 2 с последующим восстановлением водородом или азотоводородной смеси магнетита (Fe 3 O 4) до металла. Промоторы создают высокоразвитую поверхность катализатора, препятствуют его рекристаллизации и повышают активность основного компонента катализатора – железа. Железный катализатор быстро и необратимо отравляется сернистыми соединениями, образуя сульфиды. СО и СО 2 отравляют железо обратимо, т.е. его можно в этом случае восстановить.
Более поздняя композиция (ГИАП-16) имеет следующий состав, % масс.: NiO – 25; Al2O3 – 57; СаО – 10; MgO – 8.
Процесс синтеза аммиака включает следующие стадии:
- диффузию Н 2 и N 2 к поверхности катализатора;
- проникновение Н 2 и N 2 в поры катализатора;
- активированную адсорбцию (химическую) Н 2 и N 2 поверхностью катализатора;
- химическую реакцию с последовательным образованием имида NH=, амида NH 2 – и, наконец, аммиака NH 3;
- десорбцию NH 3 из пор катализатора к поверхности;
- десорбцию NH 3 с поверхности катализатора в реакционный объем;
- удаление NH 3 из реакционной зоны.
Лимитирующей стадией синтеза аммиака на железном катализаторе является третья стадия – активированная адсорбция азота поверхностью катализатора. Скорость реакции описывается уравнением Темкина – Пыжова:
U = U 1 – U 2 =  =
= 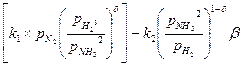 , (10.20)
, (10.20)
где k 1, k 2 – константы скорости прямой и обратной реакций, соответственно;
р N  ; p H
; p H 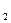 ; p NH
; p NH 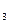 – парциальные давления азота, водорода и аммиака соответственно
– парциальные давления азота, водорода и аммиака соответственно
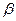 – коэффициент, зависящий от давления;
– коэффициент, зависящий от давления;
 – для железного катализатора равен 0,5.
– для железного катализатора равен 0,5.
Энергия активации прямой реакции равна в условиях процесса 170 кДж/моль.
При температурах 400–500 о С максимальная степень превращения в процессе составляет 20 %, а обычно – 14–17 %. Поэтому синтез аммиака реа-лизован по циклической схеме, при которой непревращенное сырье рециркулируют в исходное. Благодаря этому приему, почти отсутствуют вредные выбросы в атмосферу.
Исследования по оптимизации параметров технологического процесса синтеза аммиака, позволили установить следующие их значения:
Температура – 450–550 о С;
Давление – 30–32 МПа;
Объемная скорость подачи сырья – (3–4) · 104 м 3 /м 3 · ч;
Объемный состав азотоводородной смеси – стехиометрический (V 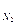 :V
:V 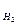 = 1:3).
= 1:3).
На рисунке 10.2 представлена технологическая схема процесса.

 циркуляционный газ NH3 (газ)
циркуляционный газ NH3 (газ)

 АВС
АВС







 8 3
8 3
































































































 6
6



 2 5
2 5
 1
1
 пар вода
пар вода





 |  |





 4 4 NH3 (ж.)
4 4 NH3 (ж.)

Рис. 10.2. Технологическая схема процесса синтеза аммиака
1 – колонна синтеза; 2 – холодильник-конденсатор; 3 – смеситель (инжектор) свежей АВС и циркуляционной смеси; 4 – конденсационная колонна; 5 – газоотделитель; 6 – испаритель жидкого аммиака; 7 – теплообменник (котел-утилизатор); 8 – турбокомпрессор.
Процесс синтеза аммиака осуществляется следующим образом.
Циркуляционный газ турбокомпрессором 8 подается на смешение со свежей азотоводородной смесью в смесителе 3 и далее в конденсационную колонну 4, где из циркуляционного газа конденсируется часть аммиака, а остальное количество рециркулирует в реактор-колонну 1. Выходящий из колонны газ, содержащий до 20 % аммиака, направляется в водяной холодиль-ник-конденсатор 2, а затем в газоотделитель 5, где из него выделяют жидкий аммиак. Несконденсированный газ компримируют турбокомпрессором 8, смешивают со свежей азотоводородной смесью и направляют в конденсационную колонну 4, а затем в испаритель жидкого аммиака 6, где при –20 о С также конденсируется большая часть аммиака.
Промышленность выпускает аммиак первого сорта с концентрацией NH 3 99,9 % и второго сорта с концентрацией 99,6 % и аммиачную воду с долей NH 3 25 %. Аммиак первого сорта используют в качестве хладоагента в холодильных агрегатах и удобрений, второго сорта – в производстве азотной кислоты.
Контрольные вопросы
1. Расскажите о распространении азота в природе. В чем заключается проблема «связанного» азота?
2. Дайте сравнительную оценку эффективности «связывания» азота различными промышленными способами. Приведите химизм процессов.
3. Назовите основные направления использования аммиака.
4. Каковы источники получения азота и водорода для синтеза аммиака?
5. Приведите химизм процессов конверсии метана.
6. В чем состоят особенности парокислородной и паровоздушной конверсии аммиака?
7. Представьте технологическую схему паровоздушной конверсии метана. Дайте ее описание.
8. Объясните необходимость очистки природного и конвертированного газа. Приведите химизм процессов очистки.
9. Расскажите о катализаторах конверсии метана.
10. Сделайте анализ процесса синтеза аммиака с точки зрения термодинамики и кинетики.
11. Опишите промышленные условия синтеза аммиака. Какой катализатор используется в процессе?
12. Приведите технологическую схему процесса синтеза аммиака. Дайте ее описание.
13. Почему в производстве аммиака применяют циклическую схему?
Дата публикования: 2015-10-09; Прочитано: 495 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
