 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Производство серной кислоты
|
|
Этот процесс – один из самых многотоннажных среди неорганических производств и занимает одно из ведущих мест в химической технологии.
В 2007 г. в мире выпускалocь свыше 175 млн. т серной кислоты. Объем ее выпуска превышает производство соляной, азотной, уксусной и других кислот вместе взятых. Серная кислота находит применение в производстве минеральных удобрений (около 50 %), взрывчатых веществ, минеральных солей и кислот, для очистки нефтепродуктов, и их синтезе (например, алкилирование изобутана), при обработке металлов, производстве продуктов органического синтеза, лекарственных препаратов и т.д. Многообразие областей применения серной кислоты представлено на диаграмме (рис. 9.1).
 |  |  |  |
Производство хроматов Производство сульфатов Минеральные Сульфат



 удобрения аммония
удобрения аммония
 | |||
 | |||

 Взрывчатые вещества Травление металлов
Взрывчатые вещества Травление металлов
 |  |  |
Производство спиртов, Цветная
 эфиров, кислот и др. СЕРНАЯ КИСЛОТА металлургия
эфиров, кислот и др. СЕРНАЯ КИСЛОТА металлургия






 органических веществ
органических веществ






 Производство красителей
Производство красителей
 Минеральные кислоты
Минеральные кислоты
 |  |  |  |
Производство глюкозы Химические Очистка Катализатор В сернокис-
 и патоки волокна, нефте- алкилирования лотных ак-
и патоки волокна, нефте- алкилирования лотных ак-





 текстиль продуктов и др. процессов кумуляторах
текстиль продуктов и др. процессов кумуляторах
Рис. 9.1. Области применения серной кислоты
Больше всeго серной кислоты производится в США – 30 млн. т. Другими крупными ее производителями являются Германия и Япония.
Феномен высокого объема производства серной кислоты обусловлен комплексом ее физико-химических свойств. Она – самая дешевая из всех сильных кислот, не дымит и не имеет запаха, удобна в транспортировке, т. к. в концентрированном виде не разрушает черные металлы.
В технике под серной кислотой подразумевают любые смеси SO3 c H2O (mSO3 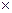 nH2O). Формуле H2SO4 соответствует моногидрат (m = n = 1) с плотностью 1850 кг / м3.
nH2O). Формуле H2SO4 соответствует моногидрат (m = n = 1) с плотностью 1850 кг / м3.
Разделение H2SO4 по сортам во многом связано с ее концентрацией и в значительной мере определяется температурой замерзания растворов ее с водой. Диаграмма кристаллизации системы SO3 – H2O представлена на рис. 9.2.


 | Н2SO4 | хSO3 | |||||||||
       
| H2SO4 | х2SO3 | |||||||||
          Н2О Н2О
| Н2SO4 | SO3 | |||||||||
 
| |||||||||||
  
| |||||||||||
 
| H2SO4 x | 4H2O | |||||||||
   
| H2SO4 x2H | 2H2O | |||||||||
 
| |||||||||||

| |||||||||||

| |||||||||||

| |||||||||||

|
0 0 20 40 60 80 100 20 40 60 80 100
% Н2SО4 % SO3 (своб.)
Концентрация, % масс.
Рис. 9.2. Диаграмма кристаллизации системы Н2О – SO3
Из диаграммы следует, что при концентрациях от 0 до 64,5 % SO 3 образуется 6 химических соединений-гидратов SO 3, растворимых друг в друге в жидком состоянии, а при кристаллизации образуют эвтектические смеси. В области концентраций от 64,5 % до 100 % SO 3 при замерзании образуются твердые растворы. Для того, чтобы кислота не замерзала в зимнее время, все ее товарные сорта имеют концентрации, близкие к эвтектическим составам.
Ниже приведена еще одна диаграмма – кипения системы Н 2 О – SО 3 при атмосферном давлении (рис. 8.3).
Кислота, содержащая 98,3 % Н 2 SO 4, является азеотропом и кипит при температуре 336,6 о С. Диаграмму, изображенную на рис. 9.3, применяют при концентрировании кислоты выпариванием воды. Из диаграммы следует, что при нагревании кислоты, содержащей менее 90 % Н 2 SО 4, в пар переходит почти исключительно вода. При концентрации выше 93 % Н 2 SО 4 состав паров быстро приближается к составу жидкой фазы. Поэтому практически серную кислоту концентрируют упариванием только до купоросного масла, т. е. до 92 % Н 2 SО 4. При повышении температуры пары Н 2 SО 4 диссоциируют на SО 3 и Н 2 О, а затем SО 3 распадается на SО2 и О2. При 700 о С в парах преобладает SО2, а выше 900 оС SО3 диссоциирует полностью.
 340
340
   
| |||||||||
  
|  Пар Пар
|  Пар Пар
| |||||||

| |||||||||
        
| |||||||||

| |||||||||
        
| |||||||||

| |||||||||

| Раствор | ||||||||
  
| Раствор | ||||||||
  
| |||||||||
 
| |||||||||
 
| |||||||||
 
|
 0 20 40 60 80 100 20 40 60 80 100
0 20 40 60 80 100 20 40 60 80 100
Н2SО4 SO3 (cвоб.)
Концентрация, % масс.
Рис. 9.3. Диаграмма кипения системы Н2О–SО3 при атмосферном давлении
Дата публикования: 2015-10-09; Прочитано: 463 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
