 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
А. Расчет реакторов при проведении простых реакций
|
|
Пример 2.1.
Натриевую соль дихлорфеноксиуксусной кислоты получают в водном растворе
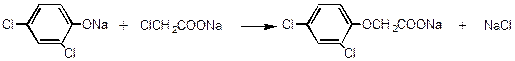
 k= 20,8·10-3 м/моль.хв
k= 20,8·10-3 м/моль.хв
Исходная смесь содержит 2,2 моль/дм3 дихлорфенолята и 2,2 моль/дм3 монохлорацетата. Степень превращения равняется 98%, а выход натриевой соли дихлорфеноксиуксусной кислоты равняется 85%. Определите размер реактора для производства 2000 т/год, если время загрузки и разгрузка реактора 7 часов. Коэффициент загрузки аппарата 2/3
Решение
Время цикла РИС-П

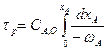
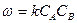


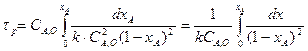

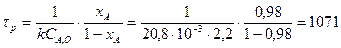 хв = 17,84 часов
хв = 17,84 часов
С учетом вспомогательного времени
 ч.
ч.
Мощность реактора будем считать по продукту реакции
Gг=2000 т/год = 2·109 т/год
Молекулярная масса продукта 243
2·109/243=8,23·106 моль/год
Так как выход 85%, а степень преобразования 0,98, то исходного реагента надо:
n=8,23·10-6/0,85·0,98=9,9·106 моль/год
Объем раствора который надо переработать:
9,9·106/2,2=4,5·103 м3/год
Количество загрузок за год
8000/24,84=320
Тогда объем смеси на одну загрузку
4,5·103/320=14 м3
Объем реактора  м3
м3
Пример 2.2. Определить объём РИС-Н и РИВ и сравнить эти объёмы
Условия
Реакция гидролиза уксусного ангидрида (А) проводится в большом избытке воды (В):
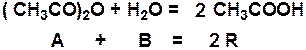
Объёмный расход реагентов Vc 20 дм3/мин
Константа скорости реакции К 0.38 мин-1
Степень превращения хА 0,1 – 0,9
Решение
Расчет проводим по следующим уравнениям:
для РИС-Н:
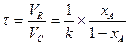 ,
,
для РИВ
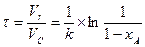
Результаты расчета по уравнениям (а) и (б) при хА=0,1 – 0,9 приведены в табл. 1.3 и показаны на рис. 1.1
Таблица 2.3.
| хА | VРИС-Н, л | VРИВ, л | VРИС-Н / VРИВ |
| 0,1 | 5,85 | 5,5 | 1,06 |
| 0,3 | 22,6 | 18,8 | 1,2 |
| 0,5 | 52,8 | 36,4 | 1,47 |
| 0,7 | 123,0 | 63,5 | 1,93 |
| 0,9 | 470,0 | 121,0 | 3,88 |

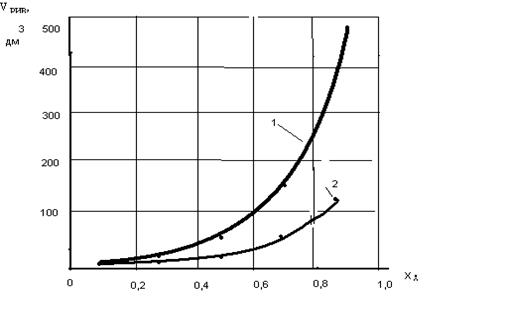
Рис. 1.1. Зависимость объёма ректоров от степени превращения:
1- непрерывный реактор идеального смешения (РИС-Н);
2- реактор идеального вытеснения (РИВ)
Пример 2.3
Реакцию омыления этилацетата щелочью
NaOH + CH3COOC2H5 = CH3COONa + C2H5OH
можно проводить в реакторах разных моделей.
Рассчитать объемы РИС-Н, РИВ и К-РИС, необходимые для достижения заданной степени превращения и сравнить эффективность указанных реакторных систем.
Условия
Этилацетат и щелочь подаются в реактор отдельными потоками и смешиваются перед входом в реактор.
Концентрация щелочи в потоке - СNaOH пот = СAпот = 0,16 моль/дм3;
Концентрация этилацетата в потоке - СEАпот = СВпот = 0,12 моль/дм3;
Общий объемный расжод реагентов - VC = 6 м3/ч;
Соотношение между объемным расходом щелочи - VNAOH = VA и этилацетата
– VЭА = VB составляет VA: VВ = 1:3
Константа скорости реакции (при температуре 20ºС) К = 5,0 дм3/моль мин
Степень превращения щелочи – xNaOH = XA = 0,7
Объем единичного реактора в каскаде -  0,1 м3
0,1 м3
Решение
а) определение объема единичного РИС-Н
Объем РИС-Н равняется:

где τзм – время пребывания реагентов в реакторе смешения.
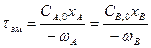
Скорость реакции –ωА или –ωВ (они в данном случае равные, так как стехиометрические коэффициенты при А и В одинаковые и равные 1) с учетом того, что один из компонентов реакции взятый с некоторым излишком, определяется по уравнению:
 ,
,
где СА и СВ – концентрации щелочи и этилацетата в реакторе, при степени превращения хА, моль/дм3;
СА,0 и СВ,0 – начальные концентрации щелочи и этилацетата, моль/дм3;
Последние рассчитывают, исходя из концентрации щелочи и этилацетата в потоках
(САпот и СВпот ), и соотношение объемных затрат VA и VB:
 моль/дм3
моль/дм3
 моль/дм3
моль/дм3
Для расчета скорости реакции необходимо еще знать хВ. Она не равняется хА так как А и В взятые не в стехиометрических соотношениях
(в избытке -В)
Чтобы не рассчитывать каждый раз хВ:
 ,
,
ее можно выразить через хА.
 ,
,
можно записать

СВ,0 также можно выразить через СА,0.
Исходя из соотношения начальных концентраций:

находим

Тогда
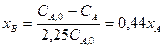
Окончательно для расчета скорости реакции получаем уравнение:
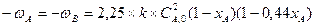
Находим скорость при хА=0,7:
-ωА= 2,25 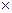 5
5 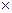 0,042(1-0,7)(1-0,44
0,042(1-0,7)(1-0,44 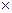 0,7) =37,4
0,7) =37,4 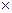 10-4 моль/дм3
10-4 моль/дм3 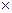 мин
мин
Время пребывания в реакторе смешения:
 мин.
мин.
Объем реактора смешения
VRзм = VCτзм = 100 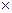 7,49 = 0,749 м3 = 749 дм3
7,49 = 0,749 м3 = 749 дм3
б) определение объема реактора идеального вытеснения VРИВ
VРИВ = VCτвит
τвит =  ,
,
тогда
VРІВ = VC 
Для нахождения численного значения интеграла применяют способ графического интегрирования. Для этого необходимо построить зависимость подинтегральной функции от переменной, по которой ведется интегрирование, т.е.

Данные для построения этой зависимости приведенные в табл. 2.4.
Таблица 2.4
СА 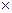 103,моль/дм3 103,моль/дм3
| ||||||||
| хА | 0,2 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 | |
-ωА 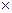 103,
моль/дм3 103,
моль/дм3 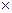 мин мин
| 18,0 | 13,1 | 8,9 | 7,02 | 5,3 | 3,74 | 2,33 | 1,09 |
 дм3 дм3 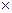 мин/моль мин/моль
| 55,6 | 76,33 | 112,4 | 142,5 | 188,7 | 267,4 | 429,2 | 917,4 |
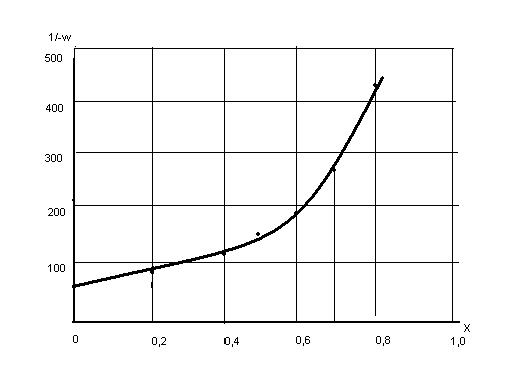
Рис. 2. Зависимость обратной величины скорости от степени превращения
На рис.2. построенная зависимость  и показана площадь, который численно равняется значение определенного интеграла. Для нашего случая S = 41,4 дм3 моль/мин. Тогда τвит = СА,0·Ѕ = 0,04?41,4 = 1,66 мин
и показана площадь, который численно равняется значение определенного интеграла. Для нашего случая S = 41,4 дм3 моль/мин. Тогда τвит = СА,0·Ѕ = 0,04?41,4 = 1,66 мин
Объем реактора идеального вытеснения
Vвит =VС·τвит =100·1,66 = 166 дм3 = 0,166 м3
в) определение объема каскада реакторов идеального смешения
Для расчета числа реакторов в каскаде применим графический метод. Для этого требуется графическая зависимость  , построенная по данным табл. 2.4. и приведенная на рис.3
, построенная по данным табл. 2.4. и приведенная на рис.3
Для каждой ступени каскада справедливое уравнение для единичного РИС-Н
 ,
,
из которого легко получить следующую зависимость

Это уравнение прямой с тангенсом угла наклона а, равным
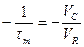 .
.
Из точки со значением начальной концентрации СА,0 = 0,04 моль/дм3 проводим прямую с 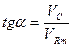

(VC = 6 м3/ч = 100 дм3/мин; VRm = 0,1 м3 = 100 дм3)
 Рис. 3. Зависимость скорости реакции от концентрации
Рис. 3. Зависимость скорости реакции от концентрации
Таким образом, для осуществления реакции нужны были бы следующие объемы реакторов:
РИС-Н - 0,749 м3
РИВ - 0,166 м3
К-РИС - 0,500 м3
Пример 2.4.
Найти кинетическое уравнение реакции, которая протекает в газовой фазе по схеме

на основании экспериментальных данных, приведенных в таблице 2.5.
| № опыта | |||||
| Время τ (для условий на входе в реактор), с | 25,4 | ||||
| Степень превращения хА | 0,22 | 0,63 | 0,75 | 0,88 | 0,96 |
Таблица 2.5
Исходная концентрация СА,0 = 0,325 кмоль/м3
Решение
Для каждого с пяти опытов вычислим значение скорости реакции, используя для этого характеристическое уравнение для реактора идеального смешения (значение скоростей реакции приведены в табл.6).

Принимаем, что скорость реакции описывается кинетическим уравнением вида:

 (а)
(а)
Реакция протекает с изменением объема, коэффициент изменения объема, εА равняется:
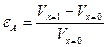

С учетом коэффициента изменения объема уравнения (а) можно записать в виде:

Для проверки соответствия этого уравнения экспериментальным данным логарифмируем его:
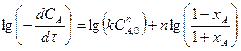 (б)
(б)
и построим график в координатах (рис. 3)

(данные для построения графика приведенные в табл. 2.6).
Таблица 2.6
| № досліда | τ, сек | ХА | 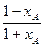
| 
| 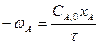
| 
|
| 0,22 | 0,639 | 1,805 | 281∙ 10-5 | 3,440 | ||
| 0,63 | 0,277 | 1,356 | 67 ∙10-5 | 4,828 | ||
| 0,75 | 0,143 | 1,156 | 30,1∙ 10-5 | 4,479 | ||
| 0,88 | 0,064 | 2,805 | 10,8∙ 10-5 | 4,033 | ||
| 0,96 | 0,021 | 2,322 | 2,71∙ 10-5 | 5,433 |
В результате получаем прямую линию, итак, вид кинетического уравнения избран правильно.
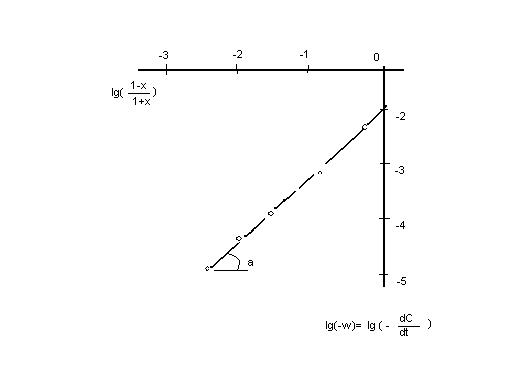
Рис. 4. Определение кинетических констант реакции
Из наклона прямой находим значение n:

Величина отрезка, который отсекается на оси ординат, представляет
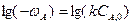 при хА=0, когда
при хА=0, когда 
Из величины этого отрезка определяем значение константы скорости по уравнению «бы»:

или
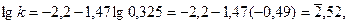
откуда к = 3,4·10-2.
Таким образом, кинетическое уравнение приобретает вид:

 кмоль/м3·сек-1
кмоль/м3·сек-1
Пример 2.5
Определите объем реактора идеального вытеснения (РИВ) для проведения газофазной реакции, описываемой кинетическим уравнением первого порядка (n = 1).
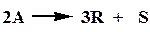
Условия
Давление Р 1000 Па
Скорость подачи реагента А, ВА,0 2,5· 10-3 кмоль· сек-1
Степень превращения хА = 0,9
Температура 457?С
Константа скорости реакции К 1,25·10-3
Решение
Объем РИВ находим по уравнению:
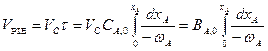 (а)
(а)
Реакция протекает с изменением объема реагентов. Учитывая то, что в этом случае для реакции первого порядка время пребывания
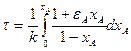
уравнение примет вид:
 ,
,
где

Определим СА,0 по уравнению:
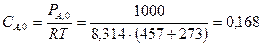 кмоль· ч-3
кмоль· ч-3
(R = 8,314 кДж· кмоль-1· град-1)
Тогда
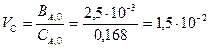 м3· сек-1
м3· сек-1
 м3
м3
Дата публикования: 2015-10-09; Прочитано: 3771 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
