 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Материальные балансы
|
|
Химико-технологические расчеты составляют главную, наиболее трудоемкую часть проекта любого химического производства, они же являются завершающей стадией лабораторного технологического исследования и выполняются также при обследовании работающих цехов и установок. Целью этих расчетов может быть определение кинетических констант и оптимальных параметров производства или же вычисление реакционных объемов и основных размеров химических реакторов.
Материальные и тепловые расчеты являются основой технологических расчетов. К ним следует отнести определение выхода основного и побочных продуктов, расходных коэффициентов по сырью, производственных потерь. Только определив материальные потоки, можно произвести необходимые конструктивные расчеты производственного оборудования и коммуникаций, оценить экономическую эффективность и целесообразность процесса. Составление материального баланса необходимо как при проектировании новых производств используется опыт существующих с учетом результатов современных новейших исследований. На основе сравнительного технико-экономического анализа действующих производств, возможно выбрать наиболее рациональную технологическую схему, оптимальные конструкции аппаратов и условия осуществления процесса.
Материальный баланс может быть представлен уравнением, левую часть которого составляет масса всех видов сырья и материалов, поступающих на переработку G, а правую – масса получаемых продуктов G’ плюс производственные потери Gпот.
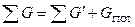 (1.1)
(1.1)
Балансы ХТС передают законы сохранения массы - материальные балансы и энергии - энергетические балансы, в частности тепловые балансы. Балансы ХТС складываются, как правило для стационарных процессов или для ХТС в целом, или для отдельных элементов или групп элементов. В последних случаях из схемы “вырезается” элемент или совокупность элементов (рис. 1)
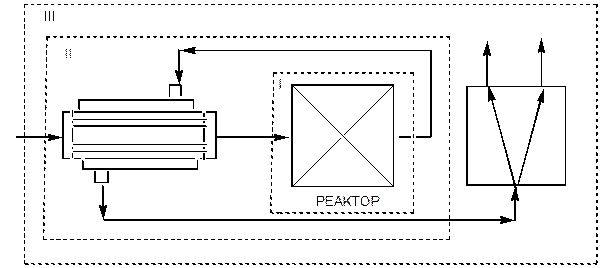
Рис 1. К порядку расчета ХТС
Выделено: І- один элемент; ІІ – группа элементов; ІІІ – ХТС в целом.
Таблица 1. Материальный баланс
G1, G2 ,G3 – массы исходных веществ; G4 ,G5,G6 – массы целевого, побочного продуктов и отходов соответственно.
| Приход | Расход | ||||||
| Исходное вещество | кг | м3 | % | продукт | кг | м3 | % |
| G1 G2 G3 | G4 G5 G6 | ||||||
| Всего | Всего |
Для всех производств в начале изложения технологического процесса по каждой стадии в таблице 3 приводят сведения о видах и количестве (массе, объема, кг/молях, штуках) используемых и получаемых в производстве сырья, полуфабрикатов, материалов, отходов, потерь и готового продукта. Таблица 3 нумеруется в зависимости от номера стадии:3.1, 3.2, 3.3 и т.д. Стадии по ходу технологического процесса имеют сквозную нумерацию, независимо от их индекса: «ВР», «ТП», «УМО» и др.
Таблица 2.. Количество израсходованной и полученной продукции на стадии
| Наименование | Содержание основного вещества % масс. | Израсходовано и получено | ||||||
| масса | Объем, дм3 | Коли- чество штук | ||||||
| кг | кг основного вещества | кг/моль | ||||||
 1– израсходовано на стадии:
1– израсходовано на стадии:
Полупродуктов:
Сырья:
Материалов:

ИТОГО:
 2– получено на стадии::
2– получено на стадии::
Полупродуктов:
(на конечной стадии-
готовых продуктов)
Отходов, в том числе:
Потерь, в том числе:
ИТОГО  :
:
Примечание:
1. Суммировать количество различных наименований продукции можно, если они имеют одинаковые единицы измерения.
2. Ниже наименований отходов и потерь указывают содержащиеся в них сырье, материалы и полупродукты. При наличии в отходах и потерях большого числа ингредиентов допускается не перечислять их, а привести только их суммарное количество.
Пример 1
В реактор для гидратации ацетилена в ацетальдегид производительностью 1 т/час ацетальдегида вводят ацетилен, который содержит 2 %
инертных примесей.Ацетилен в реакторе гидратируется на 40%, а непрореагировавший ацетилен после отделения от ацетальдегида возвращают назад. Определите выход ацетальдегида, если для поддерживания
концентрации инертных примесей на уровне 25 % часть газа выбрасывается в атмосферу.
Решение
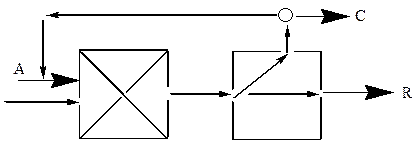
CH ≡ CH + H2O → CH3COH
М.м. М.м. М.м.
26 18 44
Производительность реактора 1т/час =1000кг/44 = 22,72кг моль/ч.
Обозначим количество введенного свежего газа через А, количество полученного ацетальальдегида R и выведенного из кругооборота газа (сдувка) - С. В таком случае молярный баланс всех веществ будет следующим:
NA = NR + NC или NC = NA - NR
В этом уравнении два неизвестных, поэтому нужное еще одно уравнение.
Баланс по ацетилену:
0,98NA = NR + 0,75NC
Баланс по инертным примесям:
0,02NA = 0,25 NC
Получаем систему уравнений:
NA = NR + NC
0,02NA = 0,25 NC
Откуда NA = 22,72 + NC, NC = 1,976
Выход ацетальдегида Ф = 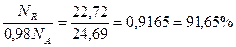
Пример 2
Аммиачная установка производительностью 1000 т/сут делает на синтез- газе 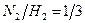 который вместит 1% инертных примесей.
который вместит 1% инертных примесей.
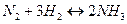
Которой должна быть сдувка, чтобы содержимое инертных смесей, в газе который циркулирует, не превосходил 20%.

N2 + 3H2 = 2NH3
г.г. г.г. г.г.
28 2 17
Решение
Производительность реактора 1000т/пор =1000кг ּ103/17 = 58,82 ּ103 кмоль/доб.
Визначим количество введенного свежего газа через А, количество полученного аммиака R и выведенного из кругооборота газа (сдувка) - С. В таком случае молярный баланс всех веществ будет следующим:
NA = 2NR + NC или NC = NA - 2NR
В этом уравнении два неизвестных, поэтому нужное еще одно уравнение.
Баланс по азото-водородной смеси:
0,99NA = 2NR + 0,2NC
Баланс по инертным примесям:
0,01NA = 0,2NC
Получаем систему уравнений:
NA = 2NR + NC
0,01NA = 0,2 NC
Откуда NA = 2ּ58,82 ּ103 + NC,
NC = 6,192 ּ103 кмоль/доб = 22,4 ּ6,192 ּ103 = 138,7 ּ103 м3/доб
Дата публикования: 2015-10-09; Прочитано: 509 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
