 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Будова деревини. 3 страница
|
|
ОЛОВО це сріблясто-білий, м'який, неміцний і вельми пластичний метал. Добре прокатується в тонкі листи. Щільність 7,29 г/см3, температура плавлення 231,9°С. Олово з природі зустрічається у вигляді з'єднань з киснем - каситериту (олов'яного каменя). Завдяки своїм властивостям олово знаходить широке застосування. Воно застосовується для захисних покриттів посудних виробів, виробництва білої жерсті, олов'яної бронзи, легкоплавких припоїв, підшипникових сплавів, фольги. Олово випускається 6 марок: ОВЧ - 000 (олово високої чистоти) - застосовується для виготовлення виробів напівпровідникової техніки, 01 - для лудіння жерсті, 01ПЧ - для лудіння консервної жерсті. Важливе значення мають олов'яно-свинцеві припої, що позначаються, ПОС- 90, ПОС - 61, ПОС - 50, ПОС - 40 і ін. Цифри указують на вміст олова у відсотках.
НІКЕЛЬ - метал світло-сріблястого кольору, блискучий, тугоплавкий (температура плавлення 1455°С), тягучий з щільністю 8,9 г/см3. Нікель має малу електропровідність.
У природі він зустрічається у вигляді сірчистої руди - так званого залізонікелевого колчедану, що містить до 22% нікелю і до 42% заліза; у вигляді сернистомиш’якової руди - нікеліну, що містить до 44% нікелю; силікатної руди – ревденскиту. Залізо нікелевий колчедан є головною вихідною сировиною для отримання металевого нікелю. Очищають нікель шляхом електролізу або окислювальною плавкою. Промисловість випускає технічний нікель із вмістом 97 6 - 99.9% нікелю Нікель має високу стійкість до дії лугів, до корозії, проте легко розчиняється в сірчистій і азотній кислотах, гірше - в сірчаній і соляній.
Оскільки|тому що| нікель стійкий до дії кисню повітря, то його застосовують для створення|створіння| захисних-декоративних покриттів, а також для виготовлення сплавів з|із| іншими металами Нікель вводять|запроваджують| до складу корозійностійких |хромонікелевих сталей|, сплавів з|із| особливими тепловими властивостями, магнітних, електротехнічних| високої напруги, жароміцних сплавів
ХРОМОМ є метал з яскраво сріблястим блиском, він дуже твердий, тугоплавкий (температура плавлення 1950°С), щільність 7,14 г/см3. Цей метал відмінно полірується, стійкий до стирання і атмосферної корозії, слабо розчиняється з розведення сірчаній і соляній кислотах.
Хром зустрічається в природі у вигляді хромошпинелідів, що містять 18 - 62% окислів хрому Сr2О3, і хромату свинцю - мінералу крокоїту. що містить близько 31% хромового ангідриду СrО3. Хром отримують в електропечах відновленням окислу хрому вугіллям або нагріванням Сr2О3, з порошком металевого алюмінію. Алюмотермічним способом хром виділяють до 97-98,5%.
Застосовують хром як складову частину багатьох сплавів - хромистої| і хромонікелевої неіржавіючої|нержавіючій| сталі, ніхрому, хромалей| тощо. Металевий хром використовують як протикорозійне і декоративне| покриття на інших металах. Хромові покриття відрізняються високою зносостійкістю. Хромують частини|частки| машин і приладів, предмети широкого застосування|вживання|, інструменти, вимірювальні прилади, годинники тощо. З'єднання|сполучення| тривалентного хрому застосовують для дублення натуральних шкір.
СВИНЕЦЬ - синювато-сірий блискучий метал, дуже пластичний, з низькою твердістю. Щільність свинцю 11,3 г/см3, температура плавлення 327СС. Розбавлені соляна і сірчана кислоти не діють на свинець, краще всього він розчиняється з азотній кислоті середньої концентрації, стійкий до дії лугів. З'єднання свинцю дуже отруйні.
Свинець застосовується для відливання|виливка| друкарського шрифту і стереотипних матриць для свинцево-олов’янистих| і свинцевих бабітів| - підшипникових сплавів, в хімічній промисловості (для кислотостійких баків), для виробництва труб|труба-конденсаторів| акумуляторних| пластин, захисних оболонок| електричних кабелів|. Зі|із| свинцю| із|із| вмістом|вмістом| 0,3% миш'яку ллють дріб. Свинець входить до складу різних| металевих сплавів
ТИТАН - легкий| метал, щільність 4,54 г/см3 температура плавлення 1730°С|. За поширеністю в природі цей елемент займає|позичає| четверте місце|місце-миля| (після|потім| алюмінію, заліза і магнію). Виробляють титан переважно з|із| мінералів рутилу і ільменіту.
Титан має високі механічні властивості, добре обробляється тиском|тисненням| і піддається спаюванню|зварюванню|. За своєю корозійною| стійкістю титан перевершує навіть високолеговані корозійностійкі стали. Його застосування|вживання| постійно розширюється|, для багатьох цілей він перспективніший|перспективний|, ніж будь-які інші метали. В даний час|нині| титан ще дефіцитний, оскільки|тому що| не розроблені високоефективні методи його отримання|здобуття|.
Титан можна легувати алюмінієм, оловом, хромом, молібденом| та іншими елементами. Сплави титану з|із| алюмінієм і оловом відрізняються високою жароміцністю. Високою міцністю (вчетверо| вище, ніж у|біля| звичайної конструкційної сталі) володіє спеціальний титановий|титан| сплав TIV| 13 Сг 11 А 14 (Ti+13%V+11| %Cr+4%AI).
Майже 90 % титана, що виплавляється в світі, споживають авіація, космічна і ракетна техніка. Найбільшим споживачем| титану є|з'являється| хімічна промисловість Титан використовується| у виробництві товарів народного споживання|вжитку| (посуд, столові прилади).
ВОЛЬФРАМ - білий важкий|тяжкий| метал з|із| дуже високою температурою| плавлення (3380°С|), по міцності не має рівних серед металів. Характеризується високою корозійною, стійкістю.
Вольфрамом легують швидкорізальні інструментальні стали і з невеликою кількістю добавок його використовують для виготовлення ниток накалювання в електричних лампах, деталей радіоламп, кінескопів, нагрівачів електричних печей і так далі
СРІБЛО - сріблясто-світлий, блискучий метал зі щільністю 10,49 г/см3 і температурою плавлення 960,5°С Срібло має хорошу ковкістю, тягучість, може прокатуватися в якнайтонші листи, добре полірується і відображає світлові і теплові промені. Теплопровідність і електропровідність срібла перевершує відповідні показники інших металів. Срібло стійке до дії атмосферних умов, чорніє під дією сірководню. З кислот на срібло найенергійніше діє азотна кислота.
У природі срібло зустрічається як в самородковому| вигляді|виді|, так і в різних рудах. З|із| руд, попередньо| тонко подрібнених, срібло виділяється слабким|слабим| розчином (0,2-0,6%) ціаністого натрію і осідає алюмінієвою стружкою. Очищається срібло, головним чином, методом електролізу.
Для виготовлення виробів (столових приладів, ювелірних виробів|) срібло застосовують у вигляді сплавів з|із| міддю. У таких сплавах| зміст|вміст| срібла називається пробою, під якою розуміють| кількість частин|часток| срібла, що містяться|утримуються| в 1000 частинах|частках| сплаву|. Найважливіші проби срібла 800, 875, 916. Застосовують також срібло для покриття інших металів (сріблення) у виробництві ювелірних виробів, годинників, посуду, столових приладів, для приготування кіно - і фотоматеріалів (світлочутливих емульсій для пластинок|платівок| і смужок|, фотопаперових емульсій), в медицині, у виробництві дзеркал тощо.
ЗОЛОТО є одним з найважчих металів. Метал жовтого кольору, з сильним блиском. Щільність 19,3 г/см3, температура плавлення 1063°С Це м'який, пластичний, але дуже стійкий метал, розчиняється тільки в царській горілці, в хлорній і бромистій воді, а також в розчині ціаністого калію. Для виробництва ювелірних виробів застосовують сплави золота з міддю і сріблом. Надбавка міді значно підвищує твердість золота, унаслідок утворення твердих розчинів. Встановлені наступні проби золота: 375, 500, 583, 750 і 958. Застосовується золото для виготовлення ювелірних виробів і в якості захисно-декоративного покриття.
ПЛАТИНА - благородний метал світло-сірого кольору. Пложость-21,5 г/см3, температура плавлення-1773°С. Платина стійка до царської горілки, хлорної води, розплавлені луги її роз'їдають. Володіє значною твердістю і великою тягучою. Платина є|з'являється| незамінним металом| для виготовлення тиглів, чашок для хімічних лабораторії. У ювелірних виробах застосовується для облямовування коштовних каменів.
ТЕРМІНОЛОГІЧНИЙ СЛОВНИК
МЕТАЛИ — прості речовини, що мають у звичайних умовах характерними властивостями: високою электро- і теплопровідністю, негативним температурним коефіцієнтом електропровідності, здатністю добре відображати електромагнітні хвилі (блиск і непрозорість), високою міцністю і пластичністю.
ЧОРНІ МЕТАЛИ — сплав заліза з вуглецем, в якому можуть міститися в більшій або меншій кількості інші хімічні елементи. Кобальт, нікель, а також близький до них за властивостями марганець нерідко відносять до чорних металів. Чорні метали отримали найбільше розповсюдження|поширення|, що обумовлене відносно високим вмістом заліза в земній корі, його низькою вартістю, високими механічними і технологічними властивостями.
ЧАВУН — сплав заліза (основа) з вуглецем (зазвичай 2...4%), що містить постійні домішки Si, Mn, S, Р, а іноді і легуючі елементи Сг, Ni, V, A1 і ін. Як правило, крихкий.
СТАЛЬ — сплав заліза (основа), що деформується (ковкий), з вуглецем (до 2%) і (або) іншими елементами (сплави). Вид мікроструктури сталей і сплавів, що остаточно сформувалася, залежить від вмісту в них вуглецю.
КОНСТРУКЦІЙНІ СТАЛІ І СПЛАВИ повинні мати певний комплекс механічних властивостей, що забезпечує тривалу і надійну роботу матеріалу в умовах експлуатації, і гарних|добрих| технологічних властивостей (обробка| тиском|тисненням|, різанням, загартовування, зварюваності і ін.).
ІНСТРУМЕНТАЛЬНІ СТАЛІ І СПЛАВИ — литі тверді сплави. Тверді сплави — матеріали з високими твердістю, міцністю, ріжучими і іншими властивостями, що зберігаються при нагріві до високих температур. Розрізняють литі і спечені (порошкові) тверді сплави.
ПРЕЦИЗІЙНІ СПЛАВИ — металеві сплави з особливими фізичними властивостями (магнітними, електричними, тепловими, пружними) або рідкісним поєднанням властивостей, рівень яких в значній мірі обумовлений точністю хімічного складу, відсутністю домішок, ретельністю виготовлення і обробки.
ЛАТУННЮ називається сплав міді з|із| цинком Кількість цинку, що міститься|утримується| в латуні, коливається|вагається| в широких межах (від 4 до 47%).
БРОНЗОЮ називають сплави міді з|із| оловом, алюмінієм, берилієм| і іншими металами. Прості з|із| них - олов'яниста бронза, відома ще з бронзового століття|віку|.
МЕЛЬХІОР сплав мідь (80 -81%) і нікелю (19 - 20%), застосовується для виготовлення високоякісного посуду, столових приладів, галантерейних виробів
«НЕЙЗИЛЬБЕР» - сплав міді з 20% нікелю і 15% цинку (з німецької «Нове срібло»). Цей сплав використовується для виготовлення посуду, художніх виробів, а також для пружин, мембран і інших деталей в приладобудуванні і інших галузях промисловості.
ЛІТЕРАТУРА
1.Ещенко В.Ф., Леженин Е.Д. Товароведение хозяйственных товаров. В 2-х томах. Т. 2. - М.: Экономика, 1984. - 400 с.
2.Закусілов А.П., Полікарпов І.С., Стадник Б.Я. Матеріалознавство і технологія виробництва товарів народного споживання. - К.: 1994. - 292с
3.Зіміна Н.К., Андрієнко В.М., Савчук Н.В. Матеріалознавство та технологія непродовольчих товарів:Навч. посібник.-К.: ІЗМН, 1998 р. с.114.
4.Федаева Н.И.Основы технологии производства товаров важнейших отраслей промышленности.- Гомель.-1995г.-152 с.
ТЕМА 7. ОБРОБКА МЕТАЛІВ ТА ЇХ СПЛАВІВ, ЗАХИСТ ВІД КОРОЗІЇ
7.1. ПОНЯТТЯ ПРО КОРОЗІЮ, МЕТОДИ ЗАХИСТУ
ВИДИ КОРРОЗІЇ
Корозією називають процес руйнування металів під час взаємодії| його із|із| зовнішнім середовищем|середою|. Розрізняють такі|слідуючі| види корозії: суцільну, яка розповсюджується|поширюється| на всю поверхню виробу; місцеву – де корозійне руйнування відбувається|походить| на окремих ділянках поверхні; міжкристалічну|, яка протікає| по межах|кордонах| зерен, в результаті|унаслідок| якої знижуються механічні| властивості металів. За механізмом процесу руйнування розрізняють| хімічну і електрохімічну|електрохімія| корозію.
Хімічна корозія — руйнування металів, яке протікає в сухих газах при підвищених температурах (газова корозія) і в неелектролітах| (бензині, сірчистій нафті, розплавах| солей|соль|). Прикладом|зразком| газової корозії може бути окислення| сталі під час її нагрівання в термічних печах (окалійноутворення|). Корозія в неелектролітах| — це корозійне руйнування металевих деталей у змащувальних|мастильних| маслах|мастилах|, які під впливом| температури, тиску|тиснення| під час тертя, окислення|окислений| і каталітичної| дії металів розкладаються|розкладають| із|із| виділенням кислот та інших| продуктів, що викликають|спричиняють| руйнування металів.
Електрохімічна|електрохімія| корозія — руйнування металів в результаті дії на них водних розчинів електролітів — солей|соль|, кислот, лугів. До цього виду|виду| корозії відносять і атмосферну корозію, при якій волога з|із| повітря конденсується на поверхні| металу, а в ній розчиняються агресивні гази. Наявність на поверхні металу пилу та інших забруднень підсилює|посилює| адсорбцію вологи і газів, а волога|вогка| плівка на поверхні| є електролітом.
Розвиток корозії залежить від внутрішніх і зовнішніх чинників|факторів|. До внутрішніх відносять склад сплаву, структура, наявність неметалевих| включень|приєднань|, стан|достаток| поверхні, ступінь|міру| напруги| металу, а до зовнішніх — середовище|середу|, його концентрація і температура.|
Електрохімічна|електрохімія| корозія протікає таким чином. Метали і сплави завжди хімічно і фізично неоднорідні. Компоненти сплаву, різні фази структури, чистий метал і окисна плівка, дві сусідні ділянки з|із| різною напруженістю утворюють комплекс анодних і катодних ділянок, що є мікроскопічними гальванічними парами. А це призводить|призводить| до того, що на межі|кордоні| метал — електроліт відбувається|походить| розчинення| анодних ділянок. У гальванічній парі руйнується той метал, який виділяє| більшу кількість позитивно заряджених іонів і, відповідно|, сам отримує|одержує| вищий негативний|заперечний| заряд.
Якщо метали розташувати в наступний ряд: Аu, Рt, Аg, Сu, Вi, Sb, Рl, Sn, Ni, З, Сr, Fе, Zn, Мn, Тi, А1, Мg, то вийде, що будь-який метал, який займає в цьому ряду правіше положення, руйнуватиметься у контакті з металом, що займає лівіше положення, і тим сильніше, чим далі ці метали знаходяться один від одного в ряду.
Однорідність структури, наявність суцільних плівок, відсутність внутрішньої напруги|напруження| знижують інтенсивність корозії, а неоднорідність структури, легка розчинність плівок, напряжений| стан|достаток| металу збільшують її. Чисті метали кородують| у меншій мірі, ніж їх сплави, однофазні сплави чинять опір корозії краще, а багатофазні гірше. Менше кородують| метали, що мають чисту поверхню виробів. Метал після|потім| деформації зменшує опір корозії. Підвищення температури прискорює корозію в 1,5—2 рази на кожні| 10°| С.
Структура сталі в рівноважному стані|достатку| зазвичай|звично| складається з двох фаз — фериту і цементиту|. При електрохімічній|електрохімія| корозії цементит| залишається незмінним, а ферит розчиняється і з речовиною| електроліту утворює іржу.
Стан металу по відношенню до дії певного середовища може бути активним і пасивним. Метали легко руйнуються в корозійному середовищі в активному стані. У пасивному стані метал не кородує. Пасивність в певному корозійному середовищі металу додають зазвичай плівки оксидів деяких елементів (хрому, алюмінію, кремнію). Якщо алюміній покритий тонкою плівкою А1203, він не кородує у воді, але якщо цієї плівки немає, то алюміній у воді легко розчиняється.
ЗАХИСТ МЕТАЛІВ ВІД КОРОЗІЇ
Методи захисту від корозії:
· зміна складу металу;
· зміна складу оточуючого середовища;
· електрохімічний захист;
· раціональне конструювання виробів;
· нанесення захисних покриттів.
Зміна складу металу. При цьому до сплаву додають один або декілька легуючих елементів, що утворюють на його поверхні щільні оксидні плівки, які захищають метал від корозії. Окрім цього під час легування сплави, як правило, набувають однофазної структури, в значно меншій мірі здатній до електрохімічної корозії. Залізовуглецеві сплави набувають корозійної стійкості в агресивному середовищі за рахунок легування їх хромом, нікелем, молібденом, алюмінієм, кремнієм. Підвищення корозійної стійкості виробів із алюмінію та його сплавів досягається за рахунок видалення шкідливих домішок, перш за все заліза.
Зміна складу оточуючого середовища. Агресивність оточуючого середовища зменшують за рахунок видалення з нього речовин, які прискорюють корозію або введення речовин, що уповільнюють корозію. Вироби розміщують в поліетиленові пакети в які додають силікагель. Силікагель здатний поглинати вологу до 35% власної маси, зневоднюють середовище і вироби в якому вони знаходяться. Окрім цього використовують інгібітори (уповільнювачі) корозії. Ці речовини мають високу пружність пара, швидко заповнюють оточуюче середовище і, адсорбуються на металевій поверхні, захищають її від корозії (нітрити заміщених амінів, складні ефіри карбонових кислот, карбонати заміщених амінів, бензонат натрію обробкою їх у водних розчинах уповільнювачів.). Для захисту металевих виробів від атмосферної корозії використовують контактні уповільнювачі (нітрат натрію), які наносять на поверхню виробів
Електрохімічний захист. Проводиться з використанням протекторів. До виробу, який належить захистити від корозії, підєднують протектор з іншого металу, який має в даному корозійному середовищі більший електровід’ємний потенціал, ніж потенціал металу з якого виготовлено виріб. В такій гальванічній парі протектор буде виконувати роль аноду, а виріб – роль катоду. Під час корозії метал протектору руйнується і захищає метал виробу. В якості протекторів використовують цинк, кадмій, алюміній. Такий захист за допомогою протектору використовують під час виготовлення стального оцинкованого посуду, приладів для вікон та дверей тощо.
Раціональне конструювання виробів. Під час розробки конструкції металевого виробу слід враховувати не тільки максимальну відповідність призначенню, а й менше руйнування його від корозії, не допускати контактів металевого виробу з електродними потенціалами, які значно відрізняються один від одного, по можливості не допускати зазорів у виробах, важкодоступних місць для очищення, гострих кутів та напружень в металі.
Нанесення захисних покриттів. Всі покриття за своєю природою поділяють на: металеві, неметалеві та у вигляді оксидних плівок.
Металеві покриття поділяють на анодні і катодні. При анодному покритті захисний метал по відношенню до основного є анодом (мал. 105, а).
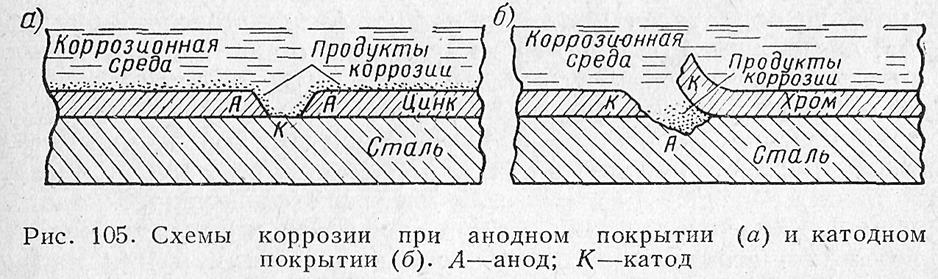
При місцевому руйнуванні покриття і потраплянні туди електроліту утворюється гальванічна пара «сталь — покриття». При цьому починає|розпочинає| розвиватися електрохімічна| корозія, при якій руйнується тільки|лише| покриття. Руйнування це буде незначним, оскільки|тому що| катодна поверхня значно менше анодної. Прикладом|зразком| анодних покриттів є|з'являється| цинкування заліза для захисту від атмосферної корозії.
Катодні покриття захищають метали тільки|лише| механічно|. Поки|доки| вони суцільні, метал надійно захищений від корозії|. У разі ж місцевого руйнування покриття починається|розпочинає| інтенсивна корозія заліза (мал. 105, б). Прикладами|зразками| катодних покриттів заліза є його хромування, нікелювання і лудіння| (покриття оловом), які широко застосовують, оскільки|тому що| хром, нікель і олово мають високу хімічну стійкість.
Існує декілька методів нанесення захисних металевих| покриттів. Гальванічне покриття застосовують при хромуванні, цинкуванні, кадміюванні і мідненні. При цьому отримують|одержують| тонкий і щільний шар захисного металу. Для нанесення більш товстого шару цинку, алюмінію, кадмію, латуні використовують металізацію, тобто напилення розплавленого металу на поверхню виробу за допомогою спеціального пістолета-розпилювача. Значне розповсюдження|поширення| має дифузійний метод насичення поверхневого| шару хромом, алюмінієм та іншими металами.
Найбільш поширеним металевим покриттям є хромування, оскільки|тому що| хромові покриття відрізняються корозійною| стійкістю, високою твердістю, зносостійкістю, дзеркальним блиском і довговічністю.
Цинкування застосовують головним чином для захисту покрівельного| заліза від атмосферної корозії. У харчовій, головним чином| в консервній, промисловості застосовують лудіння. Нікелювання застосовують виключно|винятково| з декоративною метою. Для захисту| металів від дії морської води застосовують кадміювання. Оксидування і фосфатування — методи захисту металу від корозії, що базуються на утворенні складних за складом плівок на поверхні деталей, які захищаються.
Оксидні плівки отримують|одержують| під час оксидування (вороніння |), яке полягає в кип'ятінні деталей у водному розчині, який містить|утримує| їдкий натр|, селітру і перекис марганцю. При цьому на металі утворюється гарна плівка темно-синього або чорного кольору|цвіту|, що складається в основному з магнітного окислу заліза, яка і захищає|запобігає| метал від окислення|окислений|.
Фосфатні плівки отримують|одержують| під час фосфатування, яке полягає в обробці виробів у ваннах, які містять|утримують| суміші фосфатної кислоти, залізних і марганцевих її солей|соль|. Фосфатна плівка, яка складається із фосфорнокислих| з'єднань|сполучень| заліза і марганцю, має світло-| або темно-сірий колір,|цвіт| гарну|доброю| корозійну стійкість в атмосферних умовах і при нагріві до 600°С|СССССсссс|із|, а також високі електроізоляційні властивості|.
Лакофарбові покриття і покриття пластмасами. Лаки, емалі, фарби|барви| і пластмаси - це композиція із|із| плівкоутворюючих речовин (масел|мастила|, смол, ефірів), розчинників, пігментів, пластифікаторів та інших компонентів. Для збільшення адгезії фарб|барв| до металів і підвищення їх захисних властивостей застосовують ґрунти, які наносять| на метал перед нанесенням основного захисного шару. Найважливішим засобом|коштом| боротьби проти|супроти| корозії є|з'являється| легування, тобто отримання|здобуття| корозійностійких|корозіоностійких| (неіржавіючих|нержавіючих|) сталей|. Високий опір корозії мають і спеціальні сплави на основі нікелю, титану і інших металів|.
Значення боротьби з|із| корозією зростає у зв'язку з електрифікацією| залізниць, оскільки|тому що| в металевих конструкціях|, що знаходяться|перебувають| поблизу контактної мережі|сіті|, виникають блукаючі струми, які|токи| прискорюють процес корозії металу.
7.2. ТЕРМІЧНА ОБРОБКА МЕТАЛЕВИХ СПЛАВІВ
Термічна і хіміко-термічна обробка є|з'являється| останнім| етапом формування властивостей металевих сплавів. Для досягнення заданих властивостей сплав певного складу піддають термообробці, головною метою|ціллю| якої є отримання|здобуття| необхідних механічних властивостей сплаву за рахунок зміни його структури.
Термічна обробка — це обробка, яка полягає в зміні структури і властивостей матеріалу заготівки внаслідок теплових дій. Основні параметри термічної обробки: температура нагріву, швидкість нагріву, тривалість витримки при температурі нагріву і швидкість охолоджування.
Вибір температури нагріву сплаву при конкретному виді термічної| обробки визначається температурами фазових перетворень (наприклад, критичними температурами на відповідній діаграмі| стану|достатки|). Температура нагріву не повинна перевищувати температуру плавлення (лінію солідус на діаграмі стану|достатку|).
Швидкість нагріву вибирається залежно від ряду|лави| чинників|факторів|: теплопровідності| матеріалу, форми і розмірів виробів, загальної|спільної| маси виробів, що нагріваються, характеру|вдачі| їх розташування в печі і деяких інших.
Тривалість витримки|витягу| при заданій температурі нагріву визначається швидкістю фазових перетворень. Витримка|витяг| необхідна для повного|цілковитого| завершення фазових перетворень і вирівнювання температури| по всьому об’єму виробу.
Швидкість охолодження|охолодження| вибирається залежно від ступіня|міри| стійкості| фази, що фіксується, при даному хімічному складі, а також від потрібних структури і властивостей.
Отже, ТЕРМІЧНОЮ ОБРОБКОЮ називають нагрівання виробів і заготовок| до певної температури у поєднанні з витримкою|витягом| при цій температурі і подальшому|наступному| охолоджуванні|охолодженні| із|із| заданою швидкістю|.
Термічна обробка може поєднуватися|сполучатися| з|із| хімічним впливом| або з|із| пластичною деформацією, що також дозволяє| змінювати|зраджувати| властивості сплавів в потрібному напрямі|направленні|.
Термічній обробці піддають вироби з|із| вуглецевої і легованої сталі, чавунів і сплавів кольорових металів. Термічну обробку застосовують для підвищення міцності ножів, ножиць, бритв, інструментів, деталей побутових машин.
Розрізняють чотири види термічної обробки: ВІДПАЛ, НОРМАЛІЗАЦІЮ|, ГАРТУВАННЯ|гартування| І ВІДПУСК|відпуск|.
ВІДПАЛ сталі полягає у нагрівання її вище або нижче температури фазових перетворень, витримці|витягу| при цій температурі і повільному охолодженні|охолодженні| разом із піччю, в термічних колодязях. В результаті|унаслідок| відпалу в сталі утворюється стійка структура, вільна| від внутрішньої напруги|напруження|; сталь стає м'якою, в'язкою і дрібнозернистою.
Розрізняють відпал першого і другого роду. ВІДПАЛ ПЕРШОГО РОДУ застосовують з метою зняття залишкової напруги|напруження| і спотворень кристалічної решітки після|потім| попередньої обробки. Відпал першого роду підрозділяють на гомогенізацію (дифузний| відпал), відпал рекристалізації і відпал для зняття залишкової напруги |напруження|.
Гомогенізацію застосовують для усунення неоднорідності в «будові|споруді| злитків|зливків| і великих відливків|виливків|, а також для вирівнювання хімічного складу всередині|всередині| зерен. Процес гомогенізації включає| нагрів| до температури 1100|...1200°С, витримку|витяг| при цій температурі протягом 8...20 год і повільне охолодження|охолодження|. Час витримки|витягу| може досягати до 100 год і залежить від маси деталі, яка обробляється.| Рекристалізаційному відпалу піддають холоднодеформовану| сталь. При холодній обробці металів (холодному плющенні, штампуванні, волочінні) де відбувається|походить| пластична деформація| викликає|спричиняє| спотворення кристалічної решітки і підвищення| твердості металевих сплавів. Таке явище називається| клепанням. Наклепаний метал стає крихким, що ускладнює |його подальшу|дальшу| обробку. Рекристалізаційний відпал здійснюють при нагріві вище порогу рекристалізації (звичайно| 700°С|), витримці|витягу| при цій температурі протягом 0,5...1,5 год, з|із| подальшим|наступним| охолодженням|охолодженням|. В процесі такого відпалу знімається клепання, підвищується пластичність сталі, міцність або твердість металу дещо знижується. Відпал також використовують для зняття залишкової напруги |напруження| для сталевих виробів після|потім| литва|лиття|, зварювання|зварювання| та механічної обробки|. Його проводять при різних температурах залежно від виду попередньої обробки (від 16°С| до 600°С|). Тривалість такого відпалу зазвичай|звично| складає 2...3 години.
ВІДПАЛ ДРУГОГО РОДУ здійснюють для зниження фазової неоднорідності сталі і проводять при температурах, що перевищують температуру фазових перетворень. Різновидами відпалу другого роду є повний ізотермічний і неповний відпал, а також нормалізація
Повний|цілковитий| відпал застосовують для перекристалізації доевтектоїдної| сталі з метою подрібнення зерен і зняття залишкової напруги|напруження|. Повний|цілковитий| відпал проводиться при температурі на 30-50°С| вище 911°| С|із| до завершення фазового перетворення і повільного охолодження|охолодження| разом із піччю. Швидкість нагріву залежить від типу|типа| печі, тривалість витримки|витягу| після|потім| нагріву складає 0,5 год - 1 год на 1 т. металу, швидкість охолодження залежить від стійкості структури сплаву. Повний відпал покращує механічні властивості сталі і використовується для підготовки заготовок до механічної обробки різанням (інструменти, болти, гайки тощо).
Для легованих сталей застосовується ізотермічний відпал, який характеризується витримкою при температурі 85СГС і більш швидким охолодженням при перенесенні в іншу піч. Для невеликих деталей час охолодження знижується в 2-3 рази, зменшується шорсткість їх поверхні, поліпшується оброблюваність різанням.. :
Дата публикования: 2015-09-18; Прочитано: 445 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
