 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Опыт №1. Определение молярной массы эквивалента алюминия
|
|
В реакциях, протекающих с выделением газа, молярную массу эквивалента вещества можно определить объёмным методом – по объёму выделяющего газа.
Методика опыта. В пробирку наливаем 5-6 мл раствора соляной кислоты НCl и на край пробирки помещаем навеску алюминия Al таким образом, чтобы металл не соприкасался с кислотой. Затем соединяем пробирку с прибором для определения объёма газа – он состоит из двух стеклянных заполненных водой трубок, соединённых между собой по типу сообщающихся сосудов. Отметив уровень воды в трубке, с которой соединена пробирка, сбрасываем навеску металла в кислоту. В ходе реакции выделяется газообразное вещество, и уровень воды в трубке, с которой соединена пробирка, понижается. Когда уровень воды в трубке стабилизируется, заканчиваем опыт.
В ходе опыта происходит следующая реакция:
2 Al + 6 HCl = 2 AlCl3 + 3 H2↑
Запишите исходные данные для расчёта молярной массы эквивалента алюминия по следующему образцу:
Исходные данные:
Масса навески – m, г;
Объём выделившегося водорода – V, мл;
Температура опыта – t, °С;
Атмосферное давление – P, мм рт. ст.;
Упругость водяных паров – h, мм рт. ст.
Приводим объём выделившегося водорода к нормальным условиям по формуле:
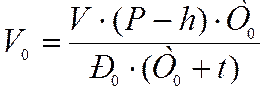 ,
,
где V – объём выделившегося водорода, мл;
Р – атмосферное давление, мм рт.ст.;
t – температура опыта, °С;
h – упругость водяных паров при температуре опыта, мм рт.ст;
Т0 – температура, соответствующая нормальным условиям, К;
Р0 – давление, соответствующее нормальным условиям, мм рт.ст.
Запишите расчёт приведения объёма выделившегося водорода к нормальным условиям по вышеуказанной формуле с учётом полученных исходных данных.
Рассчитываем молярную массу эквивалента алюминия по формуле:
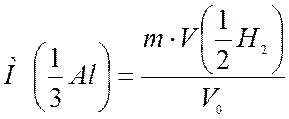 ,
,
где m – масса навески, г;
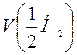 – молярный объём эквивалента водорода, мл/моль;
– молярный объём эквивалента водорода, мл/моль;
V0 – объём выделившегося водорода в пересчёте на нормальные условия, мл.
Запишите расчёт молярной массы эквивалента алюминия по вышеуказанной формуле.
Относительную ошибку опыта рассчитываем по формуле:
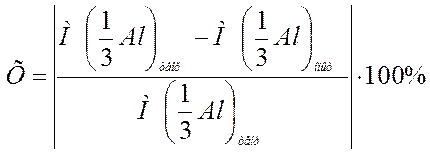 ,
,
где  – теоретическое значение молярной массы эквивалента алюминия, г/моль;
– теоретическое значение молярной массы эквивалента алюминия, г/моль;
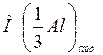 – значение молярной массы эквивалента алюминия, полученное в ходе опыта, г/моль.
– значение молярной массы эквивалента алюминия, полученное в ходе опыта, г/моль.
Запишите расчёт величины относительной ошибки опыта по вышеуказанной формуле.
Сделайте вывод о данном методе определения молярной массы эквивалента вещества и укажите, с какой ошибкой она была найдена в данном случае.
Дата публикования: 2015-09-18; Прочитано: 584 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
