 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Закон А. Авогадро (Франция 1811 г.)
|
|
«В равных объемах различных газов при (нормальных) одинаковых условиях (давлении и температуре) содержится равное число молекул».
Из закона Авогадро следует - Один моль любого газа при одинаковых условиях (нормальном давлении – 1ат. или 760 мм.рт.ст. или 101 325 кПа и нормальной температуре 0ºС (273,15 К)) занимают один и тот же объем, равный 22,4 л /моль (молярный объем).
Например, масса 1л водорода при нормальных условиях равна 0,09 г, а моляр-
ная масса молекулярного водорода равна 2,0158 г /моль
m(1л Н2) = 0,09 г /л М (H2) = 2,0158 г /моль
тогда объем занимаемый 1моль водорода равен:
V (1мольН2) = 2,0158 г /моль: 0,09 г /л = 22,4 л /моль (молярный объем).
При нормальных условиях масса 1л кислорода равна 1,429 г, молярная
масса молекулярного кислорода составляет 31,9988 г /моль.
Тогда объем занимаемый 1моль кислорода равен:
V (1мольО2) = 31,9982 г /моль: 1,429 г /л = 22,4 л/моль (молярный объем).
Следовательно, молярный объем любого газа можно рассчитать по
формуле:
Vm =  где: Vm – молярный объем газа, в л /моль;
где: Vm – молярный объем газа, в л /моль;
V – объем вещества;
n – количество вещества.
Современная формулировка - Молярный объем газа – это отношение объема вещества к количеству этого вещества.
2.7. Закон действующих масс (К.Гульдерберг и П.Вааге, норвегия,1864 – 1867).
«Скорость химической реакции при постоянной температуре прямо пропорци- ональна произведению концентрации реагирующих веществ».
Например, в реакции:
А + В = С + Д v = к 
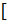 А]
А]  [ В ]
[ В ]
А + 2В = С + 2Д v = к 
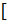 А]
А]  [ В ]2
[ В ]2
где: 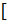 А ] и [ В ] - концентрации веществ;
А ] и [ В ] - концентрации веществ;
к - константа скорости реакции
H2SO + 2NaOH = Na2SO + 2H2O v =  к
к  [H2SO4 ]
[H2SO4 ]  [NaOH]2
[NaOH]2
Дата публикования: 2015-09-18; Прочитано: 292 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
