 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Оформлення результатів роботи. 1. Скласти схеми ГЕ. Вказати напрямок переміщення електронів по зовнішньому ланцюгу
|
|
1. Скласти схеми ГЕ. Вказати напрямок переміщення електронів по зовнішньому ланцюгу. Записати рівняння електродних процесів, скласти загальне рівняння реакції, що відображає роботу кожного ГЕ.
2. Розрахувати теоретичну величину ЕРС 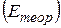 кожного з досліджених елементів, використовуючи рівняння Нернста.
кожного з досліджених елементів, використовуючи рівняння Нернста.
3. Порівняти теоретичне значення ЕРС з експериментальним.
4. Зробити висновок щодо впливу природи електродів на величину ЕРС гальванічного елемента.
Питання для самоперевірки
1. Обчислити потенціал цинкового електрода, зануреного в 0,01 М розчин сульфату цинку; потенціал водневого електрода, зануреного в чисту воду при 25 0С і тиску 1 атм.
2. Скласти схеми роботи двох ГЕ, в одному з яких мідь була б анодом, а в іншому – катодом. Написати рівняння реакцій, що відбуваються при роботі цих елементів, і розрахувати ЕРС елементів у стандартних умовах.
3. Користуючись таблицею стандартних електродних потенціалів, відзначити, який з наведених нижче атомів та іонів може:
а) окиснюватися за допомогою 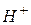 :
:

б) відновлюватися за допомогою  :
:
 .
.
Скласти молекулярні та іонні рівняння можливих реакцій.
Лабораторна робота № 14
ЕЛЕКТРОЛІЗ
Мета роботи – ознайомлення з процесами, що відбуваються при електролізі водних розчинів солей.
Дата публикования: 2015-09-18; Прочитано: 283 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
