 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Общая характеристика гравиметрического метода анализа
|
|
Гравиметрический анализ - метод количественного химического анализа, при котором количество элементарного вещества (в исследуемой пробе судят о массе вещества) получается в результате анализа.
Пример: в молоке, хлебе, во влаге. Для метода осаждения применяют реакции: обмена, разложения, комплексообразования.
Вещество, в виде которого выделяется в осадок определяемый компонент, называют осажденной формой.
Требования к осаждаемой форме:
1) Осаждаемое вещество должно быть плохо растворимо, произведение растворимости (ПР) меньше 1*10-8 моль/л;
2) осадок должен быть крупнокристаллическим;
3) осадок не должен легко загрязняется посторонними веществами из раствора (например: амфотерные осадки, особенно студенистые Al(OH)3..
Соединение, по массе которого судят о количестве определяемого компонента, называют весовой формой или гравиметрической. Иногда весовая форма совпадает с осажденной формой (например: BaSO4), если не совпадает, то необходимо, чтобы осаждаемая форма легко и быстро превращалась в весовую.
Требования к весовой форме:
1) должна иметь весовой состав, точно соответствующий химической формуле (если весовая форма не имеет точно определенный состав, то прибегают к прокаливанию);
2) полученная весовая форма должна быть химически устойчива, прокаленный осадок не должен быть заметно гигроскопичен (впитывание влаги);
3) отношение массы весовой формы к массе определенного компонента должно быть наибольшим, в этом случае погрешности определения меньше скажутся на результате анализа.
Произведение растворимости (ПР) - произведение концентрации ионов (ПКИ) в насыщенном растворе труднорастворимого эликтролита, является величиной постоянной при постоянной температуре. Величина ПР зависит от природы электролита, растворителя и температуры.
ПРAgCl=[Ag+][Cl-]


 CaCl2 [Ca22+][Cl-]2
CaCl2 [Ca22+][Cl-]2
АВ= аА + вВ
ПР = [А]а [В]в
Растворенный карбонат кальция (CaCO3)=6,15*10-3г/л. Найти ПР CaCO3 -?
 CaCO3 [Ca2+][ CO32-]
CaCO3 [Ca2+][ CO32-]
Выразим растворимость в молях
CaCO3= 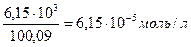
Так как каждая молекула карбоната кальция, дает по одному иону, то [Ca2+] = [ CO32-] = 6,15 моль.
Условия осаждения:
1) выбор растворителя - при реакции с определенным компонентом необходимо, чтоб получалась нужная осаждаемая форма.
Осадитель должен быть специфическим, удобно, чтобы осадитель был летучим веществом;
2) количество осадителя - наибольшее полное осаждение происходит тогда, когда в растворе количество определенного соединения не превышает на 0,0002 г.
Для этого применяют избыток осадителя (в 1,5-2 раза больше, чем в вычисленном по уравнению реакции).
3) влияние температуры - ПР увеличивается с помощью температуры, с другой стороны, повышение температуры способствует росту кристаллов осадка или коагуляции коллоидных частиц, поэтому осаждение ведут из горячего раствора.
Важнейшие операции гравиметрического анализа:
- Подготовка тиглей: проводят в то время, когда проводят осаждение, фильтрование или промывание осадка. Температура прокаливания тигля должна соответствовать температуре прокаливания осадка по методике, время прокаливания в печи =30-40 минут
 эксикатор на 30-40 минут, для остывания
эксикатор на 30-40 минут, для остывания  взвешивание на аналитических весах до 4 знака после запятой
взвешивание на аналитических весах до 4 знака после запятой  в муфельную печь на 15-20 минут.
в муфельную печь на 15-20 минут.


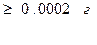
2. Осаждение - проводится в химическом стакане. Осадитель переливают маленькими порциями по внутренней стенке стакана. Обязательно непрерывно перемешивать раствор стеклянной палочкой, не задевая дно и стенки стакана.
Осадки бывают двух видов: кристаллические и амфотерные.
Условия для получения кристаллического осадка:
1) осаждение проводит из сильно разбавленных растворов;
2) прибавлять осадитель медленно, в начале осаждения по каплям;
3) осаждение проводят из горячих растворов;
4) для образования более крупных кристаллов осадка следует выдержать осадок некоторое время, в маточном растворе на холоду происходит «старение» или «созревание осадка».
Условия для получения амфотерных осадков:
1) Осаждение проводится из малоразбавленных растворов, концентрация раствором осадителя (образуются более плотные осадки)
2) Осадитель прибавляют более быстро, чем при осаждения осадка
3) Перед осаждением в раствор вводят электролит, который вызывает коагуляцию раствора.
4) Осаждение ведут из горячего раствора и немедленно начинают фильтровать.
3. Фильтрование и промывание осадка. Условия:
ü осадок должен занимать 1/3 фильтра
ü края фильтра должны быть ниже на 0,5-1 см
ü беззольные фильтры (масса золы 0,0001г). Наименьшая плотность - это с черной и красной лентой, средняя плотность - белая лента, самая плотная – голубая.
ü высушивание и прокаливание осадка (нельзя допускать воспламенения фильтра!!!)
ü взятие навески, берут на аналитических весах.
Определение массы навески:
если осаждается в виде кристаллического осадка, то навеска не должна превышать 0,5г, а если в виде студенистого осадка - 0,1 г.
mтигля=1
mфильтра=2 m 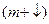 =3
=3
m 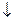 =
= 
F - фактор расчёта.
Fе2O3 содержит х= Fе
В 1 моле Fе2O3 содержит 159,7 содержат Fе3+
(2Mr(Fе))=111.7г Fе3+
159,7 - 11,7 хг Fе2O3
1г - х Fе= 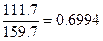
P = m*F
P - масса определяемого вещества
m - масса осадка в граммах
F - фактор пересчета.
 Если результат параллельных определений превышает величину 0,002 - 0,0004, то анализ переделывают, если укладывается в этот интервал, то берут среднее значимое
Если результат параллельных определений превышает величину 0,002 - 0,0004, то анализ переделывают, если укладывается в этот интервал, то берут среднее значимое
m=1,7937г
m=1,7939г средняя m (m1+ m2+m3): 3
m =1,7935г - промах
m=1,7939г
Х= 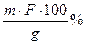 g - навеска анализируемого образца
g - навеска анализируемого образца
Дата публикования: 2015-09-17; Прочитано: 4452 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
