 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Последовательность электродных процессов
|
|
Выделение тех или иных продуктов на электродах происходит в результате окислительно-восстановительных процессов, которые в электрохимии называются процессами разряда или просто разрядом. Значение потенциала электрода, при котором происходит разряд называется потенциалом (напряжением) разложения. Из нескольких возможных процессов в первую очередь будет протекать тот, осуществление которого сопряжено с меньшей затратой энергии.
На катоде в первую очередь будут восстанавливаться те системы, потенциал разложения которых менее отрицателен (или более положителен). В случае водных растворов электролитов в электродных процессах принимает участие вода, причём, характер процесса зависит от реакции среды (табл. 5.2).
Как следует из табл. 5.2 в первом приближении, если идёт электролиз воды, то на катоде выделяется водород, а на аноде ─ кислород.
Таблица 5.2
Процессы разряда воды при электролизе
| Процесс | Реакция среды | |
| кислая | нейтральная | щелочная |
| Катодный | 2Н+ + 2ē → Н2 | 2Н2О + 2ē → Н2 + 2 ОН¯ |
| Анодный | 2Н2О → О2 + 4Н+ + 4ē | 4ОН¯→ О2 + 2Н2О + 4ē |
При электролизе водных растворов солей на катоде помимо воды и ионов водорода могут разряжаться катионы металлов расположенных после титана в ряду активности, причём электролиз солей Zn, Cr, Fe, Cd, Ni cопровождается совместным выделением металла и водорода. Приближённо выделение водорода можно не учитывать (рис. 5.8).

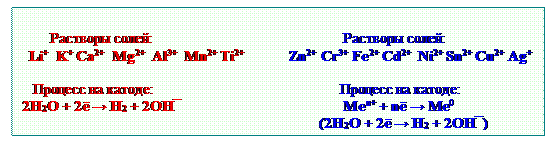
Рис. 5.8 ─ Последовательность катодных процессов при электролизе
На аноде в первую очередь будут окисляться системы с менее положительным напряжением разложения. Анодныйпроцесс в первую очередь определяется материалом анода. Очень часто в качестве анода используют Zn, Cr, Fe, Cd, Ni, Cu, Ag, это растворимые аноды, т.е. идёт окисление анода по схеме: Ме 0 ─ n ē → Ме n+ . Применяются также нерастворимые (инертные) аноды: угольные, графитовые, платиновые. На таких анодах могут разряжаться простые анионы в следующей последовательности: S2‾, J‾ Br‾, Cl‾. Кислородсодержащие ионы, например: NO3‾, SO4‾, а также F‾ в водных растворах не разряжаются, вместо них окисляется Н2О или ОН ¯ (табл. 5.2, табл. 5.3).
Таблица 5.3
Последовательность анодных процессов при электролизе
Дата публикования: 2015-07-22; Прочитано: 1640 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
