 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Поверхностное натяжение и поверхностная энергия
|
|
Поверхностные явления
(на границе газ - жидкость, жидкость- жидкость, жидкость – твердое тело)
План лекции
Поверхностное натяжение и поверхностная энергия
2. Факторы, влияющие на величину поверхностного натяжения.
3. Смачивание. Краевой угол смачивания.
4. Классификация поверхностных явлений
5. Процессы, приводящие уменьшению границы раздела фаз: приобретение каплями сферической формы, коагуляция, коалесценция.
6. Процессы, сопровождающиеся снижением поверхностного натяжения: адсорбция, адгезия, смачивание.
7. Адсорбция. Уравнения Фрейндлиха, Ленгмюра, Гиббса.
Поверхностное натяжение и поверхностная энергия
К поверхностным явлениям относят эффекты и особенности поведения веществ, которые наблюдаются на поверхностях раздела фаз. Причина поверхностных явлений – особое состояние молекул в слоях жидкостей и твердых тел, непосредственно прилегающих к поверхностям раздела. Эти слои резко отличаются по многим физико-химическим характеристикам (удельной энергии, плотности, вязкости, электрической проводимости и др.) от свойств фаз в глубине их объема (рис.1.)
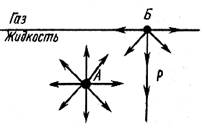
Рис.1. Состояние молекул во внутреннем и поверхностном
слоях жидкости
Поверхность жидкости, соприкасающаяся с другой средой, например, с собственным паром, находится в особых условиях по сравнению с остальной массой жидкости. Эти особые условия возникают потому, что молекулы поверхностного слоя в отличие от молекул в ее глубине, подвергаются неодинаковому притяжению молекул жидкости и газа. Каждая молекула внутри жидкости со всех сторон притягиваются соседними молекулами, расположенными на расстоянии радиуса сферы действия межмолекулярных сил (рис.1) В результате силы притяжения компенсируются, поэтому равнодействующая этих сил равна нулю.
Т.о. поверхностные молекулы жидкости всегда находятся под действием силы, стремящейся втянуть их внутрь. Это приводит к тому, что поверхность жидкости всегда стремится сократиться. Этим объясняется и шарообразная форма капли жидкости (шар имеет минимальную поверхность) и идеальная гладкая поверхность жидкости в широком сосуде.
При увеличении поверхности, например при сжатии капли или растяжении жидкой пленки, некоторое число молекул из глубины жидкости переходит на поверхность. Этот процесс переноса молекул из равновесного состояния в особое состояние молекул поверхностного слоя требует затраты внешней работы. Работа увеличения площади поверхности жидкости переходит в потенциальную энергию молекул поверхностного слоя – поверхностную энергию. Поверхностная энергия, отнесенная к единице поверхности, получила название поверхностного натяжения.
σ = F / S,
где σ – поверхностное натяжение,
F – поверхностная энергия
S – площадь поверхности
В единицах СИ поверхностное натяжение выражается В Дж./м2 или Н/м. Поверхностное натяжение для различных жидкостей неодинаково, особенно велико поверхностное натяжение у воды (7.3 . 10-2 Н/м).
Поверхностная энергия, а следовательно, и поверхностное натяжение зависят от
§ температуры,
§ природы граничащих фаз,
§ природы и концентрации растворенных веществ.
 1. Влияние температуры на поверхностное натяжение: С повышением температуры значение σ индивидуальных жидкостей на границе с воздухом линейно уменьшается. Температурный коэффициент поверхностного натяжения имеет отрицательный знак и постоянную величину.
1. Влияние температуры на поверхностное натяжение: С повышением температуры значение σ индивидуальных жидкостей на границе с воздухом линейно уменьшается. Температурный коэффициент поверхностного натяжения имеет отрицательный знак и постоянную величину.
где σ1 и σ2 – поверхностное натяжение при температурах Т1 и Т2,
α = 0,1 мН/(м × К) температурный коэффициент поверхностного натяжения
2. Правило Ребиндера определяет влияние природы граничащих фаз : Чем больше разность полярностей (ΔП) фаз, тем сильнее поверхностное натяжение на границе их раздела
 |
где e - диэлектрическая проницаемость.
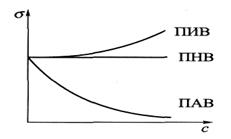
8. Вещества, растворение которых вызывает повышение поверхностного натяжения жидкостей, называют поверхностно-инактивными веществами (ПИВ: NaCl, СаСl2, Na2SO4). Вещества, при растворении которых понижается поверхностное натяжение на границе раздела фаз, называют поверхностно-активными веществами (ПАВ).
|

|
Рис. 2. Изотерма поверхностного натяжения. Строение молекулы ПАВ.
Дата публикования: 2015-07-22; Прочитано: 5051 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
