 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Пример 3. находящейся в водном растворе, смещение равновесия в сторону прямой реакции произойдёт при:
|
|
В системе:
С2Н5СООН + СН3ОН 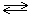 С2Н5СООСН3 + Н2О,
С2Н5СООСН3 + Н2О,
находящейся в водном растворе, смещение равновесия в сторону прямой реакции произойдёт при:
1) добавлении катализатора,
2) разбавлении реакционной смеси,
3) повышении давления,
4) отгонке сложного эфира.
Решение.
Введение катализатора в равновесную системуне влияет на смещение химического равновесия.
Так как и прямая, и обратная реакции являются бимолекулярными и имеют сходные кинетические уравнения для скоростей реакций, то изменение концентраций при разбавлении снизят скорости этих реакций в одинаковой степени, что не приведет к смещению равновесия.
Изменение давления влияет на скорости реакций, протекающих в газовой фазе. В нашем примере реакции протекают в водном растворе (жидкой фазе). Поэтому повышение давления в нашем примере не приведет к смещению равновесия.
При отгонке сложного эфира происходит уменьшение концентрации последнего в равновесной системе в соответствии с принципом Ле Шателье. В системе преимущество получают процессы, приводящие к ослаблению оказанного воздействия. Равновесие смещается вправо, т.е. в сторону образования сложного эфира.
Дата публикования: 2015-07-22; Прочитано: 498 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
