 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Квантування орбітального моменту імпульсу електрона
|
|
141. Яким виразом визначаються дозволені значення орбітального моменту імпульсу електрона L у атомі?

142. Укажіть символіку електронної оболонки, у якій максимальна кількість електронів не може бути більшою 10.
А) S. Б) p. В) d. Г) f. Д) g.
143. Визначте орбітальний момент імпульсу електрона L, який знаходиться у S -електронній оболонці
А) 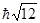 . Б)
. Б) 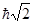 . В)
. В) 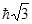 . Г)
. Г) 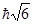 . Д) 0.
. Д) 0.
144. Визначте орбітальний момент імпульсу електрона L, який знаходиться у р -електронній оболонці
А) 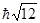 . Б)
. Б) 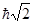 . В)
. В) 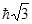 . Г)
. Г) 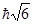 . Д)
. Д) 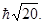
145. Модуль орбітального моменту імпульсу L одноелектронного атома у d -стані дорівнює:
А) 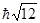 . Б)
. Б) 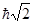 . В)
. В) 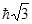 . Г)
. Г) 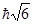 . Д)
. Д) 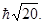
146. Модуль орбітального моменту імпульсу L одноелектронного атома у f -стані дорівнює:
А) 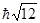 . Б)
. Б) 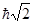 . В)
. В) 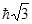 . Г)
. Г) 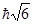 . Д)
. Д) 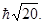
147. Визначте орбітальний момент імпульсу електрона L, який знаходиться у g -електронній оболонці
А) 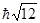 . Б)
. Б) 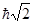 . В)
. В) 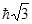 . Г)
. Г) 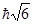 . Д)
. Д) 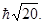
148. Укажіть найбільшу кількість електронів у d -оболонці при заданому значенні n.
А) Десять. Б) Чотирнадцять. В) Шість. Г) Вісім. Д) Вісімнадцять.
149. Укажіть найбільшу кількість електронів у f -оболонці при заданому значенні n.
А) Десять. Б) Чотирнадцять. В) Шість. Г) Вісім. Д) Вісімнадцять.
150. У зовнішній електронній оболонці незбудженого атома знаходиться один електрон з орбітальним моментом імпульсу L =0 і головним квантовим числом n =3. Що це за атом?
А) K (z=19). Б) Li (z=3). В) Mg (z=12). Г) Na (z=11). Д) Si (z=14).
151. Укажіть максимальну кількість електронів, що можуть знаходитись у 4р -оболонці.
А) Два. Б) Чотири. В) Шість. Г) Вісім. Д) Десять.
152. У якому із незбуджених атомів у 3р- оболонці знаходиться один електрон?
А) Mg (z=12). Б) Na (z=11). В) Nе (z=10). Г) P (z=15). Д) Al (z=13).
153. Скільки вільних квантових станів мають місце у d -оболонці, яка заповнена трьома електронами?
А) Сім. Б) П’ять. В) Вісім. Г) Чотири. Д) Шість.
154. Скільки різних орієнтацій у зовнішньому магнітному полі може набувати орбітальний момент електрона Lz у 5S -електронному стані?
А) Дві. Б) Одну. В) Чотири. Г) Три. Д) П¢ять.
155. Скільки різних орієнтацій у зовнішньому магнітному полі може набувати орбітальний момент електрона Lz у 2р -електронному стані?
А) Одну. Б) Дві. В) Три. Г) Чотири. Д) П¢ять.
156. Скільки різних орієнтацій у зовнішньому магнітному полі може набувати орбітальний момент електрона Lz у 3d -електронному стані?
А) Одну. Б) Дві. В) Три. Г) Чотири. Д) П¢ять.
157. Скільки різних орієнтацій у зовнішньому магнітному полі може набувати орбітальний момент електрона Lz у 4f -електронному стані?
А) Чотири. Б) Cім. В) П¢ять. Г) Шість. Д) Три.
158. Укажіть значення орбітального квантового числа l для електронної оболонки, у якій може знаходитись не більше, ніж 10 електронів.
А) l =2. Б) l =4. В) l =6. Г) l =3. Д) l =5.
159. Укажіть значення орбітального квантового числа l для електронної оболонки, у якій може знаходитись не більше, ніж 14 електронів.
А) l =2. Б) l =4. В) l =6. Г) l =3. Д) l =5.
160. Який кут j із напрямком зовнішнього магнітного поля складає момент імпульсу електрона L у атомі водню, якщо орбітальне квантове число l =2, а магнітне квантове число m =1?
А) j=600. Б) j=450. В) j=660. Г) j=540. Д) j=720.
161. Який кут j із напрямком зовнішнього магнітного поля складає момент імпульсу електрона L у атомі водню, якщо орбітальне квантове число l =3, а магнітне квантове число m =2?
А) j=350. Б) j=450. В) j=650. Г) j=550. Д) j=750.
162. Який кут j із напрямком зовнішнього магнітного поля складає момент імпульсу електрона L у атомі водню, якщо орбітальне квантове число l =3, а магнітне квантове число m =1?
А) j=390. Б) j=480. В) j=640. Г) j=560. Д) j=730.
163. Визначте максимальне значення орбітального квантового числа l для електрона у збудженому стані атому водню, якщо енергія збудження DE дорівнює 12,09 еВ.
А) l= 2. Б) l= 3. В) l= 4. Г) l= 5. Д) l= 6.
Дата публикования: 2014-11-18; Прочитано: 1094 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
