 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Вязкость растворов полимеров
|
|
По вязкости растворы высокомолекулярных соединений резко отличаются от растворов низкомолекулярных веществ и золей. При одной и той же весовой концентрации вязкость растворов полимеров значительно больше вязкости растворов низкомолекулярных веществ и лиофобных золей (рис. 77), и с увеличением концентрации она резко возрастает.
Такая высокая вязкость растворов полимеров объясняется наличием в системе макромолекул, которые увеличивают силу трения при передвижении одного слоя жидкости относительно другого. Причем с уменьшение гибкости макромолекул, с возрастанием их размеров и концентрации в растворе увеличение силы трения становится все более существенным.
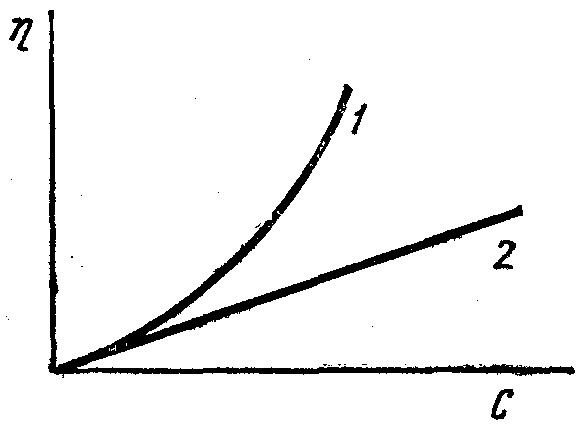
Рис. 77. Зависимость вязкости от концентрации:
1 – раствора полимера; 2 – золя
Увеличение вязкости жидкости, связанное с присутствием в ней макромолекул полимера, принято характеризовать удельной вязкостью:
hуд. = 
где η р – вязкость раствора;
η0 – вязкость чистого растворителя.
 Герман Штаудингер (1881 – 1965) получил образование в Галле (по ботанике) и Дармштадте и Мюнхене (по химии). С 1903 г. был ассистентом в Галле и Страсбурге, а с 1907 г. – профессор в Карлсруэ, где вел работы по органической химии. В 1912 г. он переехал в Цюрих, а в 1926 г. стал руководителем химической лаборатории в Фрейбурге, где в 1940 г. основал Институт высокомолекулярных соединений. Здесь были выполнены его важнейшие исследования в этой области. Г. Штаудингер основал новое направление – химию высокомолекулярных соединений на стыке органической и коллоидной химии. После 1930 г. эта новая область получила быстрое развитие как в части синтеза многих практически ценных высокополимеров, так и в отношении изучения особенностей их структуры.
Герман Штаудингер (1881 – 1965) получил образование в Галле (по ботанике) и Дармштадте и Мюнхене (по химии). С 1903 г. был ассистентом в Галле и Страсбурге, а с 1907 г. – профессор в Карлсруэ, где вел работы по органической химии. В 1912 г. он переехал в Цюрих, а в 1926 г. стал руководителем химической лаборатории в Фрейбурге, где в 1940 г. основал Институт высокомолекулярных соединений. Здесь были выполнены его важнейшие исследования в этой области. Г. Штаудингер основал новое направление – химию высокомолекулярных соединений на стыке органической и коллоидной химии. После 1930 г. эта новая область получила быстрое развитие как в части синтеза многих практически ценных высокополимеров, так и в отношении изучения особенностей их структуры.
Штаудингером установлена математическая зависимость удельной вязкости раствора полимера от его молярной массы:
ηуд. = KMC
где K – константа, характерная для полимеров данного класса;
С – концентрация полимера в растворе; М – молярная масса полимера.
Уравнение Штаудингера можно использовать в таком виде для разбавленных растворов полимеров, макромолекулы которых линейны, не взаимодействуют друг с другом и имеют небольшую молярную массу (меньше 80000).
При увеличении длины макромолекулы и ее гибкости используется модифицированная форма уравнения Штаудингера:
[η] = KMα
где [η] – характеристическая вязкость раствора, определяемая как lim ηуд./с; α – величина, учитывающая свертывание макромолекул, (т.е. гибкость их цепи). Она определяется опытным путем и принимает значения от 0,5 (когда форма макромолекул близка к сферической (рис. 78)), до 1 (для жестких, вытянутых в виде палочки макромолекул).
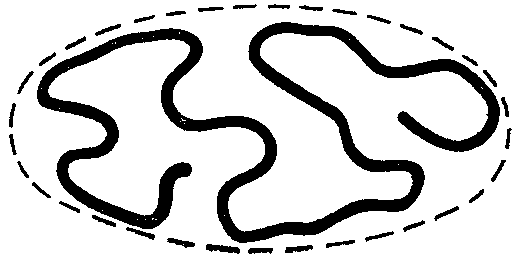
Рис. 78. Схематическое изображение молекулярного клубка в растворе
В растворах с достаточно высокой концентрацией полимера появляются ассоциаты макромолекул, которые, взаимодействуя друг с другом, могут образовывать различные пространственные структуры, затрудняющие течение жидкости. В этом случае вязкость раствора становится аномально высокой и уравнение Штаудингера к нему применять нельзя.
При увеличении скорости течения жидкости пространственные структуры полимеров могут разрушаться. В этом случае вязкость растворов полимеров уменьшается.
Дата публикования: 2014-11-03; Прочитано: 1915 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
