 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Стехиометрические соотношения горения топлива
|
|
Горючие элементы топлива вступают в химическую реакцию с кислородом в определенном соотношении. Расход кислорода (а значит и воздуха) и количество образующихся продуктов сгорания определяются на основании стехиометрических уравнений горения.
Стехиометрическое уравнение горения углерода записывается в виде
С + О2 = СО2 , (6)
т.е. 12 кг С +32 кг О2 = 44 кг СО2;
при пересчете на 1 кг С
1 кг С+ 32/12 кг О2 = 44/12 кг СО2 + 33 705 кДж/кг.
Из этого равенства следует, что для сжигания углерода требуется 32/12=2,67 кг кислорода, при этом выделяется 44/12 = 3,67 кг углекислого газа и 33 705 кДж/кг теплоты.
Для удобства расчета топливно-энергетических балансов и учета запасов энергии в топливах различной теплоценности, а также для сравнения удельных расходов топлива на единицу выработанной энергии используется понятие условного топлива с теплотой сгорания 29,3 МДж/ кг (7000 ккал/ кг). Для пересчета  натурального топлива в
натурального топлива в  условного ее делят на 29,3, конечную величину называют тепловым эквивалентом данного топлива
условного ее делят на 29,3, конечную величину называют тепловым эквивалентом данного топлива
Э = 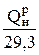 , (7)
, (7)
который используется для пересчета расхода натурального топлива в расход условного топлива
Вусл=ВнатЭ. (8)
Количество расходуемого на сжигание топлива кислорода и образующихся продуктов сгорания приведено в табл. 8.
Дата публикования: 2014-11-04; Прочитано: 1199 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
