 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Гетерогенные электрохимические процессы с участием металлов. Представление о металлической связи
|
|
Рассмотрим процессы, протекающие при погружении металла в раствор собственных ионов. Металлы имеют кристаллическое строение. В узлах решеток расположены ион-атомы, находящиеся в равновесии со свободными электронами:
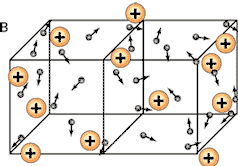 Рис. 9.3.1. Схема кристаллической решетки металла.
Рис. 9.3.1. Схема кристаллической решетки металла.
|
При погружении металла в раствор начинается сложное взаимодействие металла с компонентами раствора. Наиболее важной реакцией является взаимодействие поверхностных ион-атомов металла, находящихся в узлах решетки, с полярными молекулами растворителя (воды), ориентированными у поверхности электрода. В результате указанного процесса происходит окисление металла, и его сольватированные (гидратированные) ионы переходят в раствор, оставляя в металле электроны, заряд которых не скомпенсирован положительно заряженными ионами в металле:
Me + mH2O - ne-↔ Me.(H2O)mn+
Дата публикования: 2015-07-22; Прочитано: 958 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
