 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Свойства растворов
|
|
Пример 1. Вычислите температуры кристаллизации и кипения 2%-ного водного раствора глюкозы.
Решение. По закону Рауля понижение температуры кристаллизации и повышение температуры кипения раствора (ΔТ) по сравнению с температурами кристаллизации и кипения растворителя выражаются уравнением
 , (1)
, (1)
где К – криоскопическая или эбулиоскопическая константа. Для воды они соответственно равны 1,86о и 0,52о;
m и М – соответственно масса растворенного вещества и его молярная масса;
m1 – масса растворителя.
Пример 2. Раствор, содержащий 1,22 г бензойной кислоты С6Н5СООН в 100 г сероуглерода, кипит при 42,529оС. Температура кипения сероуглерода 46,3оС. Вычислите эбулиоскопическую константу сероуглерода.
Решение. Повышение температуры кипения ΔТ = 46,259 – 46,3 = = 0,229о. Молярная масса бензойной кислоты 122 г/моль. По формуле (1) находим эбулиоскопическую константу
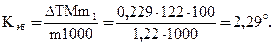
Пример 3. Раствор, содержащий 11,04 г глицерина в 800 г воды, кристаллизуется при – 0,279оС. Вычислите молярную массу глицерина.
Решение. Температура кристаллизации чистой воды 0оС, следовательно, понижение температуры кристаллизации ΔТ = 0 – (–0,279)= = 0,279о. Масса глицерина m (г), приходящаяся на 1000 г воды, равна

Молярную массу глицерина находим по формуле:
 (2)
(2)
 г/моль.
г/моль.
Пример 4. Вычислите массовую долю (%) водного раствора мочевины (NH2)2CO, зная, что температура кристаллизации этого раствора равна – 0,465оС.
Решение. Температура кристаллизации чистой воды 0оС, поэтому
ΔТ = 0 – (– 0,465) = 0,465о. Молярная масса мочевины 60 г/моль. Находим массу m (г) растворенного вещества, приходящуюся на 1000 г воды, по формуле (2)

Общая масса раствора, содержащего 15 г мочевины, составляет
1000 = 15 = 1015 г. Процентное содержание мочевины в данном растворе находим из соотношения
в 1015 г раствора — 15 г вещества
в 100 г раствора — х г вещества
х = 1,48%.
КОНТРОЛЬНЫЕ ВОПРОСЫ
141. Раствор, содержащий 0,512 г неэлектролита в 100 г бензола, кристаллизуется при 5,296°С. Температура кристаллизации бензола 5,50С. Криоскопическая константа 5,1°. Вычислите молярную массу растворенного вещества.
Ответ: 128 г/моль.
142. Вычислите массовую долю (%) водного раствора сахара C12H22O11, зная, что температура кристаллизации раствора - 0,93 °С. Криоскопическая константа воды 1,86.
Ответ: 14,6%.
143. Вычислите температуру кристаллизации раствора мочевины (NН)2CO, содержащего 5 г мочевины в 150 г воды. Криоскопическая константа воды 1,86°.
Ответ: - 1,03°С.
144. Раствор, содержащий 3,04 г камфоры С10Н16О в 100 г бензола, кипит при 80,714°С. Температура кипения бензола 80,2°С. Вычислите эбулиоскопическую константу бензола.
Ответ: 2,57о.
145. Вычислите массовую долю (%) водного раствора глицерина С3Н5(ОН)3, зная, что этот раствор кипит при 100,39°С. Эбулиоскопическая константа воды 0,52°.
Ответ: 6,45%.
146. Вычислите молярную массу неэлектролита, зная, что раствор, содержащий 2,25 г этого вещества в 250 г воды, кристаллизуется при -0,279°С. Крископическая константа воды 1,86о.
Ответ: 60 г/моль.
147. Вычислите температуру кипения 5%-ного раствора нафталина С10Н8 в бензоле. Температура кипения бензола 80,2°С. Эбулиоскопическая константа его 2,57°.
Ответ: 81,25°С.
148. Раствор, содержащий 25,65 г некоторого неэлектролита в 300 г воды, кристаллизуется при -0,465°С. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,86о.
Ответ: 342 г/моль.
149. Вычислите криоскопическую константу уксусной кислоты, зная, что раствор, содержащий 4,25 г антрацена С14 Н10 в 100 г уксусной кислоты, кристаллизуется при 15,718°С. Температура кристаллизации уксусной кислоты 16,65оС.
Ответ: 3,9о.
150. При растворении 4,86 г серы в 60 г бензола температура кипения его повысилась на 0,81°. Сколько атомов содержит молекула серы в этом растворе. Эбулиоскопическая константа бензола 2,57о.
Ответ: 8.
151. Температура кристаллизации раствора, содержащего 66,3 г некоторого неэлектролита в 500 г воды, равна -0,558°С. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,86о.
Ответ: 442 г/моль.
152. Какую массу анилина C6Н5NH2 следует растворить в 50 г этилового эфира, чтобы температура кипения раствора была выше температуры кипения этилового эфира на 0,53о. Эбулиоскопическая константа этилового эфира 2,12о.
Ответ: 1,16 г.
153. Вычислите температуру кристаллизации 2%-ного раствора этилового спирта C2Н5OH. Криоскопическая константа воды 1,86°.
Ответ: -0,82°С.
154. Сколько граммов мочевины следует растворить в 75 г воды, чтобы температура кристаллизации понизилась на 0,465°? Криоскопическая константа воды 1,86о.
Ответ: 1,12 г.
155. Вычислите массовую долю (%) водного раствора глюкозы С6Н12О6, зная, что этот раствор кипит при 100,26оС. Эбулиоскопическая константа воды 0,52о.
Ответ: 8,25%.
156. Сколько граммов фенола следует растворить в 125 г бензола, чтобы температура кристаллизации раствора была ниже температуры кристаллизации бензола на 1,7о? Криоскопическая константа бензола 5,1о.
Ответ: 3,91 г.
157. Сколько граммов мочевины (NH2)2CO следует растворить в 2 г воды, чтобы температура кипения повысилась на 0,26°? Эбулиоскопическая константа воды 0,52о.
Ответ: 7,5 г.
158. При растворении 2,3 г некоторого неэлектролита в 125 г воды температура кристаллизации понижается на 0,372о. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,86°.
Ответ: 92 г/моль.
159. Вычислите температуру кипения 15%-ного водного раствора пропилового спирта С3Н7ОН. Эбулиоскопическая константа воды 0,52°.
Ответ: 101,52°С.
160. Вычислите массовую долю (%) водного раствора метанола СНзОН, температура кристаллизации которого -2,79оС. Криоскопическая константа воды 1,86о.
Ответ: 4,58%.
Дата публикования: 2014-11-18; Прочитано: 3492 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
