 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Основы биотехнологии 1 страница
|
|
Для специальности 1-31 01 01 – Биология рекомендуется учебная программа № ТД-G.005/тип., составленная доктором медицинских наук профессором Ю.К.Фомичевым, доктором биологических наук профессором В.А.Прокулевич и кандидатом биологических наук доцентом Р.А.Желдаковой; для специальности 1-33 01 01 Биоэкология и 1-02 04 04-01 – Биология. Химия используется программа «Основы биотехнологии» д ля студентов биологических факультетов университетов, разработаная заведующим кафедрой химии Витебского государственного университета им. П.М. Машерова доктором биологических наук, профессором Чиркиным А.А.
ЗАДАЧИ ПРЕПОДАВАНИЯ КУРСА
В результате изучения основ биотехнологии студент должен:
знать
- биологические агенты, используемые в биотехнологии;
- принципы культивирования клеток;
- сущность методов молекулярной генетики, а также технологии рекомбинантных ДНК;
- принципы работы с иммобилизованными ферментами;
- этапы выделения целевых продуктов и возможные пути загрязнения внешней среды
уметь
- пользоваться языком молекулярной биотехнологии и справочными руководствами;
- выбрать биологический объект, составить алгоритм биотехнологических работ, обосновать метод наиболее эффективной очистки целевого продукта;
- применить методы спектрофотометрии, тонкослойной и колоночной хроматографии, определения активности и количества ферментов, выделения и очистки целевого продукта.
СОДЕРЖАНИЕ КУРСА
История молекулярной биотехнологии. Молекулярная биотехнология как разделы молекулярной биологии, молекулярной генетики бактерий, энзимологии, с одной стороны, и промышленной микробиологии и химической инженерии, с другой. Цели молекулярной биотехнологии: повышение урожайности сельскохозяйственных культур, создание микроорганизмов, продуцирующих различные химические соединения, создание пород сельскохозяйственных и других животных с улучшенными наследуемыми признаками, переработка отходов, загрязняющих окружающую среду, получение продуктов питания и повышение биологической ценности пищи, получения низкомолекулярных биорегуляторов и биополимеров для применения в фармации и медицине. Возможные негативные эффекты развития молекулярной биотехнологии.
Ферменты в молекулярной биотехнологии. Иммобилизованные ферменты.
I. Биологические системы, используемые в молекулярной биотехнологии: прокариоты, эукариоты; бактерии Escherichia coli, дрожжи Saccharomyces cerevisiae, культуры эукариотических клеток (насекомых, растений, млекопитающих). Ферменты. Требования, предъявляемые к биообъектам. Культивирование, основные компоненты питательных сред. Принципы селекции микроорганизмов. Биотехнологическое сырье, учитывая побочные продукты производства. Источники минерального питания. Комплексные обогатители сред. Среды для культивирования микроорганизмов. Кислород и вода. Пенообразователи и пеногасители. Значение асептики в биотехнологии.
Матричные синтезы: репликация, транскрипция, трансляция. Особенности регуляции транскрипции у бактерий и эукариот. Представления о технологии рекомбинантных ДНК. Оптимизация экспрессии генов, клонированных в прокариотические клетки. Получение рекомбинантных белков с помощью эукариотических систем. Дрожжевые системы экспрессии. Системы экспрессии с использованием культур клеток насекомых (рекомбинантные бакуловирусы). Системы экспрессии для работы с клетками млекопитающих.
II. Биотехнологический процесс культивирования микроорганизмов. Рост и развитие микроорганизмов. Основные показатели процесса ферментации. Оновные факторы среды, определяющие рост и биосинтетическую активность продуцентов. Оценка процесса ферментации. Промышленный синтез белков при участии рекомбинантных микроорганизмов. Этапы роста культуры – латентная, ускорения, логарифмическая, замедления, стационарная, отмирания (преимущественный синтез белков в логарифмической фазе, а низкомолекулярных продуктов – во время стационарной фазы). Типы биореакторов: с механическим перемешиванием, барботажные колонны, эрлифтные.
Инженерная энзимология. Строение ферментов, катализ, выделение ферментов. Источники ферментов (животного происхождения, растительного происхождения). Иммобилизованные ферменты.
Утилизация крахмала и сахаров, повышение эффективности производства фруктозы и этанола. Бродильные производства (алкогольные напитки, пиво, вино, спирт, сидр, уксус). Мультиплазмидные организмы, способные утилизировать несколько соединений. Утилизация целлюлозы через выделение прокариотических и эукариотических целлюлазных генов. Повышение образования силоса с использованием Lactobacillus plantarum. Белок одноклеточных организмов (БОО) – белковые продукты, синтезируемые монокультурой микробных клеток и используемые в качестве пищевых добавок или корма для скота (подкислители, аминокислоты, витамины и пигменты, усилители вкуса, жиры и масла, растительный клей и загустители, подсластители, пищевые кислоты – уксусная, лимонная, молочная).
Пищевые аспекты биотехнологии: получение пищевого белка, молочные продукты (казеины, казеинат натрия, казецит и копреципитаты, концентраты сывороточных и других белков, методы приближения молочных смесей к женскому молоку, брожение лактозы и коагуляция казеина, производство кисломолочных продуктов, сычужное свертывание молока и производство сыра), хлебопродукты, бродильные производства, пищевые добавки, консервированные овощи (продукты из сои, применение ферментов при выработке фруктовых соков).
Границы применения биотехнологии в пищевой промышленности. Перспективы использования продукции биотехнологии: аминокислоты, олигопептиды, ферменты, витамины, терпены и родственные соединения, органические кислоты, полисахариды.
Представление о биогеотехнологии (обогащение полезных ископаемых и удаление мешающих и опасных веществ, увеличение добычи нефти) и о биоконверсии энергии (биофотолиз воды, биогаз, биологические топливные элементы).
Бактерии, стимулирующие рост растений: непосредственно путем поставки фиксированного азота, хелатированного железа, фитогормонов, фосфатов (штаммы Rhizobium, симбиоз с растениями, клубеньки на корнях) и опосредованно через подавление роста фитопатогенных микроорганизмов.
Микробные инсектициды. Токсины, синтезируемые Bacillus thuringiensis, клонирование генов токсинов и возможность их экспрессии. Бакуловирусы как инсектицидные агенты (введение гена нейротоксина, смертельного для насекомых).
Методы иммунодиагностики: ферментный иммуносорбентный анализ (ELISA). Микробиологическое производство лекарственных средств: интерфероны, соматотропин, моноклональные антитела как лекарственные средства, производство антител с помощью E.coli, перспективы лекарств против ВИЧ. Вакцины – субъединичные, аттенуированные, «векторные».
Использование рекомбинантных микроорганизмов для получения низкомолекулярных соединений – витаминов, аминокислот, антибиотиков и др. Микробиологический синтез каучука.
Биодеградация токсичных соединений и утилизация биомассы. Метаболические пути биодеградации ксенобиотиков.
III. Культуры растительных клеток и тканей. Фертильные растения, все клетки которых несут чужеродный(е) ген(ы) (трансгенные растения). Получение трансгенных растений не содержащих маркерных генов. Выведение растений, устойчивых к насекомым-вредителям, вирусам и гербицидам. Получение растений, противостоящих неблагоприятным воздействиям и старению. Изменение свойств растений: окраски цветков, пищевой ценности, вкуса, внешнего вида плодов. Трансгенные растения, способные синтезировать ценные для промышленности и сельского хозяйства белки и химикаты.
Трансгенные животные (молочная железа – «биореактор», наследуемая устойчивость к бактериальным, вирусным инфекциям и паразитарным инвазиям); трансгенные овцы, козы и свиньи (синтез человеческого гемоглобина); трансгенные птицы, рыбы. ПЦР как метод обнаружения трансгена, перспективы и потенциальные опасности.
IV. Контроль применения биотехнологических методов: экспериментов с рекомбинантными ДНК, производства и потребления пищевых продуктов и пищевых добавок, высвобождения генетически модифицированных организмов в окружающую среду. Общее представление о правилах добротного и безопасного производства (GMP – Good Manufacturing Practice), доклинического испытания (GLP – Good Laboratory Practice) и клинического испытания (GCP – Good Clinical Practice) продуктов молекулярной биотехнологии, применяемых для улучшения качества жизни человека.
Количество часов по дисциплине
| Название факультета | Се- местр | Всего часов | Всего ауди- торных часов | Лек- ции | Лабора- торные занятия | КСР | Экза-мен, зачет |
| Биологический ДО, ЗО | Зачет |
Примечание: КСР – контролируемая самостоятельная работа студентов под контролем преподавателя.
ПРИМЕРНЫЙ ТЕМАТИЧЕСКИЙ ПЛАН ЛЕКЦИЙ ДИСЦИПЛИНЫ «ОСНОВЫ БИОТЕХНОЛОГИ» ДЛЯ СТУДЕНТОВ БИОЛОГИЧЕСКИХ СПЕЦИАЛЬНОСТЕЙ»
| № | СОДЕРЖАНИЕ | Часы |
| Введение в молекулярную биотехнологию | ||
| Биологические системы, используемые в молекулярной биотехнологии | ||
| Технология рекомбинантных ДНК, экспрессия генов | ||
| Биотехнологическая энзимология | ||
| Биотехнологические основы культивирования микроорганизмов | ||
| Молекулярная биотехнология микробиологических систем в экологии и диагностике | ||
| Молекулярная биотехнология микробиологических систем и питание | ||
| Бродильное производство | ||
| Продукты питания на основе молока и хлеб | ||
| Молекулярная биотехнология микробиологических систем и производство коммерческих продуктов | ||
| Трансгенные растения | ||
| Трансгенные животные | ||
| Контроль применения биотехнологических методов |
ИТОГО: Лекции 32 часов.
ПРИМЕРНЫЙ ТЕМАТИЧЕСКИЙ ПЛАН ЛАБОРАТОРНЫХ ЗАНЯТИЙ ДИСЦИПЛИНЫ «ВВЕДЕНИЕ В БИОТЕХНОЛОГИЮ»
| № | Наименование раздела, темы, элемента | К-во часов | Примечание |
| Белки. Качественные и количественные методы определения аминокислот и белков. Методы изучения физико-химических свойств белков. | |||
| Ферменты. Определение специфичности ферментов. Иммобилизация ферментов. Методы выделения и количественного определения количества и активности ферментов. Методы изучения кинетических свойств ферментов. | |||
| Биохимическая оценка продуктов питания: физико-химические свойства, содержание витаминов. |
Литература
Основная литература
Егорова Т.А., Клунова С.М., Живухина Е.А. Основы биотехнологии. М.: «Академия», 2003.
Глик Б., Пастернак Дж. Молекулярная биотехнология. Принципы и применение. М.: “Мир”, 2002.
Голубев В.Н., Жиганов И.Н. Пищевая биотехнология. М.:ДеЛи принт, 2001.
Горбатова К.К. Биохимия молока и молочных продуктов. Санкт-Петербург: ГИОРД, 2003.
Евтушенков А.Н., Фомичев Ю.К. Введение в биотехнологию. Минск: БГУ, 2004.
Кислухина О., Кюдулас И. Биотехнологические основы переработки растительного сырья. Каунас: «Технология», 1997.
Кислухина О.В. Ферменты в производстве пищи и кормов. М.: ДеЛи принт, 2002. – 336 с.
Семак И.В. Инженерная энзимология. Минск: БГУ, 2006.
Фомичев Ю.К., Прокулевич В.А., Желдакова Р.А. Основы биотехнологии. Учебная программа для высших учебных заведений по специальности 1-31 01 01 Биология. Минск, 2006.
Чиркин А.А. Практикум по биохимии. Минск: ООО «Новое знание», 2002.
Чиркин А.А. Введение в биотехнологию. Витебск: Издательство УО «ВГУ им. П.М.Машерова», 2004.
Чиркин А.А. Основы генной инженерии: методы рекомбинантных ДНК. Витебск: Издательство УО «ВГУ им. П.М.Машерова», 2005.
Дополнительная литература
Бейли Д., Оллис Д. Основы биохимической инженерии, в 2-х частях. М.: "Мир", 1989.
Бекер М.Е., Лиепиньш Г.К., Райнулис Е.П. Биотехнология. М.: "Агропромиздат", 1990.
Биотехнология, в 8-ми томах. Под ред. Н.С.Егорова, В.Д.Самуилова. М.: "Высшая школа", 1987-1988.
Гриневич А.Г., Босенко А.М. Техническая микробиология. Мн.: "Вышэйшая школа", 1986.
Елинов Н.П. Основы биотехнологии. СПБ: "Наука", 1995.
Варфоломеев С.Д., Калюжный С.В. Биотехнология. Кинетические основы микробиологических процессов. М.: «Высшая школа», 1990.
Виестур У.Э., Шмите И.А., Жилевич А.В. Биотехнология: биотехнологические агенты, технология, аппаратура. Рига: "Зинатне", 1987.
Кулаковская Т.В. Лабораторный практикум по биотехнологии: Учеб. пособие. Мн.: БГПУ им. М.Танка, 2001. – 45 с.
Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. М.:Минздрав РФ, ЗАО «ИИА Ремедиум», 2000.
Рыбчин В.Н. Основы генетической инженерии. СПб: СПбГТУ, 2002.
Юрченко Е.О., Синявская М.Г. Основы молекулярного маркирования грибной ДНК. Минск: ИООО «Право и экономика», 2007.
Harvey W. Blanch, Douglas S. Clark. Biochemical Engineering. N.-Y.:Marcel Dekker, 1997.
Wong C.H., White G.M. Enzymes in Synthetic Organic Chemistry. Trowbridge: Pergamon, 1995.
ТЕОРЕТИЧЕСКОЕ СОДЕРЖАНИЕ КУРСА
История развития молекулярной биотехнологии представлена в таблице 1.
Таблица 1 - Историческая справка о становлении молекулярной биологии (по Б.Глик, Дж.Пастернак, 2002)
| Дата | Событие |
| Карл Эреки ввел термин «биотехнология» на основе промышленного выращивания свиней с использованием сахарной свеклы | |
| Промышленное производство пенициллина | |
| Генетический материал – ДНК (Эвери, МакЛеод, МакКарти) | |
| Двойная спираль ДНК (Уотсон и Крик) | |
| Расшифрован генетический код | |
| Выделена первая рестриктаза (эндонуклеаза) | |
| Синтез полноразмерного гена тРНК (Корана) | |
| Создание технологии рекомбинантных ДНК (Бойер и Коэн) | |
| Описание технологии получения моноклональных антител (Колер, Мильштейн) | |
| Первые руководства для работы с рекомбинантными ДНК | |
| Методы определения нуклеотидной последовательности ДНК | |
| Произведен человеческий инсулин, полученный с помощью E. сoli | |
| Описано применение Ti-плазмиды для трансформации растений | |
| Генноинженерным путем получена высокоопухолевая линия мышей | |
| Создан метод полимеразной цепной реакции (ПЦР) | |
| Начало проекта «Геном человека» | |
| Определение нуклеотидной последовательности всех хромосом эукариотического микроорганизма (Saccharomyces cerevisiae) | |
| Клонировано млекопитающее из дифференцированной соматической клетки | |
| Завершение проекта «Геном человека» |
Термин «биотехнология» был предложен в 1917 году венгерским инженером Карлом Эреки для описания процесса крупномасштабного выращивания свиней с использованием в качестве корма сахарной свеклы. По определению Эреки, биотехнология – это «все виды работ, при которых из сырьевых материалов с помощью живых организмов производятся те или иные продукты». В 1961 году по инициативе шведского микробиолога Карла Герена Хеден было предложено название журналу «Биотехнология и биоинженерия», что определило официальное признание термина – биотехнология, т.е. наука в области «промышленного производства товаров и услуг при участии живых организмов, биологических систем и процессов». Фундаментом для этой науки явились микробиология, биохимия и химическая инженерия.
Промышленная биотехнология. Промышленный биотехнологический процесс, в котором для производства коммерческих продуктов используются микроорганизмы, обычно состоит из трех ключевых этапов.
1. Исходная обработка: обработка сырья таким образом, чтобы его можно было использовать как источник питательных веществ для микроорганизма-мишени.
2. Ферментация и биотрансформация: рост микроорганизма-мишени в большом (обычно более 100 л) биореакторе (ферментация) с последующим образованием нужного метаболита, например антибиотика, аминокислоты или белка (биотрансформация).
3. Конечная обработка: очистка нужного вещества от компонентов культуральной среды или от клеточной массы.
По Т.А.Егоровой и соавт. (2003) достижения биотехнологии перспективны в следующих отраслях:
1) в промышленности (пищевая, фармацевтическая, химическая, нефтегазовая) – использование биосинтеза и биотрансформации новых веществ на основе сконструированных методами генной инженерии штаммов бактерий и дрожжей с заданными свойствами на основе микробиологического синтеза;
2) в экологии – повышение эффективности экологизированной защиты растений, разработка экологически безопасных технологий очистки сточных вод, утилизация отходов агропромышленного комплекса, конструирование экосистем;
3) в энергетике – применение новых источников биоэнергии, полученных на основе микробиологического синтеза и моделированных фотосинтетических процессов, биоконверсия биомассы в биогаз;
4) в сельском хозяйстве – разработка в области растениеводства трансгенных агрокультур, биологических средств защиты растений, бактериальных удобрений, микробиологических методов рекультивации почв; в области животноводства – создание эффективных кормовых препаратов из растительной, микробной биомассы и отходов сельского хозяйства, репродукция животных на основе эмбриогенетических методов;
5) в медицине – разработка медицинских биопрепаратов, моноклональных антител, диагностикумов, вакцин, развитие иммунобиотехнологии в направлении повышения чувствительности и специфичности иммуноанализа заболеваний инфекционной и неинфекционной природы.
В качестве примера на рис. 1 представлены современные направления биотехнологии, предназначенные для создания продовольствия.
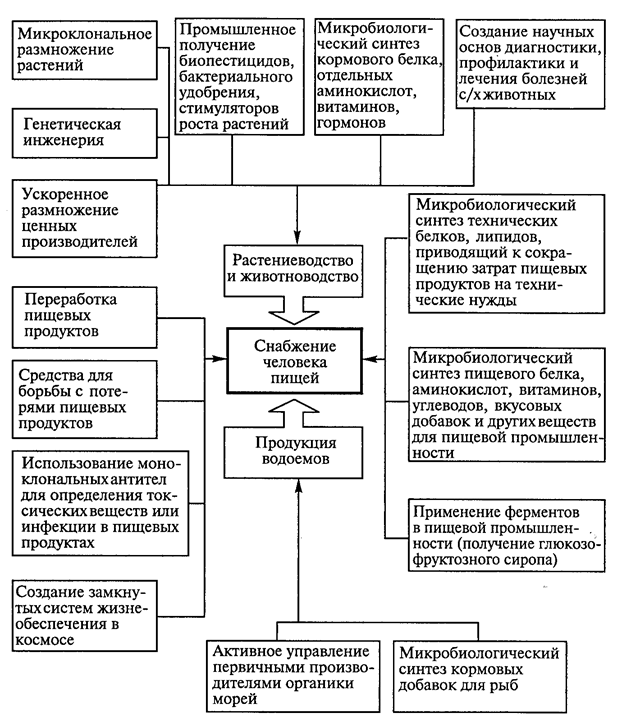
Рис. 1. Перспективные направления биотехнологии в снабжении человечества продовольствием (Т.А.Егорова и соавт., 2003).
Будущее биотехнологии некоторые исследователи связывают с протоинженерией – технологией изменения свойств природных белков на генетическом уровне, получения новых белков (инсектицидов, биостимуляторов, биосенсоров, качественных продуктов питания, лекарств и др.). Так, например, использование биосенсоров лежит в основе биоэлектроники, призванной обеспечивать революционные изменения в методах измерений и контроля в различных областях науки и техники. Основная доля успехов биотехнологии в последние годы связана с развитием методов генной инженерии – технологии рекомбинантных ДНК. Согласно определению Национальных институтов здоровья США, рекомбинантными ДНК называют молекулы ДНК, полученные вне живой клетки, в пробирке, путем соединения природных или синтетических фрагментов ДНК с векторами, способными самореплицироваться в клетке.
Современные методы биотехнологических процессов: методы промышленной микробиологии, генная инженерия, использование иммобилизованных ферментов, клеточных органелл, клеток, тканей растений, насекомых и животных.
Промышленная микробиология базируется на фундаментальных науках микробиология, иммунология и биохимия. В течение последнего столетия промышленная микробиология постепенно занимала передовые позиции в получении пищевых добавок и чистых биологически значимых веществ по сравнению с производствами, основанными на химическом синтезе. Существенным прорывом в развитии промышленной микробиологии явился синтез пенициллина и других антибиотиков. На одной из последних технологических схем синтеза пенициллина представлены типичные этапы биотехнологического процесса синтеза и выделения антибиотика (рис. 2). В промышленной микробиологии важную роль играют знания по энзимологии и генетике микроорганизмов, а также сведения по таксономии микроорганизмов.
Основу генной инженерии составляет встраивание природной или чужеродной ДНК в вектор, который представляет собой бактериальную плазмиду или геном вируса; затем рекомбинантную молекулу ДНК вводят в клетку, где она реплицируется. Клетка, содержащая такую ДНК, размножается, образуя клон трансформированных клеток, способных к экспрессии чужеродных генов и образованию специфических белков в больших количествах.
Технология иммобилизованных ферментов получила свое развитие в последние 30-40 лет. Иммобилизованные ферменты на гелевых или пористых носителях оказались высокотехнологичными при промышленном ферментативном выделении или синтезе различных химических веществ, включая пищевые продукты (получение концентрата фруктозы из крахмала, этанола и др.).
В молекулярной биотехнологии определенное место занимает использование клеток животных, например, для культивирования вирусов при производстве вакцин, интерферона, при синтезе моноклональных антител клетками гибридом, получении сложных белков.

Рис. 2. Технологическая схема производства пенициллина (Т.А.Егорова и соавт., 2003).
Для широкомасштабного производства клонов растений используют меристемы. Культуры растительных клеток применяют для синтеза различных веществ, чаще всего алкалоидов и других вторичных метаболитов. Начиная с 1970 г. исследователи нередко наблюдали, что клетки, растущие в культуре, синтезируют вещества, которые не обнаруживаются в целом растении.
Весьма перспективным является использование тканей и органов животных, насекомых и растений как биореакторов. Наибольший интерес представляет использование молочных желез крупного рогатого скота с целью получения обогащенного специальными добавками молока или лишенного лактозы молока для лиц с дефицитом кишечной лактазы.
Понятие о метаболизме, метаболических путях, карте метаболизма. Совокупность химических превращений веществ в организме называют метаболизмом. Подавляющее большинство химических реакций в живых клетках катализируется ферментами. Вещества, участвующие в метаболизме, называются метаболитами. Метаболизм выполняет 4 функции: 1) Снабжение организма химической энергией, полученной при расщеплении богатых энергией пищевых веществ или путем преобразования энергии солнца. 2) Превращение пищевых веществ в строительные блоки, которые используются в клетке для биосинтеза макромолекул. 3) Сборка макромолекулярных (биополимеры) и надмолекулярных структур живого организма, пластическое и энергетическое поддержание его структуры. 4) Синтез и разрушение тех биомолекул, которые необходимы для выполнения специфических функций клетки и организма.
По форме усвояемого углерода все живые организмы делятся на 2 группы: 1) Автотрофные клетки ("сами себя питающие") усваивают СО2 воздуха в процессе фотосинтеза, и из него строят все свои углеродсодержащие биомолекулы (фотосинтезирующие бактерии, зеленые растения). 2) Гетеротрофные клетки ("питающиеся за счет других") получают углерод из сложных органических молекул, например, глюкозы (клетки высших животных и большинства микроорганизмов), т.е. они питаются продуктами жизнедеятельности других клеток. В биосфере автотрофы и гетеротрофы являются участниками кругооборота углерода и кислорода между животным и растительным мирами (рис. 3). По отношению к кислороду гетеротрофов делят: 1) Аэробы - требуют наличия кислорода для окисления питательных веществ. 2) Анаэробы - для окисления питательных веществ кислород не требуется. 3) Факультативные анаэробы - существуют в кислородной и бескислородной средах; 4) Облигатные анаэробы - живут только в бескислородной среде. Большинство гетеротрофов - факультативные анаэробы, которые при наличии кислорода используют аэробные метаболические пути.

Рис. 3. Катаболизм и анаболизм у автотрофных и гетеротрофных организмов (Голубев В.Н., Жиганов И.Н., 2001).
Метаболические пути. В живой клетке многие тысячи метаболитов вступают в химические реакции. Реакционная способность метаболитов зависит от ряда условий и прежде всего, наличия соответствующих ферментов. Так, например, в мышечных клетках вся глюкоза реагирует только с АТФ и превращается в глюкозо-6-фосфат. Другие реакции не идут, т.к. нет ферментов, а некатализируемые реакции крайне медленны. Образовавшийся глюкозо-6-фосфат является заряженным веществом и поэтому не может покинуть клетку. Дальнейшие превращения глюкозо-6-фосфата определяются набором ферментов, катализирующих последовательные реакции. Т.о. получается ферментативная цепь реакций. Это и есть метаболический путь. Метаболические пути всех веществ связаны друг с другом общими метаболитами и образуют единую сетку реакций - карту метаболизма.
Ферменты и метаболизм. Понятие о регуляции метаболизма. Метаболизм регулируется за счет ферментов. Регуляция активности и количества ферментов лежит в основе метаболических процессов в норме и при патологии. Еще в прошлом веке Клодом Бернаром было установлено, что внутриклеточные константы сохраняются, невзирая на изменение окружающей среды. Это концепция гомеостаза в своей основе содержит координированную деятельность многих ферментативных реакций. Для идеализированной клетки используют камерную модель метаболизма. Исследователь судит о метаболизме, изучая входные и выходные параметры. Изучение самих метаболических путей затруднено. Здесь необходимы специальные приемы, например, изотопная техника. Регуляция метаболических путей осуществляется по Ленинджеру на трех уровнях: 1) Быстрое реагирование, связанное с действием аллостерических ферментов, каталитическая активность которых может меняться под влиянием особых веществ, оказывающих стимулирующее или тормозящее действие (эффекторы, модуляторы). 2) У высших организмов - гормональная регуляция, точнее - нейрогормональная регуляция. Это регуляция посредством дистантных гуморальных сигналов, действующих через мембраны, химическую модификацию или геном клетки. 3) Регуляция метаболизма (долговременная) связана с изменением концентрации данного фермента в клетке. Концентрация всякого фермента в любой данный момент определяется соотношением скоростей его синтеза и распада (индукция синтеза, например, диетой).
Катаболизм и анаболизм. Основные конечные продукты метаболизма. В наиболее употребительном значении термин "метаболизм" равнозначен "обмену веществ". В точном смысле "метаболизм" означает промежуточный обмен, т.е. превращение веществ внутри клеток с момента их поступления до образования конечных продуктов. Метаболизм складывается из двух фаз - катаболизма и анаболизма.
Катаболизм - это ферментативное расщепление крупных пищевых или депонированных молекул до более мелких с выделением энергии и запасанием ее в виде макроэргических соединений. Катаболизм идет в 3 стадии. Первая стадия - полимеры превращаются в мономеры (крахмал и гликоген - в глюкозу, белки - в аминокислоты, триацилглицерины - в жирные кислоты и др.). Вторая стадия (специфические пути катаболизма) - мономеры превращаются в общие продукты, чаще всего, ацетил-КоА. Третья стадия (общий путь катаболизма) - окисление ацетильной группы ацетил-КоА до СО2 и Н2О в реакциях цикла трикарбоновых кислот. Окислительные реакции общего пути катаболизма (ЦТК) сопряжены с цепями переноса электронов (рис. 4). При этом энергия (~ 40%) запасается в макроэргических связях АТФ.
Анаболизм - ферментативный синтез крупных полимерных молекул из простых предшественников с затратой энергии. Идет в 3 стадии, причем третья стадия катаболизма является первой стадией анаболизма.

Рис. 4. Схема катаболизма.
Анаболизм и катаболизм не являются простым обращением реакций. Анаболические пути должны отличаться от путей катаболизма хотя бы одной из ферментативных реакций, чтобы регулироваться независимо. Например, специфический путь распада глюкозы до лактата (гликолиз) включает 11 реакций; синтез глюкозы из лактата включает 8 обратимых реакций распада глюкозы и 3 дополнительных реакции с новым набором ферментов. Именно на этих стадиях за счет регуляции активности ферментов регулируются суммарные скорости распада и синтеза глюкозы. Кроме того реакции катаболизма и анаболизма часто разделены мембранами и протекают в разных отсеках (компартментах) клеток. Например, распад жирных кислот идет в митохондриях, а их синтез в цитозоле. Конечные продукты метаболизма: Н2О, СО2, NН3.
Дата публикования: 2014-11-18; Прочитано: 3701 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
