 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Окисление тиоэфиров. 3 страница. Поскольку белки плазмы крови не подлежат фильтрации, через почки выделяются лишь вещества, не связанные с белками
|
|
Поскольку белки плазмы крови не подлежат фильтрации, через почки выделяются лишь вещества, не связанные с белками. Поскольку свободная и связанная фракция ксенобиотика в крови находится в состоянии динамического равновесия, как только свободная часть отфильтровывается, связанная освобождается из связи с белками. Если связь прочная и высвобождение веществ затруднено процесс выделения вещества растягивается во времени.
Некоторые вещества практически полностью отфильтровываются в клубочках почек в течение нескольких часов. Так как в течение минуты фильтрации подвергается около 130 мл плазмы, скорость почечной элиминации веществ, выделяющихся исключительно посредством фильтрации можно рассчитать по формуле:
t1/2 = ln2 (VD/FR)
t1/2 - период полувыведения;
FR - скорость фильтрации (130 мл/мин);
VD - объем распределения.
При различных объемах распределения период выведения фильтрующихся веществ будет существенно различен:
| VD (л) | ||||
| t1/2 (мин) |
Если объем распределения вещества известен, то на основе величины периода полувыведения можно также судить, быстрее или медленнее элиминируется вещество, чем можно было бы ожидать, исходя из расчета скорости фильтрации плазмы. Если отличия существенны, следует думать о дополнительных механизмах выведения вещества через почки.
2.2. Канальцевая реабсорбция
Гломерулярный фильтрат с растворенными в нем ксенобиотиками переходит из боуменовой капсулы по извитым канальцам, петле Генле, дистальному отделу канальцев в собирательные трубки. Длина каждого из 2 млн канальцев равна 3 - 5 см. Общая площадь поверхности канальцев равна примерно 7 - 8 м2 (таблица 2).
Таблица 2. Площади поверхности различных отделов нефрона.
| Часть нефрона | Площадь (м2) |
| Гломерулы Канальцы 1 порядка (основной отдел) Петля Генле (тонкая часть) (толстая часть) Канальцы 2 порядка (дополнительный отдел) | 0,5 - 1,5 4,25 0,48 1,55 0,98 |
Первичная моча (фильтрат плазмы крови) в значительной части распространяется по этой поверхности в виде тонкой пленки. Благодаря этому удается достичь высокой эффективности процесса диффузии через клеточный слой канальца. По своим свойствам первичная моча ни чем не отличается от сыворотки крови. Она содержит такую же концентрацию ксенобиотика, как и плазма. Следовательно, между жидкостями не существует градиента концентрации веществ. В различных отделах почечных канальцев (и уже в проксимальном их отделе) происходит активная обратная резорбция из первичной мочи отфильтрованной воды, а также многочисленных химических веществ. Из 130 мл первичной мочи в канальцах реабсорбируется 129 мл воды (99%). Это приводит к очень значительному повышению концентрации растворенных в моче веществ и среди них ксенобиотиков. Таким образом, формируется высокий градиент концентрации веществ между содержимым канальцев и плазмой крови. Именно он является движущей силой обратной диффузии веществ из первичной мочи в кровь. Процессу свободной диффузии препятствует барьер, формируемый эпителием канальцев, межуточным веществом и эндотелием капилляров, оплетающих стенку канальцев. В целом свойства этого барьера аналогичны свойствам гистогематических барьеров других тканей. Определяющей является проницаемость эпителия канальцев. Закономерности, определяющие процесс диффузии ксенобиотиков и их метаболитов через стенку канальцев, полностью идентичны описанным ранее. Реабсорбции, прежде всего, подвергаются: а) жирорастворимые вещества; б) неионизированные молекулы водо-растворимых веществ; в) вещества с низкой молекулярной массой.
Проницаемость канальцевого барьера почти тождественна проницаемости слизистой кишечника, поэтому вещества, легко всасывающиеся при приеме через рот, затем трудно выводятся через почки, так как легко реабсорбируются из первичной мочи обратно в кровоток, а затем обратно - из кровотока в первичную мочу. Такая длительная тубуло-гломерулярная рециркуляция веществ (как правило, хорошо растворимых в липидах) приводит к существенному замедлению процесса их элиминации. Метаболизм кскенобиотиков (см. выше) во многом и предназначен для превращения жирорастворимых (плохо выводящихся из организма) веществ в водо-растворимые, способные к выведению из организма, соединения.
Выделение через почки слабых кислот и оснований существенно зависит от рН мочи. Как уже указывалось, вещества могут подвергаться реабсорбции в том случае, если молекула их не ионизирована. Из этого следует, что при подкислении мочи (путем назначения хлористого аммония) слабые основания (например алкалоиды) будут переходит в ионизированную форму, хуже реабсорбироваться и лучше выводиться из организма. При подщелачивании мочи (например, путем приема соды), по той же причине, из организма лучше будут выводиться слабые кислоты (например, барбитураты).
Помимо пассивной диффузии некоторые веществ в канальцах подвергаются активной реабсорбции. К числу таких веществ относятся естественные метаболиты: лактат, глюкоза, мочевая кислота, которые после их фильтрации в первичную мочу, попадают обратно в кровь. Для ксенобиотиков этот механизм не имеет существенного значения.
2.3. Канальцевая секреция
Многие органические кислоты (пробеницид, глюкурониды, салициловая кислота, пенициллин и т.д.) быстро переходят из крови в мочу. В основе быстрого переноса таких соединений в просвет почечных канальцев лежит активный транспорт. Транспортные системы находятся в проксимальном отделе почечных канальцев. Этот процесс направлен против градиента концентрации вещества, является насыщаемым, зависит от интенсивности обмена веществ, конкурентно ингибируется веществами с близким строением. Так, пробеницид блокирует экскрецию пенициллина или р-аминсалициловой кислоты. Специфичность транспортных механизмов невелика. Условием переноса является наличие в молекуле групп СООН- или SO3- и гидрофобного участка. Переносу подлежат соединения как простого, так и сложного строения. Связывание субстрата с молекулами-переносчиками осуществляется за счет ионных и водородных связей.
Иногда процессу активной секреции из крови в просвет канальцев противодействует простая диффузия вещества в противоположном направлении. Например, мочевая кислота с одной стороны активно секретируется, а с другой - пассивно диффундирует обратно в кровоток. Пробеницид в большей степени угнетает реабсорбцию вещества и поэтому при его введении наблюдается усиленная экскреция мочевой кислоты из организма.
В почечных канальцах существует система активного выведения и веществ со свойствами слабых оснований: тетраэтиламмония, алкалоидов (морфина, хинина), имипрамина, мекамиламина и др. Эта система не блокируется пробеницидом.
Механизмы активной секреции обнаруживаются у большинства позвоночных.
2.4. Совместное действие механизмов почечной экскреции
Количество отфильтрованного вещества в единицу времени можно рассчитать по формуле:
GFR Cp = V Cn, где
GFR - скорость гломерулярной фильтрации (мл/мин)
Cp - концентрация вещества в плазме крови
Cn - концентрация вещества в моче
V - объем мочи (мл)
Формула справедлива для веществ, не подвергающихся реабсорбции (например, для инулина с МВ - 5500). С помощью инулина можно оценить характеристики гломерулярной фильтрации. При достижении равновесного состояния концентрации веществ в плазме (Cp) имеем:
GFR = V Cn/Cp = Clин
Получаемая величина называется клиаренсом. Клиаренс (Cl) - это объем плазмы крови, очищаемой от токсиканта в единицу времени. В условиях клиники исследуют легко определяемый клиаренс инулина, по значению которого (129 мл/мин) можно судить о состоянии гломерулярной фильтрации.
При сравнении клиаренса инулина с клиаренсом других веществ могут быть получены три вида результатов (см. рисунок 2):
1. Clвещества/Clин = 1. Почечное выделение вещества осуществляется только путем гломерулярной фильтрации.
2. Clвещества/Clин < 1. Выделяется меньше вещества, чем отфильтровывается, т.е. возможна канальцевая реабсорбция.
3. Clвещества/Clин > 1. Выделяется больше вещества, чем отфильтровывается, т.е. возможна активная канальцевая секреция вещества.
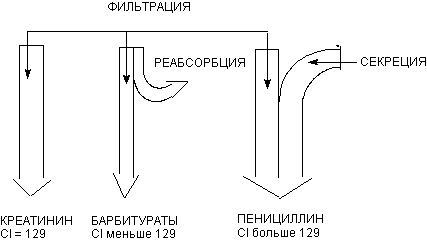
Рисунок 2. Схема, иллюстрирующая совместное действие механизмов, влияющих на почечную экскрецию
О механизмах, лежащих в основе выведения ксенобиотиков через почки, можно судить и по соотношению их концентраций в моче и плазме крови. Если это соотношение близко 100 - в основе процесса лежит фильтрация; если существенно меньше 100 - фильтрации сопутствует реабсорбция значительной части токсиканта; если больше 100 - превалируют механизмы секреции ксенобиотика (таблица 3).
Таблица 3. Соотношение концентраций в моче и плазме крови (моча/плазма) некоторых органических соединений
| Вещество | Моча/плазма |
| Алифатические углеводороды | 0,07 - 0,09 |
| Хлорированные углеводороды | 0,1 - 1,0 |
| Кетоны | 1,0 - 1,3 |
| Алифатические спирты | 1,0 - 1,3 |
| Гликоли | 3,0 - 5,0 |
| Эфиры полигликолей | 40 - 70 |
| Динитро-о-крезол | 0,2 |
| Трихлоруксусная кислота | 3,0 |
| Конъюгированные фенолы |
3. Выделение печенью
В отношении ксенобиотиков, попавших в кровоток, печень выступает и как орган экскреции и как основной орган их метаболизма. Печень выделяет химические вещества в желчь, причем не только экзогенные, но и эндогенные, такие как желчные кислоты, желчные пигменты, электролиты.
Выделяющиеся вещества должны проходить через барьер, образуемый эндотелием печеночных синусов, базальной мембраной и гепатоцитами. Структура барьера более подробно рассмотрена ранее.
В процессе экскреции ксенобиотиков осуществляется в два этапа:
- захват гепатоцитами;
- выделение в желчь.
Оба этапа могу проходить либо в форме простой диффузии, либо активного транспорта. Механизм выделения определяется строением вещества:
1. Захват гепатоцитами.
А. Диффузия:
- липофильные молекулы.
Б. Система активного транспорта:
- желчные кислоты и соединения с близким строением (фаллотоксин);
- билирубин;
- органические анионы (варфарин, оротовая кислота, рифампицин);
- органические катионы (четвертичные соединения азота, прокаинамид);
- нейтральные органические молекулы (оуабаин, стероидные гормоны);
- металлы (железо, кадмий).
В. Пиноцитоз:
- макромолекулы, протеины;
2. Билиарная экскреция.
А. Диффузия:
- неорганические ионы.
Б. Система активного транспорта:
- желчные кислоты;
- органические анионы;
а) без биотрансформации:
- хлортиозид и др.
б) после конъюгации:
- билирубин, стероиды, гексахлорфенол и др.
- органические анионы (тубокурарин);
- нейтральные органические соединения (оуабаин, моносахариды).
3. Пиноцитоз:
- макромолекулы, белки.
Свободная диффузия веществ, связанных с белками плазмы крови, практически не возможна. Напротив, путем активного захвата (пиноцитоза) из плазмы могут удаляться и связанные с белками вещества.
Ксенобиотики, попавшие в гепатоциты, отчасти определяются в цитозоле, отчасти - в отдельных субклеточных фракциях. Как известно в печени осуществляется метаболизм многих веществ. Именно они, прежде всего, и фиксируются различными протоплазматическими структурами. Часть соединений, в том числе и эндогенных (билирубин), находится в цитозоле в связанной с белками форме, что также имеет значение для их элиминации и детоксикации. Гепатоциты синтезируют специальные белки, ответственные за выведение ксенобиотиков из клеток, это так называемые мультиспецифичные переносчики органических анионов (MRP) и р-гликопротеины (P-gp). Оба типа белков первоначально были обнаружены в клетках резистентных к токсическому действию противоопухолевых препаратов. Позже было установлено, что их функция - активный транспорт ксенобиотиков через клеточные мембраны. MRP способны переносить лиганды, конъюгированные с глутатионом, глукуроновой кислотой, сульфатом. Таким образом, ll фаза метаболизма не только превращает вещества в более растворимые в воде, но и "подготавливает" к активному транспорту за пределы клетки. P-gp транспортируют в основном жирорастворимые ароматические соединения с молекулярной массой 300 - 500 дальтон и амфифильные молекулы, содержащие катионную аминогруппу.
В желчи в том или ином количестве обнаруживаются вещества, относящиеся практически ко всем классам химических соединений. В соответствии со значением коэффициента СЖ/СП (СЖ - концентрация в желчи; СП - концентрация в плазме крови) ксенобиотики могут быть разделены на три группы.
Вещества, выделяющиеся печенью путем простой диффузии, могут оказаться в желчи лишь в концентрации, равной его концентрации в плазме крови (СЖ = СП). Так, для ионов Na+, K+, Cl- коэффициент СЖ/СП приблизительно равен 1,0.
Для веществ, попадающих в гепатоцит, а затем и в желчь, с помощью механизмов активного транспорта, коэффициент может быть существенно выше 1,0. Как правило, активно выделяются печенью амфифильные вещества, содержащие в молекуле как полярные, так и неполярные группы. У некоторых соединений, нашедших применение в клинической практике, значение коэффициента очень велико (прокаинамид-этобромид - 118, хинин - 19,7). Из веществ, активно секретируемых в желчь, наиболее изученным является бромсульфолеин. У крыс при введении в дозе 5 мг/кг лишь 10% сохраняется в плазме крови, а 90% переходит в ткани, из них 80% - в печень, с последующим выделением в желчь.
Наконец, некоторые химические вещества плохо проникают в гепатоциты и желчь. Для них коэффициент СЖ/СП меньше 1,0. Среди таковых - макромолекулы, например, инсулин, фосфолипиды, белки.
Молекулярная масса соединения является важнейшим фактором, определяющим путь его элиминации. Существует порог, ниже которого располагаются вещества, выделяющиеся преимущественно через почки, выше - через печень. Значение порога достаточно условно, поскольку неодинаково у представителей различных видов: у крыс - 325 дальтон, у морских свинок - 400, у кроликов - 475, 500 - 700 - у человека. Кроме того, преимущественно через почки выделяются вещества, хорошо растворяющиеся в воде, даже с молекулярной массой выше "пороговых" значений (таблица 4).
Таблица 4. Экскреция производных бифенила у крыс
| Ксенобиотик | Мол. масса | Моча (%) | Кал (%) |
| Бифенил 4-монохлорбифенил 4,4-дихлорбифенил 2,4,5,2,5-петахлорбифенил 2,3,6,2,3,6-гексахлорбифенил |
(Hodgson E., Guthrie F.E., 1980)
Попавшие в желчь вещества увеличивают ее осмотическое давление, что вторично способствует переходу в этот секрет воды и растворенных в ней ионов. Вследствие этого ксенобиотики, активно выделяющиеся в желчь, в той или иной степени обладают желчегонным действием.
Печеночный клиаренс определяется как:
Cl = Fhep (Ca - Cv)/Ca, где
Ca - концентрация веществ в крови печеночной артерии и портальной вены;
Cv - концентрация веществ в крови печеночной вены;
Fhep - интенсивность печеночного кровотока (мл/мин).
Если захват вещества гепатоцитами осуществляется с большой скоростью, то клиаренс пропорционален скорости печеночного кровотока. Эта величина в норме у человека составляет около 1 мл/мин на г печеночной ткани.
Скорость выведения некоторых веществ в желчь весьма велика. Например период полувыведения бенз(а)пирена печенью крыс после внутривенного введения составляет около 1,7 минуты, т.е. в течение 5 минут выделяется около 60% от введенной дозы. Однако это совсем не означает, что с такой же скоростью вещество выводятся из организма. Дело в том, что если с желчью выделяется липофильное соединение, то в просвете кишечника, оно подвергается быстрой обратной резорбции и по системе портальной вены вновь поступает в печень - развивается "внутрипеченочная циркуляция" ксенобиотика. Поэтому жирорастворимые вещества (в том числе и бенз(а)пирен) надолго задерживаются в организме. Их элиминация возможна лишь в результате биотрансформации в той же печени и/или других органах (см. выше). Таким образом, путем билиарной экскреции из организма с калом могут выделяться только плохо растворимые в жирах соединения.
4. Выделение через кишечник
С экскрементами вещество или его метаболит выделяются в следующих случаях:
а) в результате неполного всасывания в желудочно-кишечном тракте;
б) в результате билиарной экскреции без последующей реабсорбции в кишечнике;
в) в результате выделения слизистой желудочно-кишечного тракта.
Упомянутые обстоятельства могут складываться изолированно, либо действовать в комплексе.
Под интестинальной экскрецией понимают процесс перехода вещества или его метаболитов из крови в просвет кишечника с последующим выделением с фекалиями.
Некоторые вещества выделяются в значительном количестве уже в желудке (морфин, некоторые другие алкалоиды). Это наблюдается даже при парентеральном способе введения указанных соединений и является следствием значительного различия рН крови и содержимого желудка (см. выше). Токсиканты, способные выделяться в просвет желудка, в кислой среде находятся исключительно в протонированной форме и потому не всасываются обратно в кровь. Однако если при переходе в кишечник (щелочная среда), выделившееся вещество вновь превращается в неионизированную форму, оно всасывается обратно в кровь и не выделяется из организма. Промывание желудка в подобных ситуациях может оказаться весьма полезной процедурой, позволяющей существенно ускорить удаление токсиканта из организма.
Жирорастворимые вещества могут выделяться в просвет кишечника путем простой диффузии, однако вследствие реабсорбции, их концентрация при этом не будет превышать концентрацию в плазме крови. Тем не менее, сравнение в эксперименте интенсивности выделения жирорастворимых веществ почками и кишечником показывает, что преобладает кишечная экскреция.
Некоторые соединения, например моночетвертичные азотсодержащие вещества (N-метилскополамин, N-метилникотинамид, тетраэтиламмоний и т.д.) после внутривенного введения экспериментальному животному обнаруживаются в просвете кишечника.
Выделение с калом характерно для тяжелых металлов. Особенности и механизмы процесса до конца не изучены. Не исключено, что экскретируются элементы в связанной с белками форме. Выведение свинца, например, существенно увеличивается при увеличении в рационе белковых продуктов.
5. Другие пути выведения
Некоторое практическое значение имеет выведение веществ с молоком кормящих матерей и секретом потовых, сальных, слюнных желез. Как правило, в основе появления токсиканта в секрете желез лежит механизм простой диффузии. Эти способы экскреции практически не сказываются на продолжительности нахождения веществ в организме, но могут лежать в основе появления отдельных признаков интоксикации (угреобразная сыпь при отравлении полигалогенированными полициклическими углеводородами; свинцовая кайма на деснах). Возможно отравление новорожденных, питающихся молоком матери, кантаминированным такими веществами как кофеин, алкоголь, витамины, гормональные препараты, галогенсодержащие инсектициды, металлы и т.д.
Элиминация ксенобиотиков в молоко зависит от степени их персистентности в организме. Быстро элиминируемые, хорошо растворимые в воде ксенобиотики таким путем практически не выделяются. Жирорастворимые соединения с большим периодом полувыведения определяются в молоке порой в значительных количествах. Так в эксперименте установлено, что элиминация хлорсодержащих инсектицидов в коровье молоко может составлять до 25% от введенного количества.
ГЛАВА 4.6. КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ТОКСИКОКИНЕТИКИ
Важнейшим этапом изучения токсикокинетики ксенобиотика является определение количественных характеристик процессов резорбции, распределения, элиминации. Методология определения токсикокинетических констант постоянно совершенствуется. Её развитие сопряжено с внедрением в практику исследований новых методов количественного определения веществ в биосредах и развитием математического аппарата анализа данных. Ниже будет представлена характеристика некоторых, наиболее часто встречающихся, методических приемов.
1. Скорость элиминации. Константа скорости элиминации. Время полуэлиминации
Как указывалось ранее, в понятие элиминации включаются все процессы, приводящие к снижению содержания чужеродного вещества в организме. Для количественной характеристики элиминации прибегают к проведению основного (базисного) токсикокинетического эксперимента. В ходе эксперимента внутривенно вводят исследуемое вещество в дозе "Д", а затем определяют в динамике концентрацию вещества "С" в плазме крови. Полученные результаты представляют в графической форме зависимости "С" от времени после введения "t" (рисунок 1). В большинстве случаев зависимость имеет вид экспоненты: временная зависимость 1-го порядка. В соответствии с кинетическим уравнением 1-го порядка имеем:
dC/dt = -КЕС,
т.е. скорость процесса в каждый момент времени пропорциональна концентрации вещества.
Мерой скорости элиминации вещества является величина угла наклона касательной к кривой, проведенной в интересующей исследователя точке, или величина дифференциала dC/dt. Скорость элиминации уменьшается с течением времени, поскольку уменьшается величина C. Однако неизменной характеристикой процесса остается коэффициент пропорциональности КЕ.
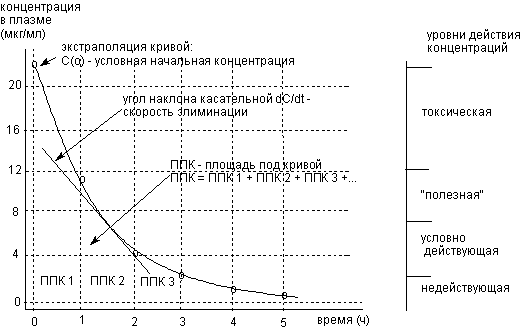
Рисунок 1. Зависимость концентрации вещества в плазме крови от времени после внутривенного введения
Интегрируя уравнение, имеем:
lnC0/Ct = KEt, где
C0 - исходная концентрация вещества;
Ct - концентрация вещества в момент времени t;
t - время после введения вещества;
KE - константа скорости процесса элиминации;
Для определения КЕ необходимо представить зависимость концентрации вещества в плазме от времени в полулогарифмической системе координат (рисунок 2). При этом зависимость приобретает линейный характер. Константа элиминации определяется как честное от деления  lnС/
lnС/  t. После определения величины КЕ легко определить еще один важный токсикокинетический параметр, а именно величину времени полуэлиминации (t1/2), т.е. время в течение которого из организма элиминируется половина введенного вещества. Время полуэлиминации связано простой зависимостью с величиной константы скорости элиминации:
t. После определения величины КЕ легко определить еще один важный токсикокинетический параметр, а именно величину времени полуэлиминации (t1/2), т.е. время в течение которого из организма элиминируется половина введенного вещества. Время полуэлиминации связано простой зависимостью с величиной константы скорости элиминации:
t1/2 = ln2/КЕ = 0,693/КЕ

Рисунок 2. Зависимость концентрации вещества в плазме крови от времени после внутривенного введения в системе полулогарифмических координат
2. Объем распределения.
Представление зависимости концентрации вещества в крови от времени в полулогарифмических координатах (рисунок 2) позволяет расширить информацию об особенностях токсикокинетики вещества, введенного внутривенно.
Начальная концентрация вещества СО в плазме крови не доступна для непосредственного измерения, поскольку необходимо время перемешивания ксенобиотика в крови (этап конвекции). Однако как условная величина СО имеет токсикокинетическое значение. Она может быть определена путем экстраполяции прямой зависимости lnC от времени к моменту t = 0. Значение С0 и величина введенной дозы Д позволяют рассчитать объем распределения вещества Vd до того, как начался процесс элиминации ксенобиотика:
Vd = Д/СО
Отнеся полученную величину к массе тела (М) получаем значение (VR):
VR = Vd/М
Значения относительного объема распределения и времени полуэлиминации некоторых ксенобиотиков представлены в таблице 1.
Таблица 1. Токсикокинетические характеристики некоторых веществ
| Вещества | VК (л/кг) | t1/2 (ч) |
| Ацетилсалициловая кислота Пенициллин G Нитроглицерол Дигитоксин Этанол Фенобарбитал Морфин Дигоксин Хлорпромазин | 0,14 0,30 0,35 0,50 0,55 0,80 3,0 10,0 20,0 | 0,25 0,5 6,5 - 2,5 |
3. Клиаренс
Под клиаренсом понимают условный объем плазмы крови (мл), который полностью освобождается от находящегося в ней ксенобиотика в единицу времени. По Досту (Dost) все процессы, участвующие в элиминации вещества в конечном итоге суммируются и определяют так называемый "общий клиаренс" вещества (Cltot). При этом можно выделить элементы общего клиаренса, обеспечиваемые деятельностью основных органов выведения: почек, печени, легких, и метаболизмом ксенобиотиков, и рассматривать их отдельно как почечный (ClR), печеночный (ClH) и т.д. клиаренс:
Cltot = ClR + ClH + Cl...
Определение общего клиаренса осуществляется на основе данных, полученных в ходе базисного токсикокинетического эксперимента (см. выше). Для этого по данным, представленным на рисунке 1, определяют величину площади под кривой зависимости "концентрация-время" (ППК). Клиаренс рассчитывают как:
Cltot = Д/ППК
Чем больше площадь под кривой при введенной дозе ксенобиотика, тем ниже значение клиаренса, т.е. тем дольше вещество выводится из организма. Клиаренс через отдельные органы рассчитывают с учетом количества вещества, выделяемого через эти органы. Значения клиаренса некоторых летучих токсикантов представлены в таблице 2.
Таблица 2. Респираторный и метаболический клиаренс некоторых летучих органических растворителей у человека
| Растворители | Респираторный клиаренс | Метаболический клиаренс | ||
| л/ч | % | л/ч | % | |
| Бензол | ||||
| Толуол | ||||
| Ксилол | ||||
| Стирол | ||||
| Дихлорметан | ||||
| Хлороформ | ||||
| Четыреххлористый углерод | ||||
| 1,1-дихлорэтан | ||||
| 1,2-дихлорэтан | ||||
| 1,1,1-трихлорэтан | ||||
| 1,1,2-трихлорэтан | ||||
| 1,1,1,2-тетрахлоэтан | ||||
| 1,1,2,2,-тетрахлорэтан | ||||
| Трихлорэтилен | ||||
| Тетрахлорэтилен |
(A. Sato, T. Nakajima, 1987)
На принципе определения величины ППК основывается расчет и другой токсикокинетической характеристики вещества - биодоступности.
4. Биодоступность
Под биодоступностью понимают способность вещества, находящегося в определенном агрегатном состоянии и связи с инертными носителями (почва, пища, растворитель и т.д.), абсорбироватся во внутренние среды организма и достигать места взаимодействия с системами-мишенями.
Поскольку место действия для подавляющего большинства токсикантов не определено, или недоступно для экспериментального анализа, принято допущение, согласно которому содержание вещества в крови линейно связано с величиной его биодоступности.
Дата публикования: 2014-11-04; Прочитано: 319 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
