 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Углеродсодержащих соединений
|
|
Научной основой плазмохимической переработки углеродсодержащих веществ послужили результаты термодинамического анализа равновесных систем, включающих элементы природных горючих соединений в соответствующих соотношениях и плазмообразующих газов, в температурном диапазоне от 2000 до 5000 К.
Как было изложено в главе 3, располагая надежными термодинамическими константами, можно, а в большинстве случаев и необходимо, оценивать оптимальные условия проведения реакций, интервалы температур, давлений, соотношение реагентов, значения ожидаемых выходов целевых и побочных продуктов, энергетические показатели процессов. Путём сопоставления экспериментальных и рассчитанных термодинамических равновесных составов можно выяснить следующее:
- являются ли экспериментальные составы равновесными или они образуются на промежуточных стадиях химических превращений;
- оптимальны ли выбранные условия проведения экспериментов (температура и давление, затраты энергии на получение целевого продукта);
- оптимален ли режим закалки, применявшийся в экспериментах;
- какова доля в полученных конечных продуктах тех или иных радикалов и промежуточных соединений, рекомбинирующих в процессе закалки.
Как было показано в главе 3 (рис. 3.1), результаты термодинамического расчёта системы С-Н в температурной области от 1500 до 5000 К выше 2500 К единственным стабильным углеводородом является ацетилен. Его максимальная концентрация соответствует температуре Т ~ 3300 К. Другими основными продуктами в этом узком температурном интервале являются конденсированный углерод (С)к и водород. В этой связи очевидны направления и условия реализации процессов пиролиза углеродсодержащих веществ в промышленности.
Применительно к реальным условиям процесса плазменного пиролиза конкретных углей 3-х месторождений был выполнен уточненный детальный термодинамический анализ. Характеристики этих углей и их состав даны в табл. 4.1 и 4.2. Рассматривалось два варианта:
- разложение угля без учёта разбавления угольной массы плазмообразующим газом - аргоном и
- реальный процесс пиролиза углей в инертной среде аргона, содержание которого в системе составляло 99 мас. %.
Таблица 4.1
Характеристика исследуемых углей, мас.% (на рабочую массу)
| Уголь | № пробы | W | A | C | H | S | O | N |
| Подмосковный | 5,78 | 3,13 | 56,16 | 5,24 | 1,97 | 26,70 | 1,02 | |
| Агулакский | 0,84 | 3,96 | 70,21 | 4,33 | 2,38 | 17,28 | 1,00 | |
| Будаговский | 7,23 | 31,23 | 45,20 | 5,82 | 0,50 | 9,06 | 0,96 |
Таблица 4.2
Состав минеральной части исследуемых углей, мас.%
| Уголь | № пробы | Al2O3 | SiO2 | Fe2O3 | СаО | МgO | К2O | Nа2О |
| Подмосковный | 22,10 | 60,90 | 8,80 | 4,40 | 1,90 | 1,90 | - | |
| Агулакский | 13,00 | 47,00 | 8,00 | 26,0 | 5,00 | 0,50 | 0,50 | |
| Будаговский | 11,66 | 70,18 | 6,05 | 9,50 | 2,37 | 0,04 | 0,19 |
Основная особенность использования математической модели заключалась в рассмотрении гетерогенной системы угольной массы в двухфазном приближении. Расчёт предусматривал следующие допущения. Газовая фаза – смесь идеальных газов, конденсированная фаза – идеальный раствор жидких и твёрдых веществ с неограниченной растворимостью. Основной принцип расчёта – минимизация свободной энергии реагирующей системы – функции Гиббса.
Результаты расчёта проиллюстрированы на рис. 4.1 и 4.2.
Основные выводы, полученные из термодинамического анализа плазменного пиролиза углей в области температур от 2000 до 5000 К, говорят о следующем:
· Угольная система в рассматриваемой температурной области равна по фазам (газовая и конденсированная) при температуре 800 К и предпочтительна в газовой фазе выше 1000 К. При температурах 3000-3500 К весь уголь переходит в газообразное состояние.
· Из всего обилия компонентов основными газовыми компонентами равновесной системы являются Н2, СО и С2Н2.
· Ацетилен является единственным углеводородом, присутствующим в системе в области 2500-5000К и максимум его концентрации при Т»3200 К равен 8 об.%.
· В равновесной системе присутствует радикал С2Н-, в концентрациях, соизмеримых с С2Н2, в значительных количествах находятся такие радикалы и атомы, как СН+, СН2, С2, С, Н и др., которые можно рассматривать как источник дополнительного образования ацетилена в процессе их рекомбинации в стадии закалки.
· Равновесный состав газовой смеси слабо зависит от элементного состава исходного угля. Картины равновесных систем крайних представителей углей одного морфологического ряда очень схожи по своему составу их газовой фазы.
· Разбавление угольной массы (аргоном, водородом) сдвигает максимумы концентраций ряда компонентов в область более низких температур.
· Образование таких соединений, как Н2О, СО2, SO2, SO, NO, NO2, CH4 термодинамически "запрещено" в рассматриваемой температурной области.
· Существование конденсированной фазы ограничено температурой 3500 К.
· Качественный состав конденсированной фазы одинаков для всех углей. Он представлен в основном такими соединениями, как конденсированный (твёрдый) углерод, карбид кремния, диоксид кремния, жидкими металлами Al и Fe, жидким кремнием.
· В реальном процессе, варьируя температуру плазмообработки, можно получить твёрдый остаток заданного состава. И наоборот, зная точный состав твёрдого остатка, можно оценить конечную температуру прогрева угля за время его пиролиза в плазме.
Знания, полученные теоретическим путём, обогатили и углубили понимание реального процесса пиролиза углей и позволили наметить пути повышения совершенства процесса по его основным показателям.
Для процесса плазмохимической газификации углей также неоднократно проводился термодинамический анализ.
В качестве еще одного примера приведем основные выводы, полученные при расчёте термодинамического равновесного состава системы С-Н-О-S-N-Si-Al-Fe.
Расчёт выполнен в диапазоне температур 1000-3000 К и давлении (0,1-1,0).105 Па при заданных соотношениях между элементами. В результате расчёта получены следующие основные выводы:
· Основные целевые продукты, (СО + Н2) – синтез-газ, являются равновесными в рассматриваемом диапазоне температур и давлений.
· При паровой газификации максимальные концентрации (СО + Н2) находятся в области 1400-1800 К. Повышение температуры выше 2000 К ведёт к заметной диссоциации водорода и снижению концентрации синтез-газа.
· С энергетической точки зрения из всех вариантов газификации (воздух, кислород, пар, пар-воздух) наиболее экономична паровая и паровоздушная газификация, осуществляемая при стехиометрическом соотношении С:О.
· Возможно получение синтез-газа с заранее заданным составом, например, (СО + Н2):N2 = 3:1, путём варьирования исходного состава компонентов.
· В указанном выше диапазоне температур состав конденсированной фазы не влияет на процесс газификации.
· Повышение давления в системе с 0,1.105 до 1,0.105 Па приводит к росту энергозатрат в 1,5-2 раза.
Таким образом, приведенные расчёты по термодинамике равновесного состава угольных систем в области температур 1000-5000 К убедительно и наглядно показывают возможность переработки углеродсодержащих веществ путём привлечения плазменной техники, обеспечивающей достижение указанных температур, либо непосредственно в ацетилен, а также синтез-газ и технический углерод в качестве побочных продуктов, либо в синтез-газ как основной продукт (в зависимости от вида плазмообразующего газа). При этом образование таких нежелательных с точки зрения экологии продуктов, как оксиды серы и азота термодинамически невозможно. Диоксид углерода также отсутствует в газовой фазе в условиях пиролиза, а при газификации его концентрации чрезвычайно низки.
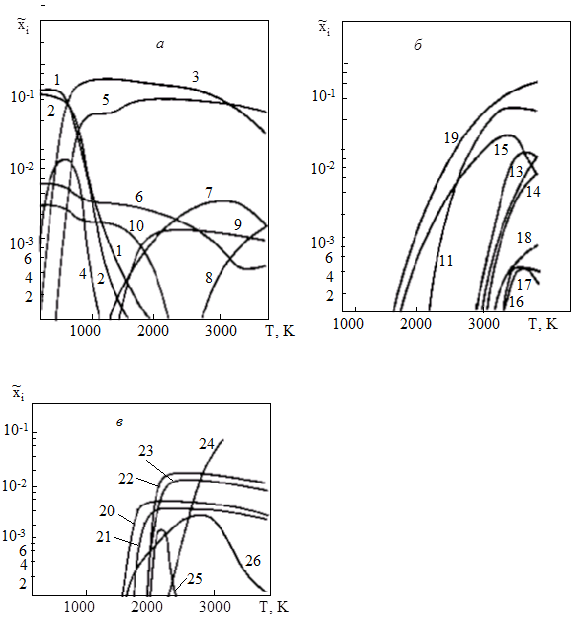
Рис. 4.1.(а, б, в). Равновесный состав газовой фазы угольной массы (уголь № 3) без учета разбавления аргоном:
1 – СН4; 2 – Н2О; 3 – Н2; 4 – СО2; 5 – СО; 6 – N2; 7 – НСN; 8 – СN; 9 – СS; 10 – Н2S; 11 – С2Н2; 12 – С2Н; 13 – С; 14 – С2; 15 – С3; 16 – С4; 17 – С5; 18 – СН; 19 – Н; 20 – Fе; 21 – Мg; 22 – Са; 23 – Аl; 24 – Si; 25 – Аl2О, 26 – SiО

Рис. 4.2. Равновесный состав конденсированной фазы угольной массы (уголь № 3) без учета разбавления аргоном:
1 – С; 2 – SiО2(l); 3 – SiС(с)-β; 4 – СаО(с); 5 – Al2O3(с); 6 – FеО(l); 7 – МgО(с); 8 – Fе3О4; 9 – Fе2О3(с); 10 – AlКО2(l). (Индексы (с) и (l) относятся соответственно к твердому и жидкому состоянию соединений)
Дата публикования: 2014-11-02; Прочитано: 585 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
