 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Катаболизм аминокислот. Пере- и дезаминирование аминокислот
|
|
Промежуточный метаболизм аминокислот белковых молекул, как и других пита-тельных веществ в живых организмах, включает катаболические (распад до конеч-ных продуктов обмена), анаболические (биосинтез аминокислот) процессы, а также ряд других специфических превращений, сопровождающихся образованием биологически активных соединений. Условно промежуточный метаболизм аминокислот можно разделить на общие пути обмена и индивидуальные превращения отдельных аминокислот.
Дезаминирование аминокислот:
Доказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы). Выделены соответствующие ферментные системы, катализирующие эти реакции, и идентифицированы продукты реакции. Во всех случаях NH2-группа аминокислоты освобождается в виде аммиака.
I. Восстановительное дезаминирование
II. Гидролитическое дезаминирование
III. Внутримолекулярное дезаминирование
IV. Окислительное дезаминирование
Помимо аммиака, продуктами дезаминирова-ния являются жирные кислоты, оксикислоты и кетокислоты. Рассмотрим более подробно механизм окислительного дезаминирования аминокислот, протекающего в две стадии.
Первая стадия является ферментативной и завершается образованием неустойчивого промежуточного продукта (иминокислота), который на второй стадии спонтанно без участия фермента, но в присутствии воды распадается на аммиак и а-кетокислоту.
Под переаминированием подразумевают реакции межмолекулярного переноса аминогруппы (NH2 —) от аминокислоты на а-кетокислоту без промежуточного образования аммиака. Реакции переаминирования являются обратимыми и универсальными для всех живых организмов. Эти реакции про-текают при участии специфических ферментов-аминофераз. Теоретически реакции трансаминирования возможны между любой амино- и кетокислотой, однако наиболее интенсивно они протекают в том случае, когда один из партнеров представлен дикарбоновой амино- или кетокислотой.
 22.Пути выведения аммиака из организма. Биосинтез мочевины.
22.Пути выведения аммиака из организма. Биосинтез мочевины.
Распад биогенных аминов
Обезвреживание NH3 в организме путем связывания и образования водорастворимых,выделяющихся с мочой не таксичных соединений.Типы азотистого обмена: -амониотелический(рыбы)-гл.конечн. продукт NH3,-уреотелический(чел-к,животные) основной конечный продукт-мочевина,- урикотеличе-ский(птицы,рептилии) главный конечный продукт-мочевая к-та.
Один из путей связывания и обезвреживания аммиака в мозге,сетчатке,почках,печени,мышцах-биосинтез Глм и Асп в Глн-синтетазной р-ции,выделяется в небольших количествах с мочой и выполн-щих транспортную фун-ию переноса NH3 в нетаксичной фор-ме.Асп+АТФ+NH3(или Глн)→Асп+ АМФ+РР1+(Глу)
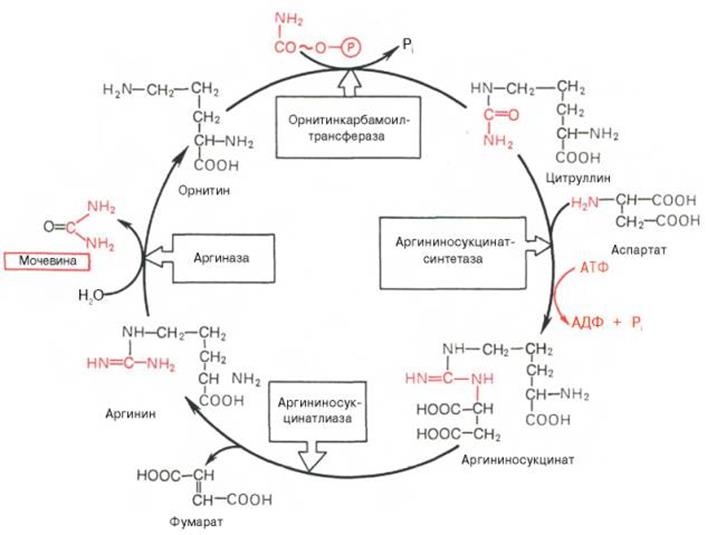
α-кетоглутарат→глутамат→глутамин.Основной механизм обезвреживания NH3-биосинтез в печени мочевины, экскретируемой с мочой (80-85% от всего азота мочи) в качестве основного конечного продукта белкового(АМК)обмена.Цикл мочевинообразования:синтез макроэргического соединения карбомоилфосфата-метаболич.активная форма NH3,исполь-ая в кач-ве исход-го продукта для синтеза пиримидиновых нуклеотидов

Пути синтеза карбомоилфосфата:1-использ.для синтеза Арг и мочевины
2-преимущ-но использ. для синтеза пиримидиновых нуклеотидов:
3-использ. для ресинтеза АТФ
Дата публикования: 2015-11-01; Прочитано: 1422 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
