 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Решение. Из данных задачи следует, что град
|
|
Из данных задачи следует, что  град. Для определения массовой доли сахарозы в растворе воспользуемся уравнением
град. Для определения массовой доли сахарозы в растворе воспользуемся уравнением
 ,
,
в которое подставим известные величины: ККР – криоскопическую константу, ККР = 1,86 град·моль-1·кг, 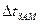 и молярную массу сахарозы М(С12Н22011) = 342 г/моль. Отношение
и молярную массу сахарозы М(С12Н22011) = 342 г/моль. Отношение

представляет собой массу растворенного вещества, приходящуюся на 1000 г растворителя, тогда
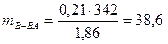 г.
г.
На 1000 г растворителя приходится 38,6 г сахарозы, поэтому для определения массовой доли растворенного вещества можно воспользоваться формулой

или составить пропорцию:
1038,6 г раствора содержит 38,6 г сахарозы;
100 г раствора – х г сахарозы.
Следовательно, массовая доля растворенного вещества составляет 3,71 %.
Пример 4. Определение молярной массы неэлектролита по температуре кристаллизации (кипения).
Раствор неэлектролита содержит 2,5 г растворенного вещества в 25 г бензола и замерзает при температуре 4,3 °С. Определить молярную массу растворенного вещества.
Дата публикования: 2015-10-09; Прочитано: 388 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
