 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Константа диссоциации. Взаимосвязь константы диссоциации и степени диссоциации. Закон разбавления Оствальда
|
|
Для некоторого электролита, распадающегося в растворе на ионы в соответствии с уравнением:
АaВb aАx + + bВy –,
константа диссоциации выразится следующим соотношением
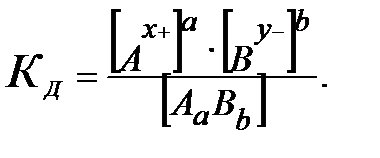
|
Константа диссоциации (KД или просто К) – отношение произведения равновесных концентраций ионов в степени соответствующих стехиометрических коэффициентов к концентрации недиссоциированных молекул.
Чем больше константа диссоциации КД, тем сильнее диссоциирует электролит. В отличие от степени диссоциации КД зависит только от природы растворителя, электролита и температуры, но не зависит от концентрации раствора.
В многоосновных кислотах и многоокислотных основаниях диссоциация происходит ступенчато, причем каждая ступень характеризуется своей величиной степени диссоциации. Так, ортофосфорная кислота диссоциирует по трем ступеням (таблица 1).
Таблица 1 – Диссоциация ортофосфорной кислоты
| Реакция | Константа диссоциации KД | Степень диссоциации α, % | |
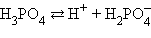
| 
| К1 = 7,1∙10–3 | |
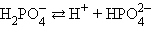
| 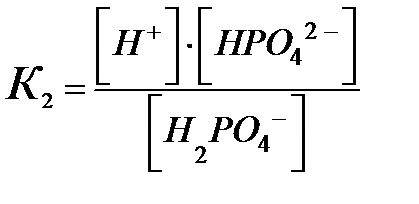
| К2 = 6,2∙10–8 | 0,15 |
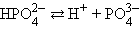
| 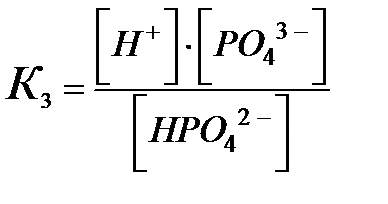
| К3 = 5,0∙10–13 | 0,005 |
Как видно, K1 > K2 > K3. Следовательно, наиболее полно диссоциация протекает по первой стадии, поскольку:
1) ион проще оторвать от нейтральной молекулы, чем от заряженного иона;
2) происходит подавление диссоциации, протекающей по второй и последующим стадиям, ионами, образующимися при распаде молекулы по первой ступени.
Между константой диссоциации КД, и степенью электролитической диссоциации α существует связь, выражаемая с помощью закона разбавления (разведения) Оствальда
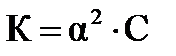
|
Отсюда
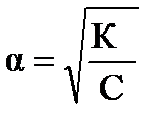 . .
|
Следовательно, степень диссоциации слабого электролита обратно пропорциональна концентрации и прямо пропорциональна разбавлению раствора, т. е. степень диссоциации слабого электролита в растворе тем выше, чем более разбавлен раствор.
Дата публикования: 2015-10-09; Прочитано: 2082 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
