 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Конкуренция за катион или анион
|
|
| 1) изолированное гетерогенное равновесие – образование в системе одного малорастворимого электролита: В растворе присутствуют в равных концентрациях ионы натрия Na+ и серебра Ag+. При введении хлорид-ионов Cl- образуется хлорид серебра. В реальных системах встречается редко. | 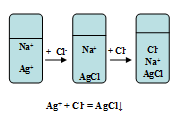
|
2) совмещенное гетерогенное равновесие – образование в системе нескольких малорастворимых электролитов, в первую очередь образуется менее растворимое соединение (с меньшим значением KS), затем более растворимое (с бóльшим значением KS). Происходит дробное осаждение.
а) исходная система – раствор ионов:
| 
|
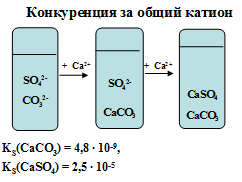
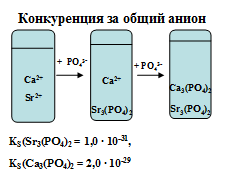
| В растворе присутствуют в равных концентрациях карбонат-ионы CO32- и сульфат-ионы SO42-. При введении ионов кальция в первую очередь в осадок переходит карбонат кальция, т.к. KS (CaCO3) < KS(CaSO4), а затем выпадает сульфат кальция | В растворе присутствуют в равных концентрациях ионы стронция Sr2+ и кальция Ca2+. При введении фосфат ионов PO43- в первую очередь в осадок переходит фосфат стронция, т.к. KS(Sr3(PO4)2) < KS(Ca3(PO4)2), а затем выпадает фосфат кальция. |
б) исходная система – насыщенный раствор малорастворимого электролита над осадком. Растворение осадка.
↓ CaSO4 + Na2CO3 ↔ ↓ CaCO3 + Na2SO4
насыщ. р-р
эта реакция идет легко и практически до конца в направлении слева направо (при нагревании, действием концентрированного раствора соды), т.к. KS(CaSO4) / KS(CaCO3) ≈ 5000. Т.к. сульфаты щелочноземельных металлов не растворяются в кислотах и щелочах, их перевод в легко растворимые карбонаты имеет практическое значение.
Важно учитывать при расчетах:
- Значение Кs.
- Концентрации веществ.
- Электролитный фон: I(КРОВИ) = 0,167, γ(Ca2+) = 0,42.
Дата публикования: 2015-10-09; Прочитано: 6648 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
