 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Мицеллярная теория строения коллоидной частицы
|
|
Всякий лиофобный (гидрофобный) коллоидный раствор состоит из двух частей: мицелл и интермицеллярной жидкости. Мицеллы — это отдельные коллоидные частицы, которые в совокупности составляют дисперсную фазу золя, а интермицеллярная жидкость — это дисперсионная среда того же золя, включающая помимо растворителя все другие растворенные в нем вещества (электролиты и неэлектролиты), которые не входят в состав мицелл.
Коллоидная мицелла имеет значительно более сложное строение, чем обычные молекулы. В ней различают две основные части: внутреннюю — нейтральную, обычно называемую ядром, и внешнюю — ионогенную, в свою очередь состоящую из двух слоев (двух ионных сфер).
Ядро составляет основную массу коллоидной мицеллы и представляет собой комплекс, состоящий из атомов (в случае гидрозолей металлов или неметаллов) или нейтральных молекул [в золях гидроксида железа (III) или иодида серебра]. Общее число входящих в состав ядра атомов или молекул огромно (от нескольких сот до миллионов) и зависит от степени дисперсности золя и от размеров самих атомов или молекул.
В процессе образования гидрофобного золя рост ядра в той или иной стадии может быть приостановлен созданием так называемого адсорбционного слоя из ионов стабилизатора. Ионная сфера вокруг ядра коллоидной мицеллы состоит из двух слоев (или двух сфер)— адсорбционного и диффузного. Адсорбционный слой слагается из слоя потенциалопределяющих ионов, адсорбированных на поверхности ядра и сообщающих ему свой заряд, и части противоионов, проникших за плоскость скольжения и наиболее прочно связанных электростатическими силами притяжения. Вместе с ядром эта ионная атмосфера образует как бы отдельный гигантских размеров многозарядный ион — катион или анион, называемый гранулой. Диффузный слой, расположенный за плоскостью скольжения, в отличие от адсорбционного не имеет в дисперсионной фазе резко очерченной границы. Этот слой состоит из противоионов, общее число которых равняется в среднем разности между всем числом потенциалопределяющих ионов и числом противоионов, находящихся в адсорбционном слое.
Гранула вместе с диффузным слоем противоионов составляет коллоидную частицу — мицеллу. Мицелла всегда электронейтральна. Необходимо отметить, что противоионами могут служить любые ноны тех электролитов, которые участвуют в реакциях при образовании данного золя или же присутствуют как посторонние примеси. Для примера рассмотрим получение гидрозоля иодида серебра методом конденсации. Оно основано на химической реакции
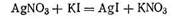
Согласно теории строения коллоидной мицеллы ядро в данном случае будет состоять из нейтральных молекул AgI.
11. Молекулярно-кинетические свойства коллоидных систем. Броуновское движение. Осмотическое давление. Седиментация.
Как показали многочисленные исследования, коллоидные системы по своим молекулярно-кинетическим свойствам принципиально ничем не отличаются от обычных (истинных) растворов, только эти свойства у золей и растворов высокомолекулярных соединений выражены значительно (в сотни и тысячи раз) слабее.
Все их молекулярно-кинетические свойства обусловлены броуновским движением.
Броуновское движение. Частицы дисперсной фазы золя под влиянием ударов молекул растворителя находятся в состоянии непрерывного хаотического движения. Так, если рассматривать какой-либо золь в ультрамикроскоп, можно заметить, что частицы золя все время беспорядочно движутся.
Впервые это явление было обнаружено английским ботаником Р. Броуном (1827). Он рассматривал суспензию растительной пыльцы в воде в микроскоп и подробно описал беспорядочные колебательные движения (в виде своеобразного, никогда не прекращающегося «танца»), совершаемые частицами пыльцы.
Вначале Броун считал, что эти движения присущи только живым существам, но вскоре убедился, что они свойственны любым суспензиям и эмульсиям органических и неорганических веществ при условии, что размер частиц достаточно мал (в пределах от 1 до 5 мкм).
Опыты показали, что броуновское движение совершенно не зависит от природы вещества; оно изменяется в зависимости от температуры, вязкости среды и размеров частиц.
Осмотическое давление. Для коллоидных растворов, как и для истинных, характерно осмотическое давление. Оно, подобно газовому давлению, является коллигативным свойством растворов, т. е. зависящим только от числа свободно движущихся коллоидных частиц.
Если учесть, что объем и масса коллоидной частицы значительно больше, чем объем и масса молекулы низкомолекулярных веществ, то при одной и той же весовой концентрации коллоидного и истинного растворов в единице объема золя содержится значительно меньше частиц, чем в единице объема истинного раствора. Вот почему по сравнению с последними коллоидные растворы обладают ничтожно малым осмотическим давлением.
осмотическое давление коллоидных растворов обратно пропорционально кубу радиуса частиц и, следовательно, прямо пропорционально кубу степени дисперсности.
Экспериментально осмотическое давление золей измеряют в приборах осмометрах. Для отсчета берут разность давлений в манометре. и вычисляют осмотическое давление.
Седиментационное равновесие. Частицы вещества, диспергированного в жидкой или газообразной среде, постоянно находятся под влиянием двух противоположно направленных сил — силы тяжести, под действием которой частицы данного вещества оседают, и сил диффузии, под влиянием которых частицы стремятся переместиться из области больших в область меньших концентраций, т. е. к равномерному распределению в объеме.
В зависимости от преобладания тех или иных сил в системе наблюдается осаждение частиц дисперсной фазы (под влиянием сил тяжести) или (в случае преобладания сил диффузии) выравнивание концентрации во всем объеме системы. Процесс оседания частиц под действием силы тяжести носит название седиментации (от лат. sedimentum — оседание). Скорость оседания частиц зависит не только от их размера, но и от разности плотностей частиц d—d0, а также от вязкости этой среды.
с большей скоростью оседают более крупные частицы. Диффузия в случае более мелких частиц дисперсной фазы протекает с большей скоростью и замедляется с увеличением их размера. Если степень дисперсности вещества мала (радиус частиц больше 2 нм), то частицы не совершают броуновского движения, следовательно, их способность к диффузии равна нулю. В данном случае сила тяжести значительно преобладает над силами диффузии.
Если в системе силы тяжести полностью уравновешены силами диффузии, наступает так называемое седиментационное равновесие, которое характеризуется равенством скоростей седиментации и диффузии.
Седиментационное равновесие наблюдается не только в коллоидных растворах, но и в молекулярно-дисперсных системах. Это равновесие характеризуется постепенным уменьшением концентрации частиц в направлении от нижних слоев к верхним. Распределение частиц в зависимости от высоты столба жидкости подчиняется гипсометрическому (или барометрическому) закону Лапласа в применении к золям: при увеличении высоты столба золя в арифметической прогрессии концентрация частиц убывает в геометрической прогрессии.
На определении скорости оседания частиц дисперсной фазы основаны все методы седиментационного анализа. Определив экспериментально скорость оседания частиц, можно рассчитать их размер, т. е. степень дисперсности.
12. Оптические свойства коллоидных систем. Светорассеивание. Эффект Тиндаля.
Дисперсные системы неоднородны, они гетерогенные. Обладают оптической неоднородностью, которая зависит от структуры, размеров и формы частиц.
В коллоидных системах частицы соизмеримы с длиной волны видимого света, поэтому для них характерно светорассеивание - рассеяние электромагнитных волн видимого диапазона при их взаимодействии с веществом. При этом происходит изменение пространственного распределения, частоты, поляризации оптического излучения, хотя часто под рассеянием понимается только преобразование углового распределения светового потока..
Интенсивное светорассеивание происходит, когда луч света проходит через дисперсную систему, частицы которой имеют размеры меньше длины волны падающего света.
Световой луч встречает частицу, как бы огибая её, изменяя своё направление.
В коллоидных растворах светорассеивание проявляется в виде опалисценсии – матовое свечение. Голубоватого оттенка или в проходящем свете – красновато-желтый оттенок.
Согласно теории светорассеивания интенсивность рассеивания света будет зависеть от числа частиц и Vчастиц, показателей преломления и длины волны падающего света.
Оптические методы являются наиболее распространенными методами изучения состава и структуры дисперсных систем.
Эффект Тиндаля, рассеяние Тиндаля —оптический эффект, рассеивание света при прохождении светового пучка через оптически неоднородную среду. Обычно наблюдается в виде светящегося конуса, видимого на тёмном фоне.
Характерен для растворов коллоидных систем (например, золейметаллов, разбавленных латексов, табачного дыма), в которых частицы и окружающая их среда различаются по показателю преломления. На эффекте Тиндаля основан ряд оптических методов определения размеров, формы и концентрации коллоидных частиц и макромолекул.
Эффект Тиндаля назван по имени открывшего его Джона Тиндаля.
13. Электрокинетические явления коллоидных систем. Фи- и дзета-потенциал. Электрофорез и электроосмос.
Электрокинетические явления были открыты профессором Московского университета Ф.Ф.Рейсом в 1808г. при исследовании электролиза воды.
Явление перемещения жидкости в пористых телах под действием электрического поля получило название электроосмоса, а явление перемещения частиц –электрофореза.
На границе раздела коллоидных частиц и дисперсной среды происходит образование двойного электрического слоя (ДЭС).
Электро-кинетические явления подразделяются на 2 гр:
1. Прямые явления – возникают под действием внешнего электрического поля (электрофорез и электроосмос)
2. Обратные явления – при механическом перемещении фазы возникает электронные потенциал (потенциал протекания и потенциал седиментации).
Электрофорез
Направленное перемещение частиц дисперсной фазы под действием приложенной разности потенциалов (электрофорез) можно наблюдать в седиментационно устойчивых дисперсных системах. При наложении на такую систему внешней разности потенциалов происходит разрыв двойного электрического слоя по плоскости скольжения, в результате чего частица получает определённый заряд и перемещается к соответствующему электроду.
При электрофорезе можно непосредственно измерять скорость движения частиц. Прибор представляет собой U-образную трубку, в колено которой вставлены электроды.
Трубку заполняют до уровня а-а исследуемым золем, на поверхность которого наливают контактную жидкость, имеющую одинаковую с золем электропроводность, и на электроды подают напряжение. Через определённые промежутки времени отмечают уровень золя в обоих коленах трубки. Естественно, что скорость перемещения частиц дисперсной фазы определяется значением -потенциала на частицах твёрдой фазы.
Отношение скорости движения дисперсной фазы к напряжённости электрического поля при электрофорезе называют электрофоретической подвижностью:
Электроосмос
Направленное перемещение жидкости в пористом теле под действием приложенной разности потенциалов (электроосмос) удобно изучать с помощью прибора
Прибор представляет собой U-образную трубку, в одно колено которой впаян капилляр 1 для точного определения количества протекающей жидкости, в другом -между электродами располагается пористое тело 2 (мембрана) из силикогеля, глинозёма и др. материалов.
В прибор наливают воду или водный раствор и отмечают уровень жидкости в капилляре. Если к электродам приложить разность потенциалов, то противоионы диффузного слоя, энергетически слабо связанные с поверхностью твёрдой фазы (мембрана), будут перемещаться к соответствующему электроду и благодаря молекулярному трению увлекать за собой дисперсионную среду (водный раствор). Чем больше потенциал диффузного слоя, тем больше переносчиков зарядов, тем выше скорость перемещения жидкости в пористом теле. Скорость течения жидкости и её направление при постоянной напряжённости электрического поля определяются свойствами мембраны и раствора. Таким образом качественное изучение электроосмоса позволяет однозначно определить знак -потенциала, а количественные измерения -установить зависимость между скоростью переноса жидкости и -потенциалом. Изменяя состав и свойства дисперсной среды, можно проследить за изменением структуры двойного электрического слоя по изменению значения электрокинетического потенциала.
Электрокинетический потенциал ξ-потенциал, дзета-потенциал, часть общего скачкапотенциала на границе двух фаз, определяющая перемещение этих фаз приэлектрокинетических явлениях. Общий скачок потенциала припересечении межфазной границы в дисперсных системах обусловлен существованием двойногоэлектрического слоя.
Э. п. — перепад потенциала по той частидиффузного слоя, в пределах которой жидкость может быть вовлечена в тангенциальное движениеотносительно межфазной поверхности при внешнем воздействии на систему.
Под влиянием сильноадсорбирующихся на поверхности ионов или изменения pH жидкости может произойти перемена знака напротивоположный («перезарядка» поверхности). Э. п. в изоэлектрической точке равен нулю.
14. Кинетическая и агрегативная устойчивость коллоидных систем. Коагуляция и факторы её вызывающие. Правила Шульце-Гарди. Порог коагуляции. защитное действие молекулярных адсорбирующих слоёв.
Кинетическая устойчивость состоит в том, что концентрация коллоидных растворов одинакова по всему объему системы и не изменяется во времени. Влению седиментации (осаждению) противодействует тепловое движение частиц дисперсной фазы – Броуновское движение.
Агрегативная устойчивость – препятствует слипанию одноименно-заряженных частиц, которое ведет к агрегации и выпадению осадка.
Седиментальная устойчивость – обусловлена размерами частиц и способностью их к оседанию под силой тяжести.
Коагуляция – процесс объединения коллоидных частиц (слипание) с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости и оседание их под силой тяжести.
В результате коагуляции укрупненные частицы дисперсной фазы легко седиментируют, и происходит расслоение системы. Таким образом, причиной коагуляции является потеря агрегативной устойчивости коллоидным раствором, а следствием коагуляции – уменьшение его седиментационной устойчивости.
Факторы, вызывающие коагуляцию:
- Нагревание
- Охлаждение
- Замораживание
- Механическое встряхивание
- Ультрозвуковое воздействие
- Добавление электролитов
Порог коагуляции – минимальная концентрация электролита, которую надо добавить к 1 л золю, чтобы вызвать явную коагуляцию (заметную на глаз) – помутнение раствора или изменение его окраски.
Величину, обратную порогу коагуляции, называют коагулирующим действием. Коагулирующее действие электролитов на коллоидные растворы с ионным стабилизатором подчиняется правилу Шульце – Гарди: «Коагуляцию золей вызывают любые ионы, которые имеют знак заряда, противоположный заряду гранул. Коагулирующая способность ионов тем сильнее, чем выше заряд иона-коагулянта». Коагулирующее действие иона-коагулянта прямо пропорционально его заряду в шестой степени: = f (z6).
Дата публикования: 2015-10-09; Прочитано: 4325 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
