 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Первое начало термодинамики. Удельная и молярная теплоемкости
|
|
Внутренняя энергия системы может изменяться в результате различных процессов, например совершения над системой работы, либо теплообмена системы с окружающей средой.
При взаимодействии тел происходит переход энергии из одного вида в другой, а также обмен механической и внутренней энергией. При нагревании газа под поршнем энергия теплового движения молекул переходит в механическую энергию движения поршня. При соприкосновении тел передается их внутренняя энергия, энергия теплового движения молекул. При этих превращениях соблюдается закон сохранения и превращения энергии, получивший название первого начала термодинамики:
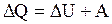 (19)
(19)
количество теплоты 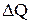 , переданное системе, идет на изменение ее внутренней энергии
, переданное системе, идет на изменение ее внутренней энергии 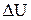 и на совершение системой работы
и на совершение системой работы 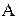 .
.
Количество теплоты 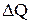 считается положительным, если тепло передается из окружающей среды данной системе, механическая работа
считается положительным, если тепло передается из окружающей среды данной системе, механическая работа 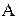 считается положительной, если система производит работу над окружающими телами.
считается положительной, если система производит работу над окружающими телами.
Первое начало термодинамики в дифференциальной форме:
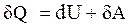 ,
,
где 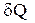 - бесконечно малое количество теплоты (не является полным дифференциалом),
- бесконечно малое количество теплоты (не является полным дифференциалом), 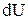 - бесконечно малое изменение внутренней энергии системы (полный дифференциал),
- бесконечно малое изменение внутренней энергии системы (полный дифференциал), 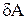 - элементарная работа (не является полным дифференциалом).
- элементарная работа (не является полным дифференциалом).
Согласно (19), единицы измерения количества теплоты в СИ: 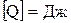 .
.
Удельная теплоемкость вещества – величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К:
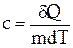 .
.
Молярная теплоемкость - величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К:
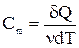 . (20)
. (20)
В системе СИ: 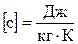 ,
, 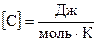 .
.
Связь удельной и молярной теплоемкости:
 ,
,
где 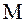 - молярная масса вещества.
- молярная масса вещества.
Дата публикования: 2015-09-17; Прочитано: 444 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
