 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Контрольні завдання. 261. Як зміниться швидкість реакції
|
|
261. Як зміниться швидкість реакції
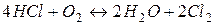 ,
,
яка відбувається в газовій фазі, якщо:
а) збільшити концентрацію  втричі;
втричі;
б) зменшити тиск удвічі?
Відповідь: а) збільшиться в 3
рази;
б) зменшиться в 32 рази.
262. Як зміниться швидкість реакції
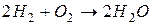 ,
,
якщо: а) концентрацію 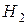 зменшити удвічі,
зменшити удвічі,
б) концентрацію  збільшити удвічі?
збільшити удвічі?
Відповідь: а) зменшиться у 4 рази;
б) збільшиться удвічі.
263. У системі  концентрацію
концентрацію 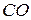 збільшили від 0,3 до 1,2 моль/л, а концентрацію
збільшили від 0,3 до 1,2 моль/л, а концентрацію  - від 0,2 до 0,6 моль/л. У скільки разів збільшилася швидкість прямої реакції?
- від 0,2 до 0,6 моль/л. У скільки разів збільшилася швидкість прямої реакції?
Відповідь: у 12 разів.
264. У скільки разів слід збільшити тиск, щоб швидкість утворення  відповідно до реакції
відповідно до реакції  збільшилася в 1000 разів?
збільшилася в 1000 разів?
Відповідь: у 10 разів.
265. Як зміниться швидкість реакції 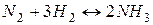 при збільшенні тиску в 3 рази?
при збільшенні тиску в 3 рази?
Відповідь: збільшиться у 81 раз.
266. Як зміниться швидкість прямої реакції 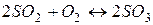 при збільшенні об’єму системи втричі?
при збільшенні об’єму системи втричі?
Відповідь: зменшиться у 27 разів.
267. Як зміниться швидкість прямої реакції 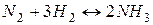 при зменшенні об’єму системи в 3 рази?
при зменшенні об’єму системи в 3 рази?
Відповідь: збільшиться у 81 раз.
268. Як зміниться швидкість прямої реакції 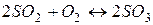 при збільшенні тиску в системі втричі?
при збільшенні тиску в системі втричі?
Відповідь: збільшиться в 27 разів.
269. Як зміниться швидкість прямої реакції 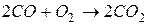 при зменшенні об’єму системи втричі?
при зменшенні об’єму системи втричі?
Відповідь: збільшиться в 27 разів.
270. Як зміниться швидкість прямої реакції  при збільшенні тиску в системі в чотири рази?
при збільшенні тиску в системі в чотири рази?
Відповідь: збільшиться в 64 рази.
271. Вказати гетерогенну систему і написати вираз для швидкості прямої реакції:
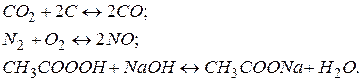
272. Як зміниться швидкість реакції

при розведенні розчину вдвічі?
Відповідь: зменшиться в 4 рази.
273. Як зміниться швидкість реакції
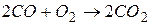 ,
,
якщо: а) концентрацію СО знизити вдвічі, б) концентрацію О 2 збільшити вдвічі?
Відповідь: а) зменшиться у 4 рази;
б) збільшиться удвічі.
274. Визначити швидкість реакції

у початковий момент, якщо константа швидкості 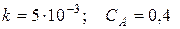 моль/л,
моль/л,
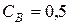 моль/л.
моль/л.
Відповідь: 0,0004 моль/л·с.
275. Як зміниться швидкість реакції
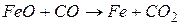 ,
,
якщо збільшити концентрацію СО втричі?
Відповідь: збільшиться в 3 рази.
276. Визначити початкову швидкість реакції
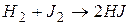 ,
,
якщо 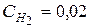 моль/л;
моль/л;  моль/л; константа швидкості k =0,16.
моль/л; константа швидкості k =0,16.
Відповідь: 1,28·10-4 моль/(л·с).
277. Як зміниться швидкість прямої реакції
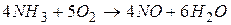 ,
,
якщо збільшити концентрацію О 2 вдвічі?
Відповідь: збільшиться в 32 рази.
278. Від яких факторів залежить швидкість хімічної реакції?
279. Яка система називається гомогенною, а яка – гетерогенною? Навести приклади.
280. Дати визначення швидкості реакції. Як впливає на визначення швидкості реакції гомогенність або гетерогенність системи?
281. У скільки разів зросте швидкість реакції, якщо температуру підвищити від 500С до 900С? Температурний коефіцієнт реакції дорівнює 2,5.
Відповідь: у 39 разів.
282. Як зміниться швидкість реакції, що відбувається в газовій фазі, якщо температуру підвищити на 400С? Температурний коефіцієнт реакції дорівнює 2.
Відповідь: зросте в 16 разів.
283. Як зміниться швидкість реакції, якщо температуру в системі знизити на 500С? Температурний коефіцієнт швидкості реакції дорівнює 2.
Відповідь: зменшиться в 32 рази.
284. На скільки градусів треба підвищити температуру реакції, щоб швидкість її збільшилася у 81 раз? Температурний коефіцієнт швидкості реакції дорівнює 3.
Відповідь: на 400.
285. Визначити температурний коефіцієнт швидкості реакції, якщо швидкість реакції збільшилася в 64 рази з підвищенням температури на 600С.
Відповідь: 2
286. На скільки градусів слід підвищити температуру в системі, щоб швидкість реакції зросла в 39 разів, якщо температурний коефіцієнт швидкості реакції становить 2,5?
Відповідь: на 400.
287. При підвищенні температури на 500 швидкість реакції зросла в 1200 разів.
Визначити температурний коефіцієнт швидкості реакції.
Відповідь: 4,13.
288. Визначити температурний коефіцієнт швидкості реакції, якщо константа швидкості її при 1200С становить 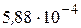 , а при 1700С -
, а при 1700С -  .
.
Дата публикования: 2015-09-18; Прочитано: 2311 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
