 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Опыт №2
|
|
Зависимость скорости реакции от температуры:
Налить в одну пробирку 10мл раствора Na2S2O3, в другую 10 мл раствора H2SO4. Обе пробирки закрепить зажимами с деревянными рукоятками и опустить в водяной термостат ТС-24А. После выдержки пробирок в термостате при температуре t1 в течение 5-7 мин слить вместе содержимое обеих пробирок, отметив время 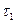 от момента сливания до помутнения раствора.
от момента сливания до помутнения раствора.
Проделать аналогичные опыты при температурах t2=t1+100 и t3=t2+100. Температура t1 задается преподавателем.
Результаты наблюдений (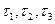 ) при температурах t1,t2,t3 записываем в таблицу №2.
) при температурах t1,t2,t3 записываем в таблицу №2.
Во время работы с термостатом запрещается:
1) работать без заземления термостата;
2) вскрывать коробку с электрическими переключателями;
3) опускать руки в термостат при включенной мешалке.
2.2 Экспериментальные результаты работы:
Таблица №1
| Номер задания | Номер опыта | Объем, мл | Концентрация
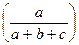
| Время
 c c
| Относительная скорость реакции | |
| Na2S2O3 + H2O (a) (b) | H2SO4 (c) | |||||
| 5 + 5 10 + 10 15 + 15 | 0,33 0,4 0,43 | t1=79 t2=64 t3=60 | t1/t2=1,24 t1/t3=1,31 | |||
| 5 + 10 10 + 5 15 + 0 | 0,25 0,5 0,75 | t1=109 t2=61 t3=39 | t1/t2=1,79 t1/t3=2,79 | |||
| 10 + 10 15 + 5 20 + 0 | 0,4 0,6 0,8 | t1=68 t2=57 t3=37 | t1/t2=1,19 t1/t3=1,84 |
Скорость реакции считаем в относительных единицах, при этом за единицу принимается скорость для наименьшей концентрации Na2S2O3.
Таблица №2
| Номер опыта | Объем, мл | Температура t, 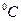
| Время
 с с
| Относительная скорость реакции, 
| |
| Na2S2O3 | H2SO4 | ||||
| t1=20 t2=30 t3=40 | t1=37 t2=26 t3=14 | t1/t2=1,42 t1/t3=2,64 |
Скорость реакции считаем в относительных единицах, при этом за единицу принимается скорость для начальной температуры t1.
2.3 Обработка результатов:
Скорость гомогенной реакции:
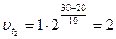
Энергия активации:

с (концентрация)
Заключение
Вывод:
Мы изучили влияние концентрации реагирующих веществ и температуры на скорость гомогенной химической реакции; выяснили, что действительно согласно закону действия масс при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ.
График (сделан в “Paint” схематически!!! по 3 заданию) 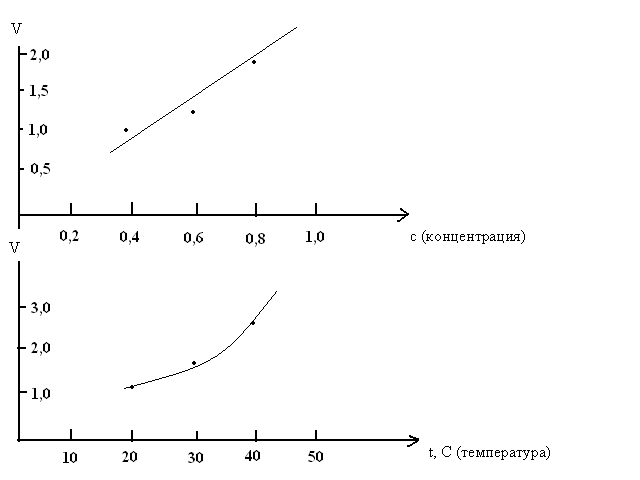
Дата публикования: 2015-07-22; Прочитано: 148 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
