 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Опыт №1
|
|
Содержание работы
2.1 Методика эксперимента:
Для исследования зависимости скорости реакции от концентрации и температуры используется реакция взаимодействия серной кислоты H2SO4 и тиосульфата натрия Na2S2O3. Эта реакция протекает в две стадии:
1) Na2S2O3 + H2SO4 = H2S2O3 + Na2SO4,
2) H2S2O3 = H2O + SO2  + S
+ S  .
.
Экспериментально доказано, что первая стадия протекает с большей скоростью. Скорость всей реакции в целом определяется скоростью второй (медленной) стадии:
 .
.
Поскольку концентрация H2S2O3 в растворе прямо пропорциональна концентрации Na2S2O3, скорость реакции можно рассматривать как:
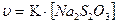 .
.
Опыт №1
Зависимость скорости реакции от концентрации Na2S2O3:
В три большие пробирки налить 2%-ный раствор Na2S2O3 и воду. Затем в три маленькие пробирки налить по 5 мл 2%-ного раствора H2SO4.
В первую большую пробирку с раствором Na2S2O3 прилить 5мл раствора H2SO4 (из маленькой пробирки) и замерить секундомером, через сколько секунд 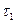 после слияния растворов наблюдается появление серы (помутнение раствора). С последующими пробирками проделываем аналогичные опыты, замеряем время
после слияния растворов наблюдается появление серы (помутнение раствора). С последующими пробирками проделываем аналогичные опыты, замеряем время  и
и 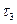 .
.
Результат трех измерений (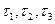 ) записываем в таблицу №1.
) записываем в таблицу №1.
Дата публикования: 2015-07-22; Прочитано: 168 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
