 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Железо является хорошим комплексообразователем
|
|
Известны комплексы железа, содержащие в качестве лиганда группу NO, например, [Fe(CN)5NO]2–, [Fe(NO)4]. Установлено, что в этих соединениях группа NOнесет отрицательный заряд. Образование нитрозильного комплекса железа используется для обнаружения монооксида азота: [Fe(H2O)6]SO4 + NO 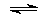 [Fe(H2O)5(NO)]SO4 + H2O
[Fe(H2O)5(NO)]SO4 + H2O
В результате этой реакции появляется характерное бурое окрашивание. Качественной реакцией на катион железа(III) является взаимодействие с тиоцианат-ионом: [Fe(H2O)6]3+ + nNCS– 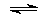 [Fe(H2O)6–n(NCS)n]3–n + nH2O
[Fe(H2O)6–n(NCS)n]3–n + nH2O
Образуется смесь тиоциантных комплексов (n = 3–6), имеющих ярко-красный цвет. Малоустойчивые тиоцианатные комплексы железа(III) легко разрушаются в присутствии лигандов, образующих более прочные комплексы, например, фторид ионов.
Большое практическое значение имеют комплексы железа с анионами ортофосфорной кислоты, которые образуются, когда ржавчина с поверхности металлического железа удаляется водным раствором кислоты. Появившиеся в кислотной среде аквакатионы железа вступают во взаимодействие с имеющимися в растворе анионами H2PO4–, HPO42– и PO43–, в результате образуется ряд комплексов, среди которых преобладает [Fe(H2PO4)4]–. В его состав входят два бидентатных и два монодентатных лиганда H2PO4–. В меньшей степени образуются [Fe(HPO4)4]3– и [Fe(PO4)4]6–.
Особой устойчивостью отличаются цианокомплексы железа. Комплексы железа K4[Fe(CN)6]·3H2O и K3[Fe(CN)6] имеют тривиальные названия «желтая» и «красная кровяные соли».
Ферраты – соли не существующей в индивидуальном состоянии «железной» кислоты – тетраоксоферрата(VI) водорода H2FeO4, – окрашивающей водный раствор в красно-фиолетовый цвет. Водные растворы H2FeO4неустойчивы и при хранении постепенно разлагаются, особенно при нагревании, с выделением метагидроксида железа FeO(OH) и кислорода O2:
4H2FeO4 = 4FeO(OH) + 3O2 + 2H2O.
Дата публикования: 2015-07-22; Прочитано: 582 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
