 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Химико-технологические критерии ХТП
|
|
Об эффективности любого технологического процесса судят по следующим экономическим показателям:
- прибыль;
- рентабельность;
- себестоимость;
- производительность труда и т.п.
Но эти показатели не отражают химическую или физико-химическую сущность явлений, происходящих в химических аппаратах.
Для характеристики ХТП используют следующие показатели:
ХА – степень превращения;
ФR – выход продукта;
φ– полную или интегральную селективность;
φ' – мгновенную или дифференциальную селективность;
П – производительность;
Р – мощность;
I – интенсивность;
τK – время контактирования;
S – объемную скорость.
Степень превращения – это доля исходного реагента, использованного на химическую реакцию.
Степень превращения реагента показывает, насколько полно в ХТП используется сырье.
Возьмем произвольно в качестве участника реакции вещество Ј, следовательно, степень превращения:
 , (2.1)
, (2.1)
где nJ,0 – количество реагента J в исходной реакционной смеси;
nJ – количество реагента J в исходной реакционной смеси, выходящей из реактора;
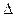 nJ – изменение количества реагента J в ходе химической реакции.
nJ – изменение количества реагента J в ходе химической реакции.
Чаще всего в химической реакции участвуют несколько реагентов, следовательно, для каждого из них можно определить степень превращения. Рассмотрим простую необратимую реакцию aA + bB = = rR + sS.
Степень превращения реагентов А и В:
 ; (2.2)
; (2.2)
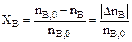 . (2.3)
. (2.3)
Изменение количества вещества в ходе химической реакции связано соотношениями:
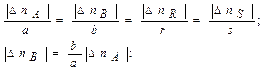
 (2.4)
(2.4)
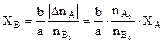 . (2.5)
. (2.5)
Уравнение позволяет рассчитывать неизвестную степень превращения одного реагента, зная степень превращения другого. Зная степени превращения реагентов, можно определить и количество продукта:
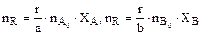 . (2.6)
. (2.6)
Если реакция протекает без изменения объема, то количество реагентов и продуктов можно заменить молярными концентрациями:
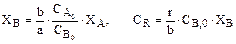 . (2.7)
. (2.7)
Если  , т.е. реагенты А и В взяты для проведения реакции в стехиометрическом соотношении (количества реагентов А и В относятся между собой как соответствующие этим веществам стехиометрические коэффициенты в уравнении реакции), то ХА = ХВ.
, т.е. реагенты А и В взяты для проведения реакции в стехиометрическом соотношении (количества реагентов А и В относятся между собой как соответствующие этим веществам стехиометрические коэффициенты в уравнении реакции), то ХА = ХВ.
Если 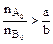 , т.е. реагент А взят в избытке по отношению к реагенту В, то ХА < ХВ.
, т.е. реагент А взят в избытке по отношению к реагенту В, то ХА < ХВ.
Если  , т.е. реагент B взят в избытке по отношению к реагенту A, то ХА > ХВ.
, т.е. реагент B взят в избытке по отношению к реагенту A, то ХА > ХВ.

 ;
; 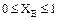 . (2.8)
. (2.8)
Если меняется объем реакционной смеси, то в расчетах приходится учитывать значение относительного изменения объема реакционной смеси:
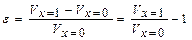 , (2.9)
, (2.9)
где Vx=1 – объем реакционной смеси при степени превращения, равной единице;
Vx=0 – объем реакционной смеси в начале химической реакции.
Основная масса химических реакций – обратимые, следовательно, конечное количество реагента будет определяться условиями равновесия.
Рассмотрим простую обратимую реакцию aA + bB  rR + sS:
rR + sS:
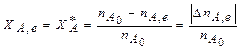 , (2.10)
, (2.10)
где nA,e – количество реагента в условиях равновесия;
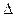 nA,e – изменение количества реагента к моменту наступления равновесия (максимально возможное при данных условиях осуществления химической реакции).
nA,e – изменение количества реагента к моменту наступления равновесия (максимально возможное при данных условиях осуществления химической реакции).
Равновесное количество продукта можно определить:


 . (2.11)
. (2.11)
Равновесные степени превращения взаимосвязаны:
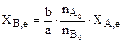 . (2.12)
. (2.12)
Если объем реакционной смеси постоянная величина, то можно использовать молярные концентрации:
 ; (2.13)
; (2.13)
 ; (2.14)
; (2.14)
 . (2.15)
. (2.15)
Выход продукта – это отношение реально полученного количества продукта к максимально возможному его количеству, которое могло бы быть получено при данных условиях проведения химической реакции.
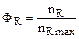 (2.16)
(2.16)
Из определения следует, что
 .
.
Выход продукта зависит от типа реакции.
Рассмотрим простую необратимую реакцию aA + bB = rR + sS.
Максимально возможное количество продукта R в такой реакции будет получено, если весь реагент А (nA,0) вступит в реакцию nRmax = r/a nA,0. Следовательно,
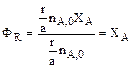 ; (2.17)
; (2.17)
 , (2.18)
, (2.18)
т.е. выход продукта и степень превращения совпадают.
Рассмотрим простую обратимую реакцию aA + bB  rR + sS.
rR + sS.
Для такой реакции максимально возможное количество продукта R определяется как равновесное количество продукта R при данных условиях осуществления реакции (температура, давление, соотношение начальных концентраций реагентов). Отсюда
 ; (2.19)
; (2.19)
 . (2.20)
. (2.20)
Таким образом, для обратимых реакций выход продукта равен доле, которую составляет реально достигаемая степень превращения от равновесной для данных условий проведения реакции.
Рассмотрим параллельные и последовательные реакции:
a1A + b1B = rR + sS (целевая реакция);
a2A + b2B = xX + yY (побочная реакция).
Максимально возможное количество продукта R будет получено в том случае, если весь исходный реагент А будет расходоваться на целевую реакцию
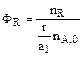 . (2.21)
. (2.21)
Следует помнить, что выразить величину nR через степень превращения и начальное количество реагента А в случае сложной реакции нельзя, т.к. расходование реагента А происходит не только в целевом направлении, но и в побочном. Так же будет выглядеть и выражение для выхода целевого продукта R для последовательных реакций, например, реакций типа аА 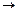 rR
rR 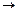 sS.
sS.
При протекании обратимых параллельных и последовательных реакций максимально возможным количеством целевого продукта будет то количество R, которое было бы получено, если бы реагент А расходовался только на целевую реакцию, и в момент равновесия продуктов побочных реакций не было бы.
Таким образом, для сложных реакций
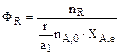 . (2.22)
. (2.22)
Полная или интегральная селективность φ – это отношение количества исходного реагента, пошедшего на целевую реакцию, к количеству реагента, пошедшего на целевую реакцию и побочное взаимодействие:
 , (2.23)
, (2.23)
где 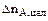 – количество реагента А, пошедшего на целевую реакцию;
– количество реагента А, пошедшего на целевую реакцию;
 – количество реагента А, пошедшего на целевую реакцию и побочное взаимодействие.
– количество реагента А, пошедшего на целевую реакцию и побочное взаимодействие.
По определению 
Для необратимой реакции выход продукта будет равен
 . (2.24)
. (2.24)
А для обратимой реакции
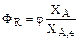 . (2.25)
. (2.25)
Высокое значение выхода продукта достигается только при высоких значениях степени превращения и полной селективности.
Мгновенная, или дифференциальная, селективность φ' – это отношение скорости расходования реагента на целевую реакцию к скорости расходования реагента на целевую реакцию и побочное взаимодействие:

 , (2.26)
, (2.26)
где  – скорость расходования реагента А на целевую реакцию;
– скорость расходования реагента А на целевую реакцию;
 – скорость расходования реагента А (на целевую реакцию и побочное взаимодействие).
– скорость расходования реагента А (на целевую реакцию и побочное взаимодействие).
По определению 0 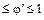 .
.
эффективности целевой реакции по сравнению с побочными взаимодействиями.
Производительность – это количество продукции, полученное в единицу времени:
 ;
;  , (2.27)
, (2.27)
где СR – концентрация продукта;
υ – объемный расход реакционной смеси.
Мощность – максимальная производительность аппарата, машины, ХТС:
P = Пmax. (2.28)
Интенсивность – это производительность аппарата, отнесенная к какой-либо величине, характеризующей размеры аппарата (объему, площади поперечного сечения и т.д.):
I = П/А. (2.29)
где А – «живое» сечение аппарата.
Интенсивность позволяет сравнивать различные аппараты для проведения одного и того же ХТП.
Время контактирования (соприкосновения) – отношение свободного объема катализатора к объемному расходу реакционной смеси:
 , (2.30)
, (2.30)
где 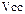 – свободный объем катализатора;
– свободный объем катализатора;
υ – объемный расход реакционной смеси.
На практике чаще всего пользуются фиктивным временем контактирования:
 , (2.31)
, (2.31)
где Vкат – объем слоя катализатора.
Объемная скорость – это величина, обратная 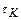 , и представляет собой
, и представляет собой
 . (2.32)
. (2.32)
Объемная скорость – это объемный расход, приходящийся на единицу объема катализатора.
Влияние времени контактирования (объемной скорости) однотипно для многих каталитических реакций. С увеличением времени 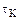 выход продукта простой каталитической реакции растет.
выход продукта простой каталитической реакции растет.
Дата публикования: 2014-10-07; Прочитано: 1502 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
