 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Способы получения солей
|
|
Известно большое число реакций, приводящих к образованию солей. Приведем наиболее важные из них.
1. Взаимодействие кислот с основаниями (реакция нейтрализации):
NаОН + НNO3 = NаNO3 + Н2О
Al(OH)3 + 3НС1 = AlCl3 + 3Н2О
2. Взаимодействие металлов с кислотами:
Fе + 2HCl = FeCl2 + Н2
Zn + Н2SО4 разб.= ZnSO4 + Н2
3. Взаимодействие кислот с основными и амфотерными оксидами:
СuO + Н2SO4 = СuSO4 + Н2О
ZnO + 2HCl = ZnСl2 + Н2О
4. Взаимодействие кислот с солями:
FeCl2 + H2S = FeS¯ + 2HCl
AgNO3 + HCI = AgCl¯ + HNO3
Ba(NO3)2 + H2SO4 = BaSO4¯ + 2HNO3
5. Взаимодействие растворов двух различных солей:
BaCl2 + Na2SO4 = ВаSO4¯ + 2NаСl
Pb(NO3)2 + 2NaCl = РbС12¯ + 2NaNO3
6. Взаимодействие оснований с кислотными оксидами (щелочей с амфотерными оксидами):
Са(ОН)2 + СО2 = СаСО3¯ + Н2О,
2NаОН(тв.) + ZnO 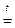 Na2ZnO2 + Н2О
Na2ZnO2 + Н2О
7. Взаимодействие основных оксидов с кислотными:
СаO + SiO2 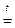 СаSiO3
СаSiO3
Na2O + SO3 = Na2SO4
8. Взаимодействие металлов с неметаллами:
2К + С12 = 2КС1
Fе + S 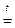 FеS
FеS
9. Взаимодействие металлов с солями.
Cu + Hg(NO3)2 = Hg + Cu(NO3)2
Pb(NO3)2 + Zn = Рb + Zn(NO3)2
10. Взаимодействие растворов щелочей с растворами солей
CuCl2 + 2NaOH = Cu(OH)2↓+ 2NaCl
NaHCO3 + NaOH = Na2CO3+ H2O
Дата публикования: 2014-10-19; Прочитано: 807 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
