 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Гліцерин
|
|
Єдиний практично важливий представник трьохатомного спирту. Сиропоподібна солодка рідина, без кольору, добре розчинна у воді. Водні розчини гліцерину замерзають при низькій температурі.
Гліцерин широко розповсюджений у природі, є основним спиртом, приймає участь у будові молекул різних груп ліпідів. У промисловості гліцерин добувають гідролізом ацилгліцеринів
Гліцерин широко використовується в багатьох галузях промисловості. Основна його кількість розходується для добування похідних - гліфталевих смол, нітрогліцерину.
У харчовій промисловості гліцерин використовують для приготування лікерів та безалкогольних напоїв, у паперовій та шкіряній промисловості - для збереження матеріалів від висихання. Він входить до складу багатьох косметичних препаратів і широко використовується як пом'ягчуюча шкіру речовина
Карбонільні сполуки містять у молекулі карбонільну групу 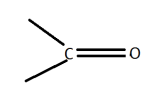 . Карбонільні сполуки поділяють на альдегіди і кетони.
. Карбонільні сполуки поділяють на альдегіди і кетони.
Альдегіди. У молекулах альдегідів карбонільна група сполучена з вуглеводневим радикалом і атомом водню (або з двома атомами водню), тобто загальна формула цих сполук R – COH.
Номенклатура. Назви альдегідів за замісниковою номенклатурою згідно з правилами IUРАК будують з назви відповідного вуглеводню з додаванням закінчення -аль. Перед коренем назви записують бічні замісники, зазначаючи їх положення і кількість. Нумерацію атомів вуглецю починають з вуглецевого атома карбонільної групи. Приклади:
4 3 2 1 5 4 3 2 1
СН2—СН2—СН2—СOH; СН3—СН—СН—СН2—СOH;
Бутаналь │ │
СН3 СН3
3,4 Диметилпентаналь
Для альдегідів широко використовують тривіальні назви, які аналогічні назвам відповідних органічних кислот. У табл. наведено назви за замісниковою номенклатурою та тривіальні назви деяких насичених альдегідів.
| Назва | ||
| Формула | ||
| За замісниковою | Тривіальна | |
| Номенклатурою | ||
| НСНО | Метаналь | Формальдегід, мураши |
| ний альдегід | ||
| СН3—СНО | Етаналь | Адетальдегід, оцтовий Альдегід |
| СН3—СН2 —СНО | Пропаналь | Пропіоновий альдегід |
| СН3—СН2 —СН2 —СНО | Бутаналь | Масляний альдегід |
| СН3—СН(СН3)—СНО | 2-Метил пропаналь | Ізомасляний альдегід |
| СН3—(СН2)3—СНО | Пентаналь | Валеріановий альдегід |
| СН3—СН(СН3)—СН2-СНО | 3 Метил бутаналь | Ізовалеріановий альдегід |
| СН3—С(СН3)2-СНО | 2,2-Диметил- | Триметилоцтоєий альдегід |
| пропаналь |
Властивості. Перший член гомологічного ряду насичених альдегідів НСНО — безбарвний газ, кілька наступних альдегідів - рідини. Вищі альдегіди - тверді речовини.
Хімічні властивості альдегідів.
1. Реакції приєднання. Альдегіди легко приєднують ціановодень НСN і гідросульфіт натрію NаНSО3:
CN
│
CH3COH + HCN → CH3 – C – OH
│
H
OH
│
CH3COH + NаНSО3 → CH3 – C – SО3Na
│
H
Продукти приєднання NaНSО3 - кристалічні речовини, розчинні у воді. При нагріванні з кислотами вони розпадаються з утворенням вихідного альдегіду. Тому останню реакцію використовують для очистки альдегідів.
При наявності нікелевих або платинових каталізаторів альдегіди приєднують водень і відновлюються до первинних спиртів, наприклад:
СН3—СН2—СOH + H2 → СН3—СН2—СН2ОН
Приєднуючи спирти, альдегіди утворюють сполуки, що мають назву ацетaлів. Реакція відбувається при наявності кислот:
OC2H5
│
СН3—СН2—СOH + 2C2H5OH 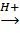 СН3—СН2—СH + H2O
СН3—СН2—СH + H2O
│
OC2H5
Ацеталі - це прості ефіри двохатомного спирту. Вони легко гідролізуються з утворенням вихідних речовин.
2. Окислення. Під час окислення альдегідів, яке відбувається дуже легко, утворюються органічні кислоти або їхні солі. Наприклад, під час окислення оцтового альдегіду утворюється оцтова кислота:
СН3COH + [О] → СН3 - СООН
Якісною реакцією на альдегіди є реакція срібного дзеркала - окислення їх аміачним розчином оксиду срібла при нагріванні:
СН3—СН2—СOH +2[Аg(NН3)2]ОН →
O
║
СН3—СН2—С—ONH4 + 2Ag + 3NH3 + H2O
Металічне срібло, яке виділяється, вкриває стінки посудини тонким блискучим шаром.
Альдегіди окислюються також гідроксидом міді (II), який відновлюється до червоно-коричневого оксиду міді (І):
СН3—СH2—СOH + 2Сu(ОН)2 → СН3—СH2—СOOH +Сu2О+2Н2О.
3. Взаємодія з галогенами. Як уже зазначалось, атом водню біля другого вуглецевого атома вуглеводневого ланцюга альдегідів має підвищену рухливість. Під час взаємодії альдегідів з хлором чи бромом цей водневий атом легко заміщується на галоген, наприклад:
СН3—СН2—СOH + Вr2 → СН3—СНВr—СOH + НВr.
Добування. 1.Альдегіди утворюються під час окислення або каталітичного дегідрування (відщеплення водню) первинних спиртів:
СН3—СН2—СН2ОН + [O] → СН3—СН2—СOH + Н2О
Пропанол 1 Пропаналь
Каталітичне дегідрування спирта відбувається при наявності металічної міді.
2.Альдегіди можна добути гідролізом дигалогенопохідних алканів, наприклад:
CH3 – CHBr2 + H2O → CH3COH + 2HBr
3. Альдегіди утворюються під час взаємодії алкенів з оксидом вуглецю (II) і воднем 9(оксосинтез):
СН2=СН2 + СО + Н2 → СН3—CH2COH
Оксосинтез відбувається при наявності каталізаторів - комплексних сполук кобальту під тиском 5-10 МПа.
Кетони
У молекулах кетонів карбонільна група сполучена з двома однаковими або різними вуглеводневими радикалами 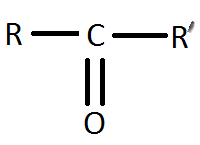 . Найпростішим кетоном є ацетон
. Найпростішим кетоном є ацетон
CH3  CH3
CH3
Номенклатура. Згідно з міжнародною номенклатурою назви кетонів будують з назв відповідного вуглеводню з додаванням закінчення -он. У кінці назви ставлять цифру, що зазначає положення в ланцюгу атома вуглецю, з яким сполучений карбонільний кисень. Нумерацію головного ланцюга починають, як завжди, з найбільш розгалуженого кінця вуглецевого ланцюга. Якщо розгалуженість однакова, то нумерують з того кінця ланцюга, до якого ближче розташована карбонільна група. Назви кетонів за раціональною номенклатурою будують з назв радикалів, сполучених з карбонільною групою з додаванням слова «кетон». Приклади:
1 2 3 4 5
СН3 — С—СН2—СН2 — СН3
║
O Пентанон 2 (метилпропілкетон)
Для деяких кетонів поширені тривіальні назви, наприклад ацетон.
Ізомерія. Ізомерія кетонів зумовлена розгалуженістю вуглецевого ланцюга і різним положенням карбонільного кисню. Розглянемо як приклад ізомери кетону С5Н10О. Для цього кетону можливі два ізомерних кетони, що містять п'ять вуглецевих атомів у головному ланцюгу і один ізомерний кетон з головним ланцюгом з чотирьох атомів вуглецю:
1 2 3 4 5
СН3— СН2— С —СН2—СН3
║
О Пентанон 3
Властивості. Простіші кетони є безбарвними рідинами, які розчиняються у воді. Вищі кетони — тверді речовини. Багато хімічних властивостей, характерних для альдегідів, виявляються і у кетонів.
1. Реакції приєднання. Так само, як і альдегіди, кетони приєднують речовини, що містять нуклеофільні частинки, наприклад ціановодень і гідросульфіт натрію:
CN
│
CH3 – C – CH3 + HCN → CH3 – C – CH3
║ │
O OH
Гідрування кетонів при наявності каталізаторів приводить до утворення вторинних спиртів:
CH3 – C – CH3 + H2 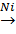 CH3 – CHOH – CH3
CH3 – CHOH – CH3
║
O
На відміну від альдегідів кетони не взаємодіють із спиртами, не вступають у реакції конденсації і полімеризації.
2. Окислення. Кетони окислюються значно важче, ніж альдегіди, і тільки сильними окислювачами. Під час окислення кетонів відбувається розрив (деструкція) вуглецевого ланцюга і утворюється суміш продуктів. Кетони не вступають у реакцію срібного дзеркала.
Добування. 1. Кетони утворюються під час окислення або каталітичного дегідрування вторинних спиртів, наприклад:
СН3-СНОН-СН3 + [О] → СН3-С-СН3 + Н2О
║
O
Каталітичне дегідрування проводять з використанням мідних каталізаторів.
2. Як і альдегіди, кетони можна добути гідролізом дигалогенопохідних алканів. Щоб утворився кетон, обидва атоми галогену у вихідній сполуці повинні знаходитись біля одного (не кінцевого) атома вуглецю:
3. Кетони утворюються внаслідок приєднання води до гомологів ацетилену при наявності каталізаторів — солей ртуті (II).
Дата публикования: 2014-11-18; Прочитано: 2244 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
