 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Спін електрона. Заповнення електронних оболонок і шарів
|
|
180. Як визначається власний механічний момент (спін) електрона Ls?
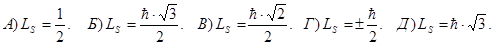
181. Як можна визначити власний (спіновий) магнітний момент електрона pms?
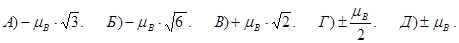
182. Яких значень може набувати проекція спінового магнітного моменту pmsz електрона на напрямок зовнішнього магнітного поля?

183. Як визначається гіромагнітне відношення для власних (спінових) магнітного та механічного моментів електрона pms/Ls.
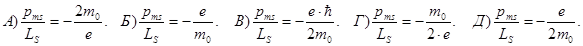
184. Визначте гіромагнітне відношення для власних (спінових) магнітного та механічного моментів електрона pms/Ls.
А)–2,83×1012 Кл/кг. Б)–4,12×1010 Кл/кг. В)–1,76×1011 Кл/кг. Г)–3,82×109 Кл/кг. Д)–9,31×1011 Кл/кг.
185. Проекції власного (спінового) магнітного моменту електрона в атомі pmsz на заданий напрямок можуть набувати значення:
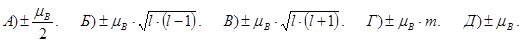
186. До яких мікрочастинок застосовний принцип Паулі?
А) Тільки до протонів. Б) До частинок із цілим спіном. В) Тільки до електронів.
Г) До частинок із напівцілим спіном. Д) Тільки до нейтронів.
187. Яка найбільша кількість електронів N може знаходитись у атомі, якщо для них збігаються значення квантових чисел n, l та m?
А) N =2×(2×l+1). Б) N =2. В) N =(2×l+1). Г) N =(n+1). Д) N =2×n2.
188. Яка найбільша кількість електронів може знаходитись у атомі, якщо для них збігаються значення квантових чисел n, l та m?
А) Шість. Б) Чотири. В) Вісім. Г) Два. Д) Десять.
189. Укажіть максимально можливу кількість електронів N у станах, що визначаються двома квантовими числами - n та l.
А) N= 2×(2l+1). Б) N= (2l+1). В) N= n2. Г) N= (n-1). Д) N= 2×n2.
190. На скільки частин N розділяється у досліді Штерна і Герлаха пучок атомів водню, які знаходяться у 1S -стані?
А) N =0. Б) N =1. В) N =2. Г) N =3. Д) N =4.
191. Якого значення може набувати спінове квантове число електрона S?
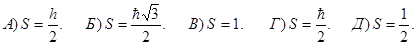
192. Укажіть максимальну кількість електронів N у атомі, які мають однакове значення головного квантового числа n без урахування спіна електрона.
А) N= 2× n 2. Б) N= 2×(2 l +1). В) N= (n -1). Г) N=n 2. Д) N= (2 l +1).
193. Укажіть кратність виродження енергетичного рівня N воднеподібного іону у стані, головне квантове число якого n= 3 без урахування спіна електрона.
А) N= 3. Б) N= 9. В) N= 12. Г) N= 18. Д) N= 24.
194. Укажіть максимальну кількість електронів N у атомі, які мають однакове значення головного квантового числа n з урахуванням спіна електрона.
А) N= 2× n 2. Б) N= 2×(2 l +1). В) N= 2. Г) N=n 2. Д) N= (2 l +1).
195. Визначте кількість електронів N у воднеподібному атомі у енергетичному стані, головне квантове число якого n= 4 (кратність виродження) без урахування спіна.
А) N =8. Б) N =16. В) N =24. Г) N =32. Д) N =4.
196. Визначте кількість електронів N у воднеподібному атомі у енергетичному стані, головне квантове число якого n= 4 (кратність виродження) із урахуванням спіна.
А) N =8. Б) N =24. В) N =16. Г) N =32. Д) N =4.
197. Який із наборів квантових чисел n, l, m та ms відповідає електрону у 1S -стані?
А) 1,0,-1,+  . Б) 1,0,0,-
. Б) 1,0,0,-  . В) 1,1,-1,+
. В) 1,1,-1,+  . Г) 2,0,0,+
. Г) 2,0,0,+  . Д) 1,1,0,
. Д) 1,1,0,  .
.
198. Який із наборів квантових чисел n, l, m та ms відповідає електрону у 2p -стані?
А) 2,1,-2,-  . Б) 2,0,1,-
. Б) 2,0,1,-  . В) 2,0,-1,+
. В) 2,0,-1,+  . Г) 2,0,0,+
. Г) 2,0,0,+  . Д) 2,1,-1,
. Д) 2,1,-1,  .
.
199. Який із наборів квантових чисел n, l, m та ms відповідає електрону у 3d -стані?
А) 3,2,-1,+  . Б) 3,1,0,-
. Б) 3,1,0,-  . В) 3,0,-2,+
. В) 3,0,-2,+  . Г) 3,1,1,+
. Г) 3,1,1,+  . Д) 2,2,-2,
. Д) 2,2,-2,  .
.
200. Який із наборів квантових чисел n, l, m та ms відповідає електрону у 4f -стані?
А) 4,2,-1,+  . Б) 4,3,0,-
. Б) 4,3,0,-  . В) 2,4,-1,+
. В) 2,4,-1,+  . Г) 4,3,4,+
. Г) 4,3,4,+  . Д) 3,3,-2,
. Д) 3,3,-2,  .
.
201. Укажіть вірну електронну конфігурацію для атома азоту (z=7) у основному стані.
А) 1S22S22p2. Б) 1S22S22p6. В) 1S22S22p3. Г) 1S22S22p5. Д) 1S22S22p4.
202. Укажіть вірну електронну конфігурацію для атома фтору (z=9) у основному стані.
А) 1S22S22p2. Б) 1S22S22p63S1. В) 1S22S22p6. Г) 1S22S22p5. Д) 1S22S22p4.
203. Укажіть вірну електронну конфігурацію для атома натрію (z=11) у основному стані.
А) 1S22S22p63S1. Б) 1S22S22p6. В) 1S22S22p63S2. Г) 1S22S22p5. Д) 1S22S22p4.
204. Укажіть вірну електронну конфігурацію для атома алюмінію (z=13) у основному стані.
А) 1S22S22p6. Б) 1S22S22p63S23р1. В) 1S22S22p63S2. Г) 1S22S22p63S23p2. Д) 1S22S22p63S1.
205. Скільки вільних квантових станів існує у електронному L -шарі, що заповнений шістьма електронами?
А) Три. Б) Чотири. В) П¢ять. Г) Один. Д) Два.
206. Скільки вільних квантових станів мають місце у електронному М -шарі, який заповнений одинадцятьма електронами?
А) Тринадцять. Б) Чотири. В) Вісім. Г) Сім. Д) Три.
207. Скільки вільних квантових станів мають місце у електронному N -шарі, який заповнений чотирнадцятьма електронами?
А) Десять. Б) Сім. В) Вісімнадцять. Г) Чотирнадцять. Д) Чотири.
208. Із яких електронних оболонок складається електронний М -шар?
А) S, p, d. Б) S, p, d, f, g. В) S, p. Г) S, p, d, f. Д) S.
209. Із яких електронних оболонок складається електронний N -шар?
А) S, p, d. Б) S, p, d, f. В) S, p. Г) S, p, d, f, g. Д) S.
210. Укажіть головне квантове число n для електронного шару, в якому не може знаходитись понад 18 електронів.
А) П’ять. Б) Чотири. В) Два. Г) Три. Д) Шість.
211. Укажіть головне квантове число n для електронного шару, в якому не може знаходитись понад 32 електронів.
А) П’ять. Б) Шість. В) Два. Г) Три. Д) Чотири.
212. Укажіть головне квантове число n для електронного шару, в якому не може знаходитись понад 50 електронів.
А) П’ять. Б) Чотири. В) Два. Г) Три. Д) Шість.
213. Укажіть кількість електронів у атомі, у якого заповнені К - та L -шари, а також 3S - оболонка.
А) Одинадцять. Б) П’ятнадцять. В) Десять. Г) Дванадцять. Д) Чотирнадцять.
214. Укажіть кількість електронів у атомі, у якого заповнені К - та L -шари, а також 3S - та наполовину 3р -оболонка.
А) Вісімнадцять. Б) П’ятнадцять. В) Десять. Г) Дванадцять. Д) Чотирнадцять.
215. Укажіть кількість електронів у атомі, у якого повністю заповнені К - та L- шари, а також 3S - та 3р -оболонки.
А) Вісімнадцять. Б) П’ятнадцять. В) Чотирнадцять. Г) Дев’ятнадцять. Д) Шістнадцять.
216. Укажіть кількість електронів у атомі, у якого повністю заповнені К - та L- шари, 3S - та 3р -оболонки, а у 3d -оболонці – 2 електрони.
А) Чотирнадцять. Б) П’ятнадцять. В) Двадцять. Г) Дев’ятнадцять. Д) Вісімнадцять.
217. У атомі деякого хімічного елемента повністю заповнені К- та L- електронні шари, а у М -шарі знаходяться 4 електрони?
А) Mg (z=12). Б) Si (z=14). В) Al (z=13). Г) P (z=15). Д) Nе (z=10).
218. У атомі якого хімічного елемента повністю заповнені К- та L- електронні шари?
А) Mg (z=12). Б) Na (z=11). В) Al (z=13). Г) P (z=15). Д) Nе (z=10).
219. У зовнішній електронній 3р -оболонці незбудженого атома деякого хімічного елемента містяться два електрони. Який це атом?
А) Al (z=13). Б) P (z=15). В) Na (z=11). Г) Si (z=14). Д) Mg (z=12).
220. У атомі деякого хімічного елемента повністю заповнені К-, L- та M - електронні шари, а у 4S -оболонці – один електрон. Який це атом?
А) Cu (z=29). Б) Zn (z=30). В) Ni (z=28). Г) Cr (z=24). Д) Fе (z=26).
221. У атомі деякого хімічного елемента повністю заповнені К-, L- та M - електронні шари, а також 4S -оболонка і наполовину 4р -оболонка. Який це атом?
А) Mn (z=25). Б) As (z=33). В) Br (z=35). Г) Zn (z=30). Д) Ni (z=28).
222. Визначте загальну кількість електронів у атомі N, у якого повністю заповнені К-, L- та M - електронні шари, а також 4S -оболонка.
А) N =26. Б) N =24. В) N =30. Г) N =32. Д) N =28.
Дата публикования: 2014-11-18; Прочитано: 646 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
