 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Порядок выполнения работы. 1. Для анализа в коническую колбу отмерить с помощью мерного цилиндра 20 мл анализируемого раствора
|
|
1. Для анализа в коническую колбу отмерить с помощью мерного цилиндра 20 мл анализируемого раствора.
2. Добавить 2-3 капли индикатора – фенолфталеина.
3. В приготовленную заранее бюретку налить 0,1 н раствор HCl. Установить уровень на нулевое деление и по каплям приливать хлороводородную (соляную) кислоту в исследуемый раствор до изменения окраски раствора с малиновой до бесцветной.
4. Записать объем израсходованной на титрование кислоты (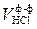 ).
).
5. В раствор, после первого титрования, добавить 2-3 капли раствора метилового-оранжевого и титровать соляной кислотой до изменения цвета с желтого на розовый (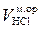 ). Результат занести в таблицу.
). Результат занести в таблицу.
6. Титрование повторить с новыми порциями исследуемого раствора еще три раза, каждый раз не забывая доливать в бюретку кислоту до нулевого уровня.
7. Результаты титрования записать в таблицу.
| № опыта | Эквивалентная конц. кислоты C Э,НCl, моль/л | Объем анализ. р–ра V, мл | Объем р–ра HCl c ф–ф V 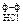 , мл , мл
| Объем р–ра
HCl с м.-ор.
V 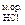 , мл , мл
|
Массу каждого из компонентов анализируемой смеси рассчитать по формулам:
m (NaOH) = 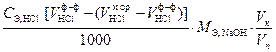 ,
,
m (Na2CO3) =  ,
,
m (NaOH)общ. =  ,
,
где m (NaOH)общ. – общая щелочность раствора, г;
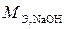 и
и 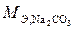 – эквивалентные массы, г/моль;
– эквивалентные массы, г/моль;
Vк – объем всего анализируемого раствора, мл;
Vп – объем анализируемого раствора, взятый для одного титрования, мл;
C Э,НCl – эквивалентная концентрация соляной кислоты, моль/л.
8. По проделанной работе сделать вывод.
Дата публикования: 2014-11-18; Прочитано: 437 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
