 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Электромеханическое сопряжение в мышцах
|
|
Электромеханическое сопряжение - это цикл последовательных процессов, начинающийся с возникновения потенциала действия ПД на сарколемме (клеточной мембране) и заканчивающийся сократительным ответом мышцы.
Нарушение последовательности процессов сопряжения может приводить к патологиям и даже к летальному исходу. Основные этапы этого процесса можно проследить по схеме рис. 7.11.

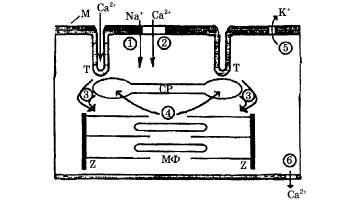
Рис. 7.11. Схема электромеханического сопряжения в кардиомиоците (М - клеточная мембрана-сарколемма, СР - саркоплазматический ретикулум, МФ - миофибрилла, Z - z-диски, Т - Т-система поперечных трубочек); 1 - поступления Na+ и 2 - поступления Са2+ в клетку при возбуждении мембраны, 3 - "кальциевый залп", 4 - активный транспорт Са2+ в СР, 5 - выход из клетки К+, вызывающий реполяризацию мембраны, 6 - активный транспорт Са2+ из клетки
Процесс сокращения кардиомиоцита происходит следующим образом
1 - при подаче на клетку стимулирующего импульса открываются быстрые (время активации 2 мс) натриевые каналы ионы Na+ входят в клетку, вызывая деполяризацию мембраны
2 - в результате деполяризация плазматической мембраны в ней и в Т-трубочках открываются потенциал-зависимые; медленные кальциевые каналы (время жизни 200 мс), и ионы Са2+ поступают из внеклеточной среды, где их концентрация ≈ 2 • 10-3 моль / л, внутрь клетки (внутриклеточная концентрация Са2+ ≈ 10-7 моль / л);
3 - кальций, поступающий в клетку, активирует мембрану СР, являющегося внутриклеточным депо ионов Са2+ (в СР их концентрация достигает ≈ 10-3 моль / л), и высвобождает кальций из пузырьков СР, в результате чего возникает так называемый "кальциевый залп". Ионы Са2+ из СР поступают на актин-миозиновый комплекс МФ, открывают активные центры актиновых цепей, вызывая замыкание мостиков и дальнейшее развитие силы и укорочения саркомера;
4 - по окончании процесса сокращения миофибрилл ионы Са2+ с помощью кальциевых насосов, находящихся в мембране СР, активно заканчиваются внутрь саркоплазматического ретикулума;
5 - процесс электромеханического сопряжения заканчивается тем, что К+ пассивно выходит из клетки, вызывая реполяризацию мембраны;
6 - ионы Са2+ активно выводятся во внеклеточную среду с помощью кальциевых насосов сарколеммы
Таким образом, в кардиомиоците электромеханическое сопряжение идет в две ступени: вначале небольшой входящий поток кальция активирует мембраны СР, способствуя большему выбросу кальция из внутриклеточного депо, а затем в результате этого выброса происходит сокращение саркомера. Описанный выше двухступенчатый процесс сопряжения доказан экспериментально. Опыты показали, что: а) отсутствие потока кальция извне клетки jCa прекращает сокращение саркомеров, б) в условиях постоянства количества кальция, высвобождаемого из СР, изменение амплитуды потока кальция приводит к хорошо коррелирующему изменению силы сокращения. Поток ионов Са2+ внутрь клетки выполняет таким образом две функции: формирует длительное (200 мс) плато потенциала действия кардиомиоцита и участвует в процессе электромеханического сопряжения.
Следует отметить, что не во всех мышечных клетках организма процесс сопряжения происходит, как в кардиомиоците. Так, в скелетных мышцах теплокровных потенциал действия короткий (2-3 мс) и медленный поток ионов кальция в них отсутствует. В этих клетках сильно развита Т-система поперечных трубочек, подходящих непосредственно к саркомерам близко к z-дискам. Изменения мембранного потенциала во время деполяризации через Т-систему передается в таких клетках непосредственно на мембрану СР, вызывая залповое высвобождение ионов Са2+ и дальнейшую активацию сокращения (3, 4, 5).
Общим для любых мышечных клеток является процесс освобождения ионов Са2+ из внутриклеточных депо - саркоплазматического ретикулума и дальнейшая активация сокращения. Ход кальциевого выброса из СР экспериментально наблюдается с помощью люминесцирующего в присутствии ионов Са2+ белка экворина, который был выделен из светящихся медуз.
Задержка начала развития сокращения в скелетных мышцах составляет 20 мс, а в сердечной — несколько больше (до 100 мс).
Яд кураре, которым пользуются охотники Амазонки, парализует жертву как раз благодаря тому, что молукулы этого яда, попав в кровь проникают к рецепторам ацетилхолина и усаживаются на них, так что когда к этим рецепторам приходит сам ацетилхолин, свободных мест уже нет, и процесс передачи сигнала на мышечные сокращения преравается. Аналогично работает белок ботулин, вызывающий одно из опаснейших пищевых отравлений, ботулизм. А вот вирус полиомелита разрушает те нервные волокна, по которым с помощью кальция подаются сигналы на мышечные сокращения, и мышцы, оставшись без употребления, постепенно высыхают. С другой стороны, этот же «кальциевый привод» можно использовать в благодетельных целях. Так, сердечыные больные нуждаются в понижении ритма биений сердца, в противном случае оно при нагрузках будет требовать больше кислорода, чем способны дать сузившиеся из-за атеросклероза сосуды. Этим людям помогают «β-блокаторы» – препараты, которые несколько блокируют кальциевые каналы, тем самым понижая уровень кальция и, соответственно, уменьшая размах сокращений сердечной мышцы.
Перемещения внутри обычных клеток осуществляют другие моторы, и в отличие от миозина их изучение началось в 1985 году, когда Том Рииз и Майкл Шитц открыли первый из них – кинезин. Молекула кинезина по своей форме напоминает молекулу миозина – те же округлые головки на длиной ножке. Двумя головками молекула хватается за поверхность микротрубочки, а к торчащей вверх ножке крепится пузырек с химическими веществами. Под воздействием АТФ молекула изгибается, так что ее передняя головка уходит чуть дальше от задней и в результате хватается за микротрубочку чуть дальше по ходу движения; затем задняя головка вновь подтягивается к передней. Затем этот «силовой толчек» повторяется. В итоге пузырек, сидящий на ножке молекулы, рывками движется по микротрубке. Картина напоминает ползущую по ветке гусеницу. Кинезин способен переносить пузырьки с необходимыми клетке химическими веществами только в одном направлении – от центра клетки к ее переферии, а динеин движется в обратном направлении Микротрубки имеют встроеные в них однонаправленные блочные конструкции (с «головой» и «хвостом»). Пока непонятно, как пузырьки узнают, в какую сторону им двигаться. В 1990 году Ричард Велли открыл еще один вид молекулярного мотора - «динамин». В настоящее время считается, что в клетках действует не менее полусотни переносящих или передвигающих груз молекул работающих по отному принципу – преобразование химической энергии в энергию изменения формы гибкой молекулы, которая за счет этого изменения способна «хватать и перехватывать» некое длинное негибкое внутриклеточное волокно и «ползти» по нему с грузом. Кроме того, молекула динеина соединяется с энергетической молекулой АТФ, происходит нечто вроде натягивания лука – центр динеиновой молекулы выходит вперед, а угол между ее концами уменьшается (как сближаются концы лука). Затем, после выполненной работы, молекула динеина как бы «распрямляется» – происходит «силовой толчок» и один конец смещается относительно другого на 15 нм. Такой механизм был расскрыт под руководством С. Берджесса в 2003 году группой ученых

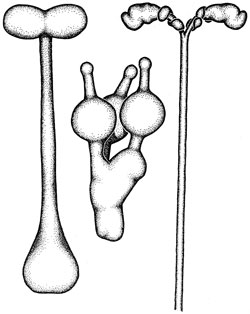
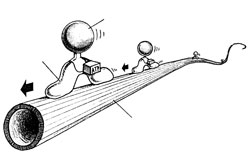
Молекулы осуществляющие функцию движения в нашем теле (а- кинезин, б- динеин, в- миозин). Б) «Молекулярный мотор» кинезина, при помощи которого молекула переносит по микротрубочкам различные вещества.
Потребности работающей мышцы в АТФ удовлетворяются за счет следующих ферментативных реакций:
1. Резерв в виде креатинфосфата. Быстрая регенерация АТФ может быть достигнута за счет переноса фосфатной группы креатинфосфата на АДФ (ADP) в реакции, катализируемой креатинкиназой [2]. Однако и этот мышечный резерв «высокоэргического фосфата» расходуется в течение нескольких секунд. В спокойном состоянии креатинфосфат вновь синтезируется из креатина. При этом фосфатная группа присоединяется по гуанидиновой группе креатина (N-гуанидино-N-метилглицина). Креатин, который синтезируется в печени, поджелудочной железе и почках, в основном накапливается в мышцах. Здесь креатин медленно циклизуется за счет неферментативной реакции [3] с образованием креатинина, который поступает в почки и удаляется из организма.
2 Анаэробный гликолиз. В мышечной ткани наиболее важным долгосрочным энергетическим резервом является гликоген. В покоящейся ткани содержание гликогена составляет до 2% от мышечной массы. При деградации под действием фосфорилазы гликоген легко расщепляется с образованием глюкозо-6-фосфата, который при последующем гликолизе превращается в пируват. При большой потребности в АТФ и недостаточном поступлении кислорода пируват за счет анаэробного гликолиза восстанавливается в молочную кислоту (лактат), которая диффундирует в кровь.
3. Окислительное фосфорилирование. В аэробных условиях образующийся пируват поступает в митохондрии, где подвергается окислению. Окислительное фосфорилирование - наиболее эффективный и постоянно действующий путь синтеза АТФ. Однако этот путь реализуется при условии хорошего снабжения мышц кислородом. Наряду с глюкозой, образующейся при расщеплении мышечного гликогена, для синтеза АТФ используются и другие "энергоносители", присутствующие в крови: глюкоза крови, жирные кислоты и кетоновые тела.
4. Образование инозинмонофосфата [ИМФ (IMP)]. Другим источником быстрого восстановления уровня АТФ является конверсия АДФ в АТФ и АМФ (AMP), катализируемая аденилаткиназой (миокиназой). Образовавшийся АМФ за счет дезаминирования частично превращается в ИМФ (инозинмонофосфат), что сдвигает реакцию в нужном направлении.
Из всех способов синтеза АТФ наиболее продуктивным является окислительное фосфорилирование. За счет этого процесса обеспечиваются потребности в АТФ постоянно работающей сердечной мышцы (миокарда). Вот почему для успешной работы сердечной мышцы обязательным условием является достаточное снабжение кислородом (инфаркт миокарда — это следствие перебоев в поступлении кислорода).
В высокоактивных (красных) скелетных мышцах источником энергии для рефосфорилирования АДФ служит окислительное фосфорилирование в митохондриях. В обеспечении этих мышц кислородом принимает участие миоглобин (Mb) - близкий гемоглобину белок, обладающий свойством запасать кислород. В малоактивных скелетных мышцах, лишенных красного миоглобина и поэтому белых, главным источником энергии для восстановления уровня АТФ является анаэробный гликолиз. Такие мышцы сохраняют способность к быстрым сокращениям, однако они могут работать лишь короткое время, поскольку при гликолизе образование АТФ идет с низким выходом. Спустя некоторое время мышцы истощаются в результате изменения рН в мышечных клетках.
Расщепление гликогена контролируется гормонами. Процесс гликогенолиза стимулируется адреналином (через b-рецепторы) за счет образования цАМФ и активации киназы фосфорилазы. Активация фосфорилазы наступает также при увеличении концентрации ионов Са2+ во время мышечного сокращения.
Дата публикования: 2014-11-04; Прочитано: 3190 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
