 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Строение слитка спокойной стали
|
|
Схема строения слитка спокойной стали приведена на рис. 2.15. Структура слитка состоит из трех зон: наружной мелкозернистой зоны 1, зоны столбчатых кристаллов 2 и зоны равноосных кристаллов 3. Наружная мелкозернистая зона состоит из неориентированных в пространстве мелких кристаллов. Ее образование обусловлено резким перепадом температур: жидкий металл — холодные стенки изложницы. Металл в этой зоне сильно переохлаждается, в нем образуется большое число центров кристаллизации, и он приобретает мелкозернистое строение.
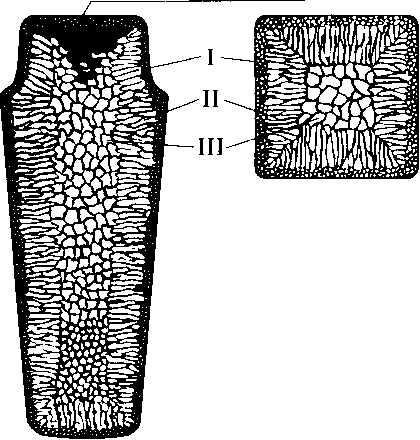
| Усадочная раковина |
| Рис. 2.15. Строение слитка спокойной стали с характерными зонами I — III |
Третья зона — зона равноосных кристаллов. В центре слитка нет определенной направленности отвода теплоты. Здесь зародышами обычно являются различные мелкие твердые частицы, оттесненные при кристаллизации к центру слитка. Относительное распределение в объеме слитка столбчатой и равноосной зон очень важно. В зоне столбчатых кристаллов металл более плотный, но в местах их стыка он имеет малую прочность. Кристаллизация, при которой зоны столбчатых кристаллов стыкуются, называется транскристаллизацией.
Для цветных металлов транскристаллизация полезна, так как металл становится плотнее и при его высокой пластичности трещины при деформации не образуются. Транскристаллизация стали нежелательна, поскольку на стыке двух кристаллов при деформации могут образоваться трещины.
Основными дефектами слитка являются усадочная раковина, усадочная пористость и ликвация. Усадочная пористость обычно образуется вблизи усадочной раковины и по оси слитка. Образование усадочной раковины и усадочной пористости обусловлено тем, что все металлы кроме висмута имеют в твердом состоянии меньший удельный объем, чем в жидком.
Вопросы для контроля
1. Перечислить основные свойства металлов и объяснить их с помощью электронного строения металлов.
2. Какое строение имеют металлы и чем отличаются кристаллические вещества от аморфных.
3. Дать определение кристаллической решетки и кристаллической ячейке и назвать типы кристаллических решеток.
4. Дать определение полиморфизма.
5. Дать объяснение анизотропии кристаллов.
6. Что называется степенью переохлаждения и как она зависит от скорости охлаждения при кристаллизации металлов.
7. Дать определение модифицирования и цель его проведения.
Раздел 2. МЕТОДЫ ИЗУЧЕНИЯ СТРУКТУРЫ И СВОЙСТВ МАТЕРИАЛОВ
Задачей материаловедения является установление взаимосвязи между строением (структурой) материала и его свойствами. Поэтому при исследовании используют как методы для изучения строения материала, так и методы, которые позволяют определять поведение материалов в условиях эксплуатации — это механические, а также физические и химические свойства.
Физические свойства определяют поведение материалов в тепловых, гравитационных, электромагнитных и радиационных полях. К физическим свойствам относятся плотность, теплоемкость, температура плавления, термическое расширение, магнитные характеристики, теплопроводность, электропроводность.
Под химическими свойствами понимают способность материалов вступать в химическое взаимодействие с другими веществами, сопротивляемость окислению, проникновению газов и химически активных веществ. Характерным примером химического взаимодействия среды и металла является коррозия.
Технологические свойства металлов и сплавов характеризуют их способность подвергаться горячей и холодной обработке, в том числе при выплавке, горячем и холодном деформировании, обработке резанием, термической обработке и особенно сварке.
Механические свойства материалов характеризуют их способность сопротивляться деформированию и разрушению под воздействием различного рода нагрузок. Механические нагрузки могут быть статическими, динамическими и циклическими. Кроме того, материалы могут подвергаться деформации и разрушению как при разных температурах, так и в различных, в том числе агрессивных, средах.
Целесообразность применения тех или иных материалов определяется не только их свойствами, но и их стоимостью.
2.1. Упругая и пластическая деформация
Деформацией называется изменение формы и размеров тела под действием напряжений. Деформация, возникающая при сравнительно небольших напряжениях и исчезающая после снятия нагрузки, называется упругой, а сохраняющаяся — остаточной или пластической. При увеличении напряжений деформация может заканчиваться разрушением.
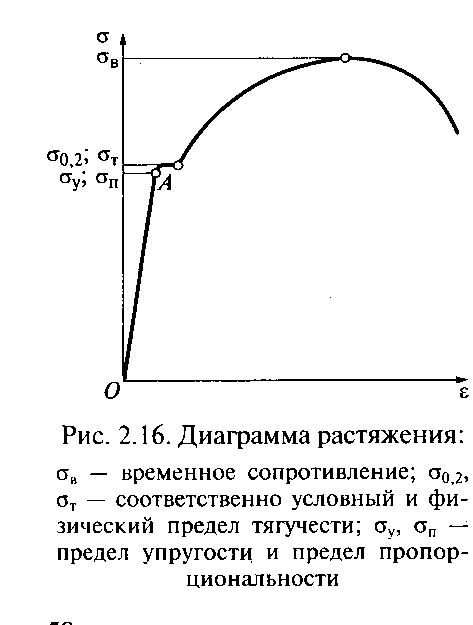
На диаграмме растяжения (рис. 2.16) упругая деформация характеризуется линией OA. Выше точки А нарушается пропорциональность между напряжением σ и деформацией δ. Рост напряжения приводит не только к упругой, но и к пластической деформации.
Упругая и пластическая деформации в своей физической основе принципиально отличаются одна от другой. При упругой деформации происходит обратимое смещение атомов из положений равновесия в кристаллической решетке. Упругая деформация не вызывает заметных остаточных изменений в структуре и свойствах металла. После снятия нагрузки сместившиеся атомы под действием сил притяжения (при растяжении) или отталкивания (при сжатии) возвращаются в исходное равновесное положение, и кристаллы приобретают первоначальную форму и размеры. Упругие свойства материалов определяются силами межатомного взаимодействия.
В основе пластической деформации лежит необратимое перемещение одних частей кристалла относительно других. После снятия нагрузки исчезает лишь упругая составляющая деформации. Пластичность, т.е. способность металлов перед разрушением претерпевать значительную пластическую деформацию, является одним из важнейших свойств металлов. Благодаря плаcтичности осуществляется ОМД. Пластичность позволяет перераспределять локальные напряжения равномерно по всему объему металла, что уменьшает опасность разрушения.
Величина напряжения, необходимого для осуществления пластической деформации, зависит от скорости деформирования и температуры. С увеличением скорости деформирования достижение заданной деформации требует больших напряжений, а при повышении температуры значение необходимых напряжений снижается. Таким образом, пластическая деформация является термически активируемым процессом. При понижении температуры предел текучести большинства металлов растет. Металлы с ГЦК решеткой имеют значительно меньшую зависимость предела текучести от температуры, чем металлы с другими типами решеток.
2.2. Механические свойства и методы их определения
Механические свойства материалов определяют на специальных образцах. В зависимости от условий приложения нагрузки различают статические и динамические испытания. При статических испытаниях нагрузка прилагается медленно и плавно возрастает. При динамических — она прилагается с высокой скоростью. Испытания могут выполняться при нормальной (комнатной) или повышенной температуре.
Наиболее распространенными механическими характеристиками являются: твердость, пределы прочности и упругости, ударная вязкость. Определяют также предел выносливости и предел ползучести.
Предел прочности определяют в испытаниях на растяжение, сжатие, кручение и изгиб.
Механическими называют свойства материала, определяющие его сопротивление действию внешних механических нагрузок.
Прочность металла при статическом нагружении - это свойство, определяющее его способность сопротивляться деформации и разрушению. Стандартными характеристиками прочности являются предел упругости, предел текучести и временное сопротивление.
Пределом упругости называют напряжение, при котором пластическая деформация достигает заданной малой величины, установленной условиями (например 0,005 % - σ0,005).
Предел текучести (условный) - это напряжение, которому соответствует пластическая деформация 0,2 % (σ0,2). Предел текучести физический устанавливают по диаграмме растяжения, если на ней есть площадка текучести.
Временное сопротивление (σв) характеризует максимальное напряжение, предшествующее разрушению образца. Различают напряжения условные и истинные. Условным напряжением называют отношение величины нагрузки к исходному сечению образца; истинным - к сечению, которое образец приобрел к моменту достижения данной нагрузки. Диаграммы растяжения пластичных металлов с условными напряжениями отличаются от диаграмм с истинными напряжениями.
Конструктивную прочность материала характеризует комплекс механических свойств, обеспечивающих надежную и длительную работу в условиях эксплуатации. Конструктивная прочность определяется критериями прочности, надежности и долговечности.
Твердость характеризует свойство поверхностного слоя материала оказывать сопротивление упругой и пластической деформации при местных контактных воздействиях.
Удельные механические свойства (удельная прочность, удельная жесткость) характеризуют эффективность материалов по массе и представляют собой отношение соответствующих характеристик материала к его плотности.
Жаропрочные материалы характеризуются длительной прочностью и ползучестью. Под пределом длительной прочности понимают напряжение, вызывающее разрушение материала при заданной температуре за определенное время. Пределом ползучести называют напряжение, вызывающее заданную скорость деформации при заданной температуре.
Надежностью называют способность материала противостоять хрупкому разрушению. Важными критериями надежности являются пластичность (относительное удлинение - δ, относительное сужение - ψ), вязкость разрушения (К1с), ударная вязкость (КCU, КCV, KCY), хладноломкость.
δ и ψ характеризуют изменения геометрических параметров стандартных образцов при напряжении, вызывающем разрушение.
Кic показывает какой интенсивности достигает напряжение вблизи вершины трещины в момент разрушения.
Ударная вязкость - это сопротивление разрушению при динамических нагрузках.
Хладноломкость определяет влияние снижения температуры на склонность материала к хрупкому разрушению. Порог хладноломкости характеризуется температурой или интервалом температур перехода металла в хрупкое состояние. Хрупкий излом имеет кристаллическое строение. Обычно в изломе можно видеть форму и размер зерен, так как излом происходит без значительной пластической деформации и зерна при разрушении металла не искажаются.
Долговечностью называют способность материала детали сопротивляться развитию постепенного разрушения, обеспечивая ее работоспособность в течение заданного времени.
Одним из критериев долговечности является выносливость, под которой понимают способность материала сопротивляться усталости, или постепенному накоплению повреждений под действием циклически повторяющихся нагрузок. Выносливость зависит от живучести, определяющей продолжительность работы детали от момента зарождения первой макроскопической трещины усталости (размером 0,5... 1,0 мм) до разрушения. Усталостный излом всегда имеет две зоны разрушения: усталостную зону предварительного разрушения с мелкозернистым, часто ступенчато-слоистым строением, иногда с отдельными участками блестящей поверхности, и зону долома, носящую характер вязкого или хрупкого разрушения.
При циклическом нагружении разрушение начинается в местах концентрации напряжений (деформации), локализующихся на различного рода повреждениях поверхностного слоя. Поверхностное упрочнение (химико-термическая обработка, поверхностная закалка, пластическое деформирование) эффективно снижает роль концентраторов, затрудняя деформацию поверхности деталей.
2.3. Методы изучения структуры
Макроскопический анализ (макроанализ) заключается в изучении строения металла невооруженным глазом или при небольших увеличениях (до 30 раз). Это позволяет одновременно наблюдать большую поверхность изделия (в отличие от микроанализа, выполняемого при больших увеличениях).
Макроанализ не позволяет определить всех особенностей строения. Его часто используют в качестве предварительного с целью выявить те участки детали, которые следует подробно изучать с помощью более тонких методов.
Наиболее типичные задачи макроанализа — это изучение:
- видов излома (различают вязкий, хрупкий и другие виды изломов)
- нарушения сплошности металла (наличие трещин, дефектов сварки, пористость и др.);
- строения слитка;
- текстурированной (направленной структуры металла, что позволяет судить о технологии изготовления детали (сварная, штампованная, полученная обработкой резанием)
ликвации, т. е. химической неоднородности металла.
Микроскопический анализ (микроанализ) выполняется при больших увеличениях с помощью металлографического микроскопа (рис. 3.2). Металлы непрозрачны, поэтому изучение структуры выполняется в отраженном свете. Исследования выполняются на специальном объекте — микрошлифе. Исследуемая поверхность микрошлифа должна иметь очень малую шероховатость — быть зеркальной, чтобы получалось правильное отражение. Для изготовления микрошлифа на объекте исследования должна быть обработана плоская поверхность. Ее образуют непосредственно на деталях малых размеров, а из больших деталей вырезается специальный образец. Зеркальной поверхности добиваются путем обработки абразивной шкуркой нескольких номеров, переходя от более грубой к более тонкой, и последующим полированием абразивными или алмазными пастами.
Для выявления структуры применяют травление шлифа растворами кислот или щелочей. При этом выявляется зерно сплавов. Это объясняется тем, что на поверхность шлифа зерна выходят разными металлографическими направлениями и, вследствие анизотропии (неодинаковость свойств в разных направлениях) травятся на разную глубину и выглядят неодинаково окрашенными в поле зрения микроскопа — травящиеся сильнее кажутся более темными. Выявляются разные фазы сплава, так как их свойства также неодинаковы и травление происходит на разную глубину. В поле зрения микроскопа наиболее темными выглядят границы зерен, так как они травятся наиболее сильно из-за скопления несовершенств пo границам, поэтому отражение от границ рассеивается, и не попадает в окуляр микроскопа и глаз наблюдателя (рис. 3.3). 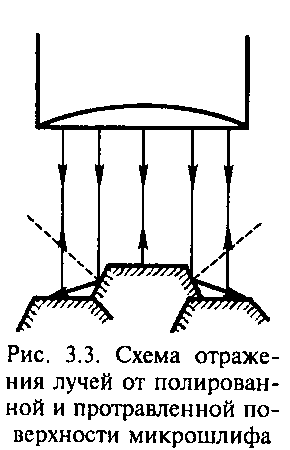 Оптические микроскопы позволяют получить увеличение до 1500 раз, что связано с длиной световой волны.
Оптические микроскопы позволяют получить увеличение до 1500 раз, что связано с длиной световой волны.
Вопросы для контроля
1. Какие задачи решает макроанализ.
2. Какие задачи решает микроанализ.
3. Какие характеристики металлов определяются при механических испытаниях.
Раздел 3. ТЕОРИЯ СПЛАВОВ. ДИАГРАММЫ СОСТОЯНИЯ
Чистые металлы во многих случаях не обеспечивают требуемых свойств, поэтому они применяются сравнительно редко. Более широко используются металлические сплавы. Их получают сплавлением или спеканием порошков двух или более металлов или металлов с неметаллами. Простые вещества, образующие сплав, называются компонентами сплава. Компоненты сплава образуют фазы. Фазой называют однородные части сплава, имеющие одинаковые состав, агрегатное состояние, кристаллическое строение, свойства и отделенные от других частей сплава поверхностями раздела. Под структурой понимают форму, размеры и характер взаимного расположения фаз в сплавах.
3.1. Типы сплавов
В процессе кристаллизации сплава могут образовываться следующие типы сплавов: твердые растворы, химические соединения и смеси.
Твердые растворы. Сплавы типа твердый раствор характеризуются тем, что при их образовании один компонент (растворитель) сохраняет свою кристаллическую решетку, а другой (растворимый) — отдает свои атомы в кристаллическую решетку растворителя. Образуется одна кристаллическая решетка, одна фаза. По механизму образования различают твердые растворы замещения и твердые растворы внедрения (рис. 4.1).
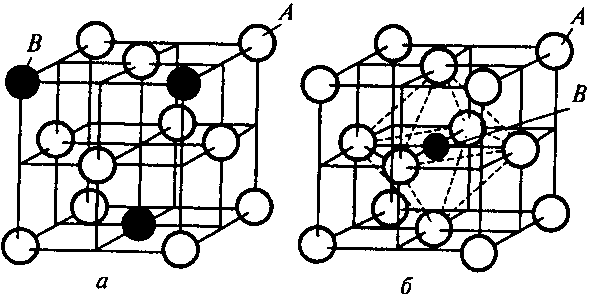
| Рис. 4.1. Схема твердых растворов замещения (а) и внедрения (б) |
При образовании твердых растворов замещения атомы растворимого компонента В замещают атомы растворителя А в его кристаллической решетке. По взаимной растворимости компонентов. различают твердые растворы замещения с неограниченной и с ограниченной растворимостью компонентов. В твердых растворах с неограниченной растворимостью компонентов возможна любая концентрация растворимого компонента (вплоть до 100 %). Твердые растворы замещения с неограниченной растворимостью образуются при следующих условиях:
-кристаллические решетки компонентов должны быть одного типа;
- различие атомных радиусов компонентов не должно превышать 8-15 %;
-компоненты должны принадлежать одной или смежным родственным группам периодической системы элементов и иметь одинаковое строение валентной оболочки электронов в атомах;
-расположение атомов в кристаллической решетке не упорядоченно.
Для образования твердых растворов замещения с ограниченной растворимостью необходимы те же условия, с той разницей, что наличие атомных радиусов может быть несколько большим. Такие твердые растворы образуют металлы, расположенные рядом в периодической системе элементов Д.И. Менделеева. При образовании твердых растворов внедрения атомы растворимого компонента В размещаются между атомами компонента растворителя А в его кристаллической решетке. Твердые растворы внедрения образуются только в тех случаях, если диаметр атома растворимого компонента невелик, такие твердые растворы возникают между металлами и элементами 1 и II периодов периодической системы элементов, имеющими малые атомные размеры (Н, N, С, В). Твердые растворы обозначают буквами греческого алфавита: α, β, γ и т. д. или А(В), где А — растворитель, В — растворимый компонент.
Твердые растворы наиболее близки по свойствам к металлу растворителю. Они, как правило, пластичны, хорошо деформируются в холодном и в горячем состояниях.
Химические соединения. Для них характерно следующее:
-кристаллическая решетка химического соединения отлична от кристаллических решеток образующих его компонентов;
-свойства химического соединения резко отличаются от свойств компонентов, которые его образовали;
- атомы в кристаллической решетке химического соединения расположены упорядоченно, т. е. атомы каждого компонента расположены закономерно и по определенным узлам кристаллической решетки;
-состав химического соединения можно описать стехиометрической формулой АmВn где n и m — взаимно простые целые числа;
-химическое соединение характеризуется постоянной температурой плавления;
-химические соединения имеют высокую твердость и хрупкость.
Химические соединения образуют вещества, имеющие большие отличия в электронном строении атомов и кристаллических решеток. Соединения типа «металл — металл» называются интерметаллидами. Соединения типа «металл — неметалл» имеют разные названия в зависимости от неметаллического материала: нитрид (металл — азот), карбид (металл — углерод), оксид (металл — кислород) и т. д. Интерметаллиды характеризуются металлическим типом связи, а соединения металлов с неметаллами — ионным.
Смеси. Такой тип соединения образуют компоненты, которые не растворяются друг в друге в твердом состоянии, а также не способны к химическому взаимодействию с образованием соединения. В сплавах типа «смесь» каждый компонент сохраняет свою кристаллическую решетку. Структура смеси гетерогенная (неоднородная), состоит из нескольких фаз (число фаз соответствует числу кристаллических решеток). Механические свойства смесей зависят от количественного соотношения компонентов, а также от размеров и формы фаз.
3.2. Диаграммы состояния сплавов
Диаграммы состояния представляют собой графическое изображение фазового состояния сплавов данной системы в зависимости от температуры и концентрации компонентов. Диаграммы состояния строят при условии равновесия системы. Равновесное состояние соответствует минимальному значению свободной энергии системы. Такое состояние может быть достигнуто при малых скоростях охлаждения или нагрева. Поэтому с помощью диаграмм состояния сплавов можно исследовать фазовые и структурные превращения, происходящие в сплавах при медленном нагреве или охлаждении.
Правило фаз. Состояние сплава зависит от внешних условий (температуры, давления) и характеризуется числом и химическим составом образовавшихся фаз. Возможность изменения внешних условий (температуры, давления, концентрации) без изменения числа фаз, находящихся в равновесии, называется вариантностью или числом степеней свободы системы. Правило фаз определяет взаимосвязь между числом степеней свободы, числом компонентов и числом фаз, находящихся в равновесии:
С = К + 2 — Ф,
Где, С — число степеней свободы; К — число компонентов; Ф — число фаз, находящихся в равновесии; 2 — число внешних факторов (температура, давление).
В металлических сплавах давление мало влияет на фазовое равновесие, поэтому приведенное уравнение принимает следующий вид:
С = К + 1 - ф.
Поскольку С не может быть отрицательным или дробным числом, то
К + 1 - Ф > 0,
Т.е. число фаз, находящихся в равновесии не может превышать число компонентов больше, чем на 1. Поэтому в двухкомпонентных сплавах в равновесии может находиться не более трех фаз. Если С = 0, это означает, что в равновесии находится максимальное число фаз (для двухкомпонентной системы — 3). При этом должны соблюдаться определенные условия — температура и концентрация компонентов не должны изменяться. Диаграммы состояния сплавов строят в координатах «температура — концентрация компонентов». Температуру откладывают по оси ординат, а концентрацию компонентов — по оси абсцисс. Общее содержание компонентов в сплаве равно 100 %, каждая точка на оси абсцисс соответствует определенному содержанию обоих компонентов. Для построения диаграмм состояния сплавов используют метод термического анализа. Он заключается в экспериментальном построении кривых охлаждения сплавов известного состава. По остановкам и перегибам на этих кривых, обусловленных тепловыми эффектами превращений, определяют температуры самих превращений. Точки перегиба или остановки на кривых охлаждения называются критическими точками и соответствуют температурам, при которых в сплавах начинают протекать или заканчиваться какие-либо превращения.
Поскольку в зависимости от числа компонентов сплавы могут быть двойными (двухкомпонентными), тройными (трехкомпонентными) и т.д., соответственно диаграммы состояния строят в системе двух координат — температура и концентрация (диаграммы состояния двойных сплавов), трех координат — температура и две оси концентрации (диаграммы состояния тройных сплавов). Для более сложных систем обычно строят пространственные диаграммы с некоторым упрощением либо сечения этих диаграмм по температурной или концентрационной оси.
В двойных сплавах по вертикали диаграммы состояния откладывают температуру, а по горизонтали — концентрацию компонентов. Каждая точка на оси абсцисс соответствует определенному содержанию одного и другого компонента с учетом того, что общее содержание компонентов в каждой точке этой оси соответствует 100 %. Поэтому по мере увеличения количества одного компонента сплава должно снижаться содержание в сплаве другого компонента.
Вид диаграммы состояния определяется характером взаимодействий, которые имеют место между компонентами сплавов в жидком и твердом состоянии. Во всех рассматриваемых далее случаях предполагается, что между компонентами сплава в жидком состоянии существует неограниченная растворимость, т.е. они образуют однородный жидкий раствор, обозначаемый буквой Ж. В твердом состоянии компоненты могут образовывать механические смеси из чистых компонентов, неограниченные твердые растворы, ограниченные твердые растворы, устойчивые химические соединения, неустойчивые химические соединения, а также испытывать полиморфные превращения.
Основные типы диаграмм состояния. Диаграмма состояния сплавов, образующих механические смеси из чистых компонентов (I poдa). Исходные данные: оба компонента неограниченно растворимы в жидком состоянии, а в твердом состоянии нерастворимы и не образуют химических соединений. Компоненты: химические элементы А, В (число компонентов К = 2). Фазы: жидкость Ж, кристаллы А, В (число фаз Ф = 3).
 Примером диаграмм этого типа является диаграмма состояния сплавов системы Pb— Sb. Диаграмма Pb — Sb строится на основе использования кривых охлаждения, полученных методом термического анализа (рис. 3.11)
Примером диаграмм этого типа является диаграмма состояния сплавов системы Pb— Sb. Диаграмма Pb — Sb строится на основе использования кривых охлаждения, полученных методом термического анализа (рис. 3.11)
Система сплавов Pb —Sb включает в себя составы со 100 % Pb и 0 % Sb, т.е. чистый свинец, и со 100 % Sb и 0 % Pb, т.е. чистую сурьму. Кривые охлаждения для этих чистых металлов имеют по одному горизонтальному участку, характеризующему температуру кристаллизации: соответственно для свинца 327° С, для сурьмы 631 °С. Сплав, содержащий 13% Sb и 87% Pb имеет один горизонтальный участок, т.е. одну критическую точку(246о С) - температуру затвердевания этого сплава. Этот сплав характеризуется тем. Что в нем происходит одновременная кристаллизация из жидкой фазы кристаллов Pb и Sb(в общем случае компонентов Аи В) с образованием механической смеси. Такая механическая смесь двух (или более) видов кристаллов, одновременно кристаллизующихся из жидкости, называется эвтектикой и обозначается буквой Э, сам сплав называется эвтектическим. Эвтектическую реакцию записывают так: Ж → Sb + Pb, или в общем виде: Ж→ А + В.
Линия, ограничивающая на диаграмме область жидкой фазы сплавов, называется линией ликвидус. Линия, ограничивающая область полностью затвердевшего сплава от остальной области на диаграмме состояний, называется линией солидус.
Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (2 рода). Исходные данные: оба компонента неограниченно растворимы в твердом и жидком состоянии и не образуют химических соединений. Компоненты: химические элементы А, В (К = 2). Фазы: жидкость Ж, кристаллы твердого раствора α (Ф = 2).
Примером сплавов с такими диаграммами состояния являются сплавы системы Си — Ni. Если два компонента (А и В) неограниченно растворяются в жидком и твердом состоянии, они не могут при затвердевании образовывать собственных кристаллов во всех сплавах на основе этих компонентов. Соответственно при кристаллизации в этих сплавах будут выделяться кристаллы твердого раствора α (α-твердого раствора), а следовательно, максимальное число фаз в этих сплавах равняется двум (жидкость и твердый раствор α). В этом случае в соответствии с правилом фаз кристаллизация всех сплавов будет протекать только в интервале температур (кристаллизация при постоянной температуре у сплавов возможна только ж наличии трех фаз) и, соответственно, на диаграмме состояния отсутствует горизонтальная линия, а присутствуют только наклонные кривые (рис.3.12).
На диаграмме присутствуют три области: область выше линии Аа|В — жидкость; область между линиями Аа'В и Аb'В — жидкость и твердый раствор; ниже линии Ab’B- область твердого раствора. Линия Аа|B является линией ликвидус, а линия Аb|В – линией солидус.
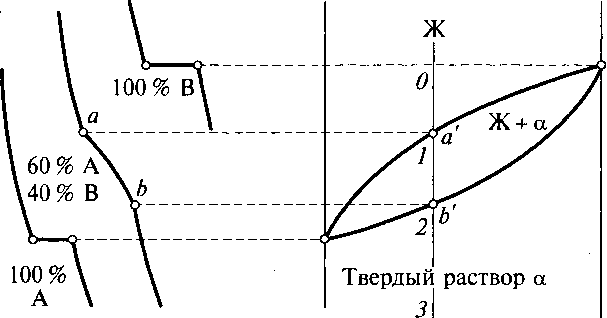

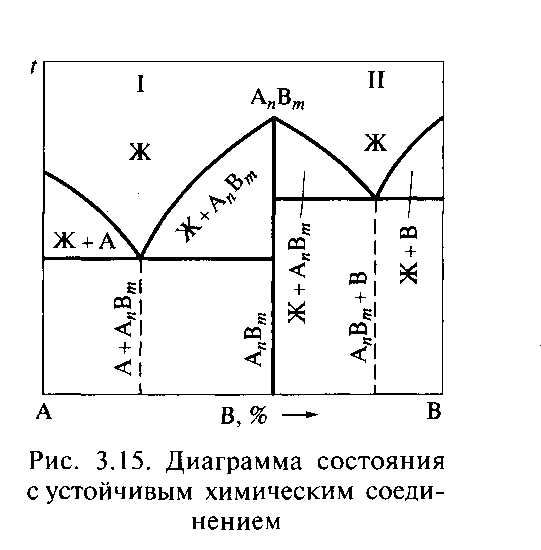
Диаграмма состояния сплавов, образующих химические соединение(IV рода). Исходные данные: оба компонента неограниченно растворимы в жидком состоянии, нерастворимы в твердом состоянии, но образуют химические соединения. Компоненты: химические элементы А и В (К = 2). Фазы: жидкость Ж, кристаллы компонентов А, В или химического соединения А nВm (Ф = 3). Химическое соединение может быть устойчивым, т.е. до расплавления сплава не разлагаться при нагреве. Соответственно неустойчивое химическое соединение при нагреве разлагается. Рассмотрим диаграмму состояния с устойчивым химическим соединением. Такая диаграмма изображена на рис. 3.15. Примером диаграмм этого типа является диаграмма состояния сплавов системы Mg —Са. Химическое соединение (например, АnBm) характеризуется определенным соотношением компонентов (например, n % компонента Аи т % компонента В). На оси концентрации компонентов (ось абсцисс) химическое соединение обозначает точку, из которой выходит вертикальная линия, фактически разбивающая диаграмму на две простые диаграммы, в которых химическое соединение выступает уже в качестве самостоятельного компонента и, соответственно, образует эвтектики с компонентом А по реакции Ж →А +АnВm (простая диаграмма I) и с компонентом В по реакции Ж → В + АпВт (простая диаграмма II). Кристаллизация сплавов в пределах простых диаграмм I и II происходит аналогично кристаллизации сплавов, образующих эвтектику из чистых компонентов (диаграмма I рода). Поэтому после окончательного остывания у эвтектического сплава на простой диаграмме I структура будет состоять только из эвтектики Э (А + АпВт),у эвтектического сплава на простой диаграмме II — из эвтектики Э (В + AnBm); у доэвтектических сплавов соответственно на простой диаграмме I и на простой диаграмме II структура будет иметь вид: А + Э (А + АпВт) и АпВт + Э (В + A„Bm); у заэвтектических сплавов на простой диаграмме I — АnВm + Э (А + АnВm) и у заэвтектических сплавов на простой диаграмме II — В + Э (В + АnВm).
3.3. Зависимость между свойствами сплавов и типом диаграммы состояния
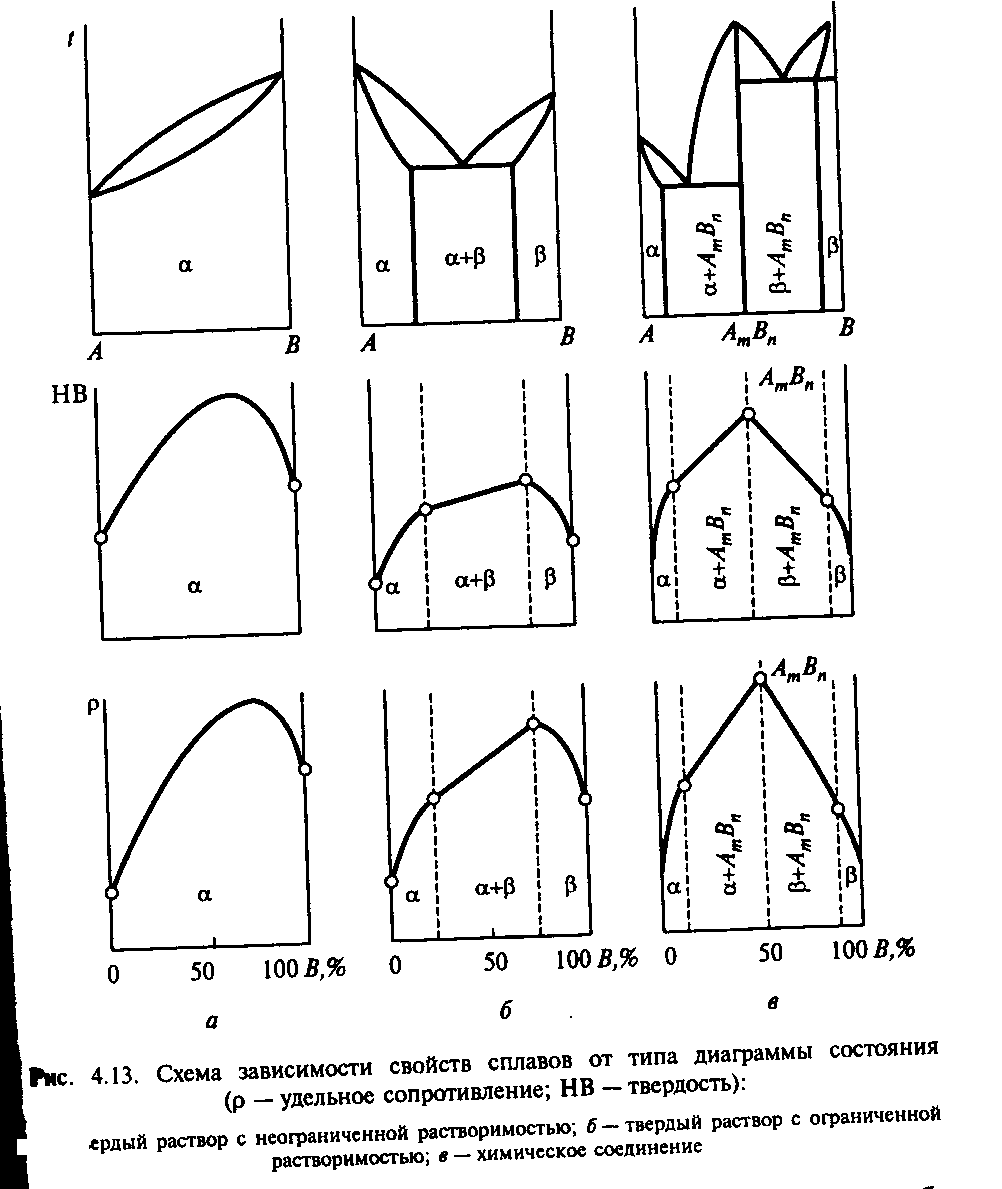
Правило Н. С. Курнакова устанавливает связь между типом диаграммы состояния и характером изменения физико-механических свойств сплавов в зависимости от содержания в них компонентов. Схематично эти зависимости представлены на рис. 4.13.
При образовании смесей значения твердости, прочности, электропроводности и некоторых других свойств изменяются прямолинейно в зависимости от концентрации компонентов.
При образовании твердых растворов свойства сплавов изменяются по криволинейной зависимости. Образование твердых растворов всегда сопровождается увеличением удельного электрического сопротивления, у сплавов оно всегда выше, чем у компонентов, образующих этот сплав.
При образовании химического соединения на кривой изменения свойств наблюдается перелом при концентрации компонентов, соответствующей химическому соединению, поскольку его свойства резко отличаются от свойств компонентов.
Вопросы для контроля
1.Дать определение компонента, фазы, структуры.
2. Перечислить типы сплавов, охарактеризовать каждый тип.
3.Какую информацию о сплавах дают диаграммы состояния? Как их строят?
4.Дать определение ликвации, виды ликвации и причина их появления.
5.Охарактеризовать зависимость между типом диаграммы состояния и свойствами сплавов.
Раздел 4. СПЛАВЫ ЖЕЛЕЗА И УГЛЕРОДА. СТАЛИ И ЧУГУНЫ.
ДИАГРАММА СОСТОЯНИЯ СПЛАВОВ «ЖЕЛЕЗО—ЦЕМЕНТИТ»
Сплавы железа широко используются в современной технике. Наибольшее применение нашли сплавы железа с углеродом - стали и чугуны. Объем их производства более чем в 10 раз превышает производство всех других металлов вместе взятых.
4.1. Железоуглеродистые сплавы (структурный и фазовый составы)
К железоуглеродистым относятся сплавы, основными компонентами которых являются железо и углерод. Железо обладает температурным полиморфизмом и может существовать в двух аллотропических модификациях: в виде α-железа с ОЦК и γ-железа с ГЦК кристаллическими решетками. С углеродом железо образует твердые растворы и химическое соединение.
Твердый раствор внедрения углерода в α-железе называется ферритом. Растворимость углерода в нем очень мала (максимум 0,02 % при температуре 727 °С). Феррит обладает низкой твердостью и высокой пластичностью.
Твердый раствор внедрения углерода в γ-железе называется аустенитом. Максимум растворимости углерода в аустените 2,14 % (при температуре 1147 °С). В равновесном состоянии аустенит существует лишь выше 727 °С. Он обладает высокой пластичностью и низкой твердостью.
Железо образует с углеродом химическое соединение Fe3C, называемое цементитом. Цементит очень тверд и хрупок.
Железоуглеродистые сплавы с концентрацией углерода, не превышающей 2,14 %, называют сталями, с более высокой - чугунами. По равновесной структуре стали в зависимости от содержания углерода подразделяют на техническое железо (С < 0,02 %), доэвтектоидные (0,02 < С < 0,8 %), эвтектоидные (С = 0,8 %) и заэвтектоидные стали (0,8 < С < 2,14 %).
В структуре технического железа присутствуют феррит и третичный цементит, выделяющийся при охлаждении сплава ниже 727 ° С из феррита.
Структура доэвтектоидной стали состоит из феррита и перлита. Перлит -это эвтектоид - механическая смесь феррита и цементита, образующаяся в результате эвтектоидной реакции из аустенита при охлаждении сплавов ниже 727 ° С (линии PSK диаграммы Fe-Fe3C). Перлит содержит 0,8 % углерода. По относительному количеству перлита можно судить о содержании углерода в сплаве. Для этого достаточно перемножить долю видимой на микрошлифе площади, занятой перлитом, на 0,8.
Эвтектоидная сталь содержит 0,8 % углерода. Структура ее полностью состоит из перлита.
В структуре заэвтектоидной стали содержатся перлит и вторичный цементит, выделяющийся при охлаждении сплава в интервале температур 1147... 727 ° С из аустенита в соответствии с линией предельной растворимости SE диаграммы Fe-Fe3C.
Чугуны в системе Fe-Fe3C называют белыми. Эти сплавы содержат углерод исключительно в химически связанном состоянии в виде Fe3C. Кристаллизация белых чугунов завершается эвтектическим превращением при температуре ниже 1147 ° С (линия ECF диаграммы Fe-Fe3C) с образованием эвтектики, называемой ледебуритом и представляющей собой механическую смесь аустенита и цементита. При охлаждении ниже 727 ° С аустенит претерпевает эвтектоидное превращение и ледебурит становится смесью перлита и цементита.
По равновесной структуре белые чугуны подразделяют на доэвтектичекие, эвтектические и заэвтектические.
Содержание углерода в доэвтектическом чугуне может находиться в пределах 2,14... 4,3 %. Структура его состоит из перлита, вторичного цементита и ледебурита.
Эвтектический чугун содержит 4,3 % углерода. Структура его состоит полностью из ледебурита.
В заэвтектическом чугуне содержится более 4,3 % углерода (до 6,67 %). Его структура состоит из первичного цементита, выделившегося из жидкости, и ледебурита.
Структуры феррита и аустенита приведены на рис. 6.2. Таким образом, в сплавах «железо—углерод» в твердом агрегатном состоянии существуют следующие фазы: феррит (Ф), аустенит А) и цементит (Ц). Они являются структурными составляющими, которые образуют различные смеси, в том числе характерные, имеющие постоянный химический состав, постоянную температуру образования и характерное строение. К их числу относятся эвтектика и эвтектоид.
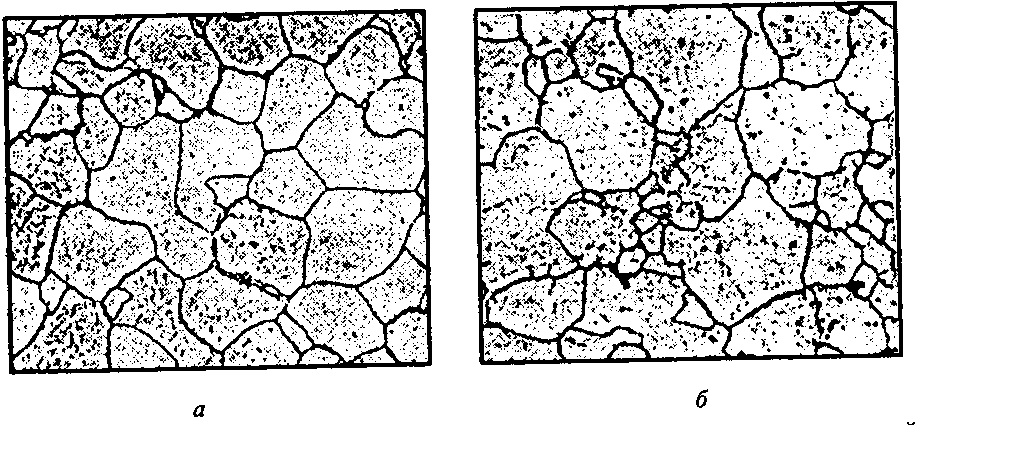
Рис. 6.2. Структура феррита (а) и аустенита б, выявленного при 1000 °С в вакуумной
камере (б), х 250
Диаграмма состояния системы железо-цементит.
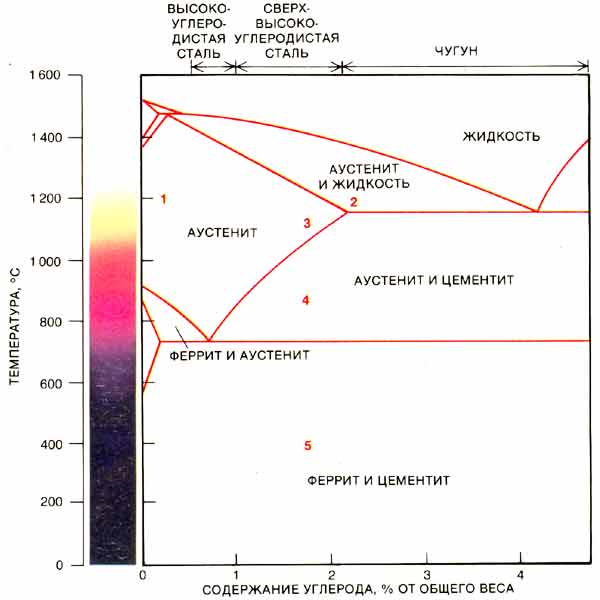
4.2. Углеродистые стали
Общая характеристика. Сплавы железа с углеродом, содержащие до 2,14 % углерода (точка Е, см. рис. 4.3) при малом содержании других элементов, называют углеродистыми сталями. Углеродистые стали завершают кристаллизацию образованием аустенита. В их структуре нет эвтектики (ледебурита), благодаря чему они обладают высокой пластичностью, особенно при нагреве, и хорошо деформируются.
Углеродистые стали выплавляют в электропечах, мартеновских печах и кислородных конвертерах. Наилучшими свойствами обладает электросталь, более чистая по содержанию вредных примесей — серы и фосфора, а также газов и неметаллических включений. Электросталь используют для изготовления наиболее ответственных деталей.
По способу раскисления различают кипящие, полуспокойные и спокойные стали. При одинаковом содержании углерода кипящие, полуспокойные и спокойные стали имеют близкие величины прочностных свойств и различаются значениями характеристик пластичности. Содержание кремния в спокойной стали составляет 0,15...0,35 %, в полуспокойной — 0,05...0,15, в кипящей — до 0,05 %.
Для раскисления кипящей стали кремний и алюминий не применяют, ее раскисляют марганцем. Кипящая сталь имеет резко выраженную химическую неоднородность в слитке. Ее основным достоинством является, высокий (более 95 %) выход годного металла. Благодаря низкому содержанию кремния и углерода кипящие стали хорошо штампуются в холодном состоянии. Из-за повышенной концентрации кислорода кипящие стали имеют сравнительно высокий порог хладноломкости, их не рекомендуют применять для изделий северного исполнения. У полуспокойной стали, раскисляемой марганцем и в ковше алюминием, выход годного металла составляет 90...95 %.
Спокойная сталь раскисляется кремнием, марганцем и алюминием. Выход годного металла слитков спокойной стали примерно 85 %, но металл значительно более плотен и имеет более однородный химический состав.
Свойства углеродистых сталей зависят от содержания основного элемента — углерода, а также от содержания постоянных и скрытых примесей.
Влияние углерода на свойства стали. Углерод является важнейшим элементом, определяющим структуру и свойства углеродистой стали. Даже малое изменение содержания углерода оказывает заметное влияние на свойства стали. С увеличением углерода в структуре стали растет содержание цементита. При содержании до 0,8 % углерода сталь состоит из феррита и перлита, при содержании более 0,8 % углерода в структуре стали кроме перлита появляется структурно-свободный вторичный цементит.
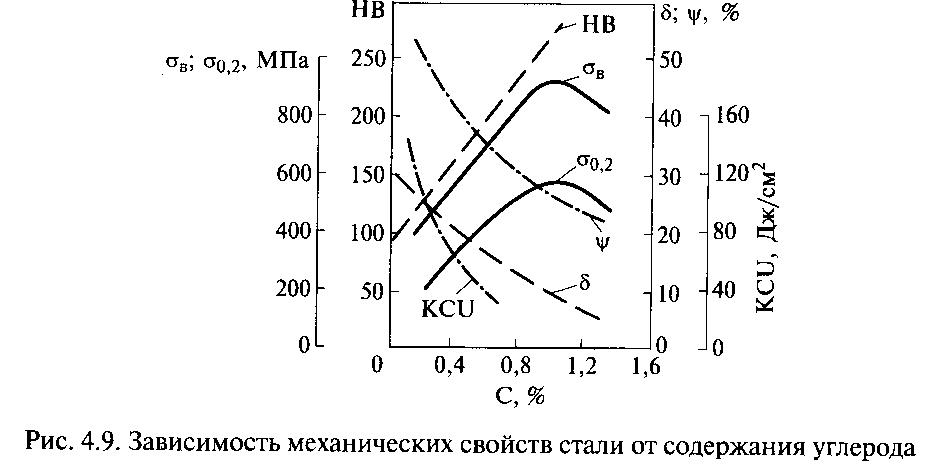
Феррит имеет низкую прочность, но сравнительно пластичен. Цементит характеризуется высокой твердостью, но хрупок. Поэтому с ростом содержания углерода увеличиваются твердость и прочность и уменьшаются вязкость и пластичность стали (рис. 4.9).
Рост прочности происходит при содержании в стали до 0,8... 1 % углерода. При увеличении содержания углерода более 1 % уменьшается не только пластичность, но и прочность стали. Это связано с образованием сетки хрупкого цементита вокруг перлитных зерен, легко разрушающейся при нагружении. По этой причине заэвтектоидные стали подвергают специальному отжигу, в результате которого получают структуру зернистого перлита.
Углерод оказывает существенное влияние на технологические свойства стали: свариваемость, обрабатываемость давлением и резанием. С увеличением содержания углерода ухудшается свариваемость, способность деформироваться в горячем и особенно в холодном состоянии.
Лучше всего обрабатываются резанием среднеуглеродистые стали, содержащие 0,3... 0,4 % углерода. Низкоуглеродистые стали при механической обработке дают плохую поверхность и трудноудаляемую стружку. Высокоуглеродистые стали имеют повышенную твердость, что снижает стойкость инструмента.
Влияние примесей на свойства стали. Постоянными примесями в углеродистых сталях являются марганец, кремний, сера, фосфор, а скрытыми — газы: кислород, азот, водород. Полезными примесями являются марганец и кремний. Их вводят в сталь в процессе выплавки для раскисления:
FeO + Mn = MnO + Fe; 2FeO + Si = Si02 + 2Fe
В углеродистой стали содержится до 0,8 % марганца. Марганец помимо раскисления в таком количестве полностью растворяется в феррите и упрочняет его, увеличивает прокаливаемость стали, а также уменьшает вредное влияние серы, связывая ее:
FeS + Mn = MnS + Fe
В полностью раскисленной углеродистой стали содержится до 0,4% кремния. Кремний является полезной примесью, так как эффективно раскисляет сталь и, полностью растворяясь в феррите, способствует его упрочнению.
Вредными примесями в стали являются сера и фосфор. Основной источник серы в стали — исходное сырье (чугун). Сера снижает пластичность и вязкость стали, а также сообщает стали красноломкость при прокатке и ковке. Сера нерастворима в стали. С железом сера образует сульфид железа FeS, хорошо растворимый в металле. При малом содержании марганца благодаря высокой ликвации серы в стали может образовываться легкоплавкая эвтектика Fe—FeS (Тпл= 988 °С). Эвтектика располагается по границам зерен.
При нагреве стальных заготовок до температуры горячей деформации включения эвтектики сообщают стали хрупкость, а при некоторых условиях могут даже плавиться и при деформировании образовывать надрывы и трещины. Марганец устраняет красноломкость, так как сульфиды марганца не образуют сетки по границам зерен и имеют температуру плавления примерно 1620 ° С, что выше температуры горячей деформации. Вместе с тем сульфиды марганца, как и другие неметаллические включения, также снижают вязкость и пластичность, уменьшают усталостную прочность стали. Поэтому содержание серы в стали должно быть как можно меньше.
Повышенное (до 0,2%) содержание серы допускается лишь в автоматных сталях ддя изготовления крепежных деталей неответственного назначения. Сера улучшает обрабатываемость стали.
Основной источник фосфора — руды, из которых выплавляют исходный чугун. Фосфор является вредной примесью, способной в количестве до 1,2 % растворяться в феррите. Фосфор, растворяясь в феррите, уменьшает его пластичность. Фосфор резко отличается от железа по типу кристаллической решетки, диаметру атомов и их строению. Поэтому фосфор располагается вблизи границ зерен и способствует их охрупчиванию, повышая температурный порог хладноломкости.
Скрытые примеси — кислород, азот, водород — присутствуют в стали либо в виде твердого раствора в феррите, либо в составе химических соединений (нитриды, оксиды), либо в свободном состоянии в порах металла. Кислород и азот малорастворимы в феррите, загрязняют сталь хрупкими неметаллическими включениями, что снижает вязкость и пластичность стали. Водород находится в твердом растворе и особенно сильно охрупчивает сталь. Повышенное содержание водорода, особенно в хромистых и хромоникелевых сталях, приводит к образованию внутренних трещин — флокенов.
Даже небольшие концентрации газов оказывают резко отрицательное влияние на свойства, ухудшая пластические и вязкие характеристики стали. Поэтому вакуумирование является важной операцией для улучшения свойств стали.
Кроме того, в углеродистых сталях присутствуют такие случайные примеси, как хром, никель, медь, наличие которых обусловлено загрязненностью шихты.
Классификация углеродистых сталей. Углеродистые стали классифицируют по структуре, способу производства и раскисления, по качеству.
По структуре различают доэвтектоидную сталь, содержащую до 0,8 % углерода, структура которой состоит из феррита и перлита; эвтектоидную, содержащую примерно 0,8 % углерода, структура которой состоит только из перлита; заэвтектоидную, содержащую 0,8...2,14 % углерода; ее структура состоит из зерен перлита, окаймленных сеткой цементита.
По способу производства различают стали, выплавляемые в электропечах, мартеновских печах и кислородно-конвертерным способом.
По способу раскисления различают кипящие, полуспокойные и спокойные стали.
По качеству различают стали обыкновенного качества и качественные стали. Стали обыкновенного качества содержат не более 0,05 % серы и не более 0,04 % фосфора. Качественные стали содержат не более 0,04 % серы (в случае инструментальных сталей до 0,03 %) и не более 0,035 % фосфора, они менее загрязнены неметаллическими включениями и газами.
В особо ответственных случаях применяют стали, содержащие менее 0,02 % серы и 0,03 % фосфора. Поэтому при одинаковом содержании углерода качественные стали имеют более высокие пластичность и вязкость, особенно при низких температурах. Качественные стали предпочтительнее для изготовления изделий, эксплуатируемых при низких температурах, в частности в условиях Севера и Сибири.
Стали обыкновенного качества изготавливают по ГОСТ 380—94. Выплавка их обычно производится в крупных мартеновских печах и кислородных конвертерах. Обозначают их буквами Ст и цифрами от 0 до 6, например: СтО, Ст1, Ст6. Буквы Ст означают «сталь», цифры — условный номер марки стали в зависимости от ее химического состава. В конце обозначения марки ставят буквы кп, пс, сп, которые указывают на способ раскисления: кп — кипящая, пс — полуспокойная, сп — спокойная.
Химический состав стали должен соответствовать нормам. Чем больше цифра условного номера стали, тем выше в ней содержание углерода. Содержание серы в стали всех марок, кроме СтО, должно быть не более 0,05%, фосфора — не более 0,04 %; в стали марки СтО серы — не более 0,06 %, фосфора — не более 0,07 %.
Качественные углеродистые стали выплавляют в электропечах, кислородных конвертерах и мартеновских печах по ГОСТ 1050—88. Качественные стали поставляют по химическому составу и механическим свойствам.
К качественным сталям предъявляют более жесткие требования по содержанию вредных примесей (серы не более 0,04 %, фосфора не более 0,035 %). Для сталей марок 11кп и 18кп, применяемых для плакировки, содержание серы должно быть не более 0,035 %, фосфора не более 0,030 %.
Качественные углеродистые стали маркируют двузначными цифрами 05, 10, 15, 60, указывающими среднее содержание углерода в сотых долях процента.
При обозначении кипящей или полуспокойной стали в конце марки указывают степень раскисления: кп, пс. Для спокойной стали степень раскисления не указывают.
По содержанию углерода качественные углеродистые стали подразделяют на низкоуглеродистые (до 0,25% углерода), среднеуглеродистые (0,3...0,5% углерода) и высокоуглеродистые конструкционные (до 0,65 % углерода).
Для изделий ответственного назначения применяют высококачественные стали с еще более низким содержанием серы и фосфора. Необходимость обеспечения низкого содержания вредных примесей в высококачественных сталях дополнительно повышает стоимость и усложняет их производство. Поэтому обычно высококачественными сталями бывают не углеродистые, а легированные стали.
При обозначении высококачественных сталей в конце марки добавляется буква А, например сталь У10А.
Углеродистые стали, содержащие 0,7... 1,3% углерода, используют для изготовления ударного и режущего инструмента. Их маркируют У7, У13, где буква У означает углеродистую сталь, а цифра — содержание углерода в десятых долях процента.
4.3. Чугуны
Железосодержащие сплавы - чугуны имеют более высокое содержание углерода, заканчивают кристаллизацию образованием эвтектики, обладают низкой способностью к пластической деформации и высокими литейными свойствами. Их технологические свойства обусловлены наличием эвтектики в структуре. Стоимость чугунов ниже стоимости стали. Чугуны выплавляют в доменных печах, вагранках и электропечах. Выплавляемые в доменных печах чугуны бывают передельными, специальными (ферросплавы) и литейными. Передельные и специальные чугуны используют для последующей выплавки стали и чугуна. В вагранках и электропечах переплавляют литейные ш. Около 20 % всего выплавляемого чугуна используют для изготовления литья. В литейном чугуне обычно содержится не более 4 % углерода. Кроме углерода обязательно присутствуют примеси серы, фосфора, марганца и кремния, причем в значительно большем количестве, чем в углеродистой стали. В зависимости от формы выделения углерода различают следующие виды чугунов.
Чугуны со структурно свободным углеродом в зависимости от геометрической формы графитных включений называют: серыми (графит пластинчатой формы), ковкими (графит хлопьевидной формы), высокопрочными (графит шаровидной формы). Металлическая основа чугунов может быть ферритной, ферритно-перлитной и перлитной. В ферритных чугунах (чугунах с ферритной металлической основой) нет углерода, связанного в Fe3C. В перлитных - 0,8 % углерода связано в цементит. При одинаковой металлической основе механические свойства чугунов возрастают от серого к высокопрочному.
Белый чугун, в котором весь углерод находится в связанном состоянии в виде цементита Fe3C. Чугун в изломе имеет белый цвет и характерный блеск.
Половинчатый чугун, в котором основное количество углерода (более 0,8 %) находится в виде цементита. Чугун имеет структуру перлита, ледебурита и пластинчатого графита.
Серый чугун, в котором весь углерод или его большая часть находится в свободном состоянии в виде пластинчатого графита, а содержание углерода в связанном состоянии в виде цементита составляет не более 0,8 %.
Чугун с отбеленной поверхностью, в котором основная масса металла имеет структуру серого чугуна, а поверхностный слой - белого чугуна. Отбеленный слой получают в толстостенных массивных деталях при литье их в металлические формы. По мере удаления от поверхности вследствие уменьшения скорости охлаждения структура белого чугуна постепенно переходит в структуру серого. Чугун поверхностного слоя в микроструктуре содержит много твердого и хрупкого цементита, который хорошо сопротивляется изнашиванию. Поэтому чугуны с отбеленной поверхностью используют для деталей с высокой износостойкостью, для валков прокатных станов, мукомольных валов, вагонных колес с отбеленным ободом, лемехов плугов с отбеленным носком и лезвием.
Серые чугуны получают при охлаждении отливок с обычными скоростями, характерными для песчаных форм. Маркируют серые чугуны буквами СЧ и числом, обозначающем временное сопротивление σв в кгс/мм2 (в десятых долях МН/м2).
Ковкие чугуны, в которых углерод находится в виде хлопьевидного графита, получают из белых чугунов путем длительного графитизирующего отжига белых чугунов. Маркируют ковкий чугун буквами КЧ и двумя числами, первое из которых - σв в кгс/мм2, второе - относительное удлинение δ в %.
Высокопрочные чугуны, в которых графит имеет шаровидную форму, получают путем модифицирования жидкого сплава магнием или церием. Маркируют чугуны буквами ВЧ и числом, обозначающим σ в кгс/мм2.
Вопросы для контроля
1. Дать определение фаз, образующихся в системе «железо-цементит».
2. Назвать характерные структуры, образующиеся в железоуглеродистых сплавах, общие параметры и принципиальное различие.
3. Описать превращения, протекающие в сплавах, содержащих 0,3%С; 0,8%С; 1,0%С; 2,5%С; 4,3%С; 5,0%С.
4. Назвать принципиальное различие сталей и чугунов.
5. Назвать постоянные примеси в сталях. В чем заключается влияние вредных примесей и какова роль полезных примесей.
6. Привести классификацию сталей по структуре, назначению и качеству. По какому принципу и как маркируют стали?
7. Назвать и охарактеризовать виды чугунов в зависимости от состояния.
Раздел 5. ТЕОРИЯ ТЕРМООБРАБОТКИ. ТЕРМИЧЕСКАЯ И ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ
5.1. Термическая обработка стали
Термической называют обработку, связанную с нагревом и охлаждением металла с целью изменения его структуры и свойств.
Температурные режимы термообработки сталей связаны с диаграммой Fe-Fe3 C. Равновесные температуры, отвечающие положению линий PSK, GS и SE диаграммы, обозначают А1, A3 и Ат соответственно. При нагреве неравновесные температуры превращений обозначают: перлита в аустенит -Ас1 превращений, связанных с получением однофазной аустенитной структуры, - Ас3 (для доэвтектоидных сталей), Аст (для заэвтектоидных). При обычных скоростях нагрева неравновесные температуры на 30... 50 °С выше соответствующих равновесных.
В зависимости от склонности аустенитного зерна при нагреве к росту различают наследственно крупнозернистые (зерно склонно к росту) и наследственно мелкозернистые (зерно не склонно к росту) стали. Свойства стали, возникшие в результате той или иной обработки, определяются реально образовавшимся зерном - действительным зерном. Наследственная зернистость должна учитываться при назначении режимов обработки, влияющей на размер получаемого действительного зерна, например, при закалке, отжиге.
Основными видами термической обработки сталей являются отжиг (первого и второго рода), закалка, отпуск.
Отжиг состоит в нагреве металла, выдержке и последующем медленном охлаждении (вместе с печью). Отжиг приближает металл к равновесию.
Отжиг первого рода проводят для получения более равновесной, чем исходная, структуры, не связывая эту цель с наличием или отсутствием фазовой перекристаллизации. Примерами отжига первого рода являются рекристаллизационный отжиг, диффузионный отжиг.
При рекристаллизационном отжиге деформационно упрочненный металл нагревают несколько выше температурного порога рекристаллизации. В результате отжига материал приобретает такие же механические свойства, какие он имел до деформации.
Диффузионный (гомогенизирующий) отжиг проводят при нагреве до высоких температур (применительно к сталям - значительно выше Ас3 или Аст предполагающих интенсивную диффузию атомов. Такому отжигу подвергают, например, отливки для устранения дендритной ликвации (гомогенизации сплава).
При отжиге второго рода непременно протекает, хотя бы частичная, фазовая перекристаллизация. К отжигу второго рода относятся неполный отжиг, полный отжиг.
При неполном отжиге нагрев ведут до температуры Ас] (ниже Ас3 или Аст). Происходит частичная перекристаллизация сплава (меняется перлитная составляющая). Чаще неполный отжиг применяют для заэвтектоидных сталей (сфероидизирующий отжиг).
При полном отжиге сталь нагревают до Ас3 или Аст. Происходит полная перекристаллизация сплава.
Закалка состоит в нагреве сплавов выше температур фазовых превращений и последующем быстром охлаждении, фиксирующем их высокотемпературное состояние (истинная закалка) или состояние, промежуточное между высокотемпературным и равновесным, характерным для нормальной температуры.
Теоретическая возможность осуществления закалки определяется видом диаграммы состояния системы, которой принадлежит сплав. Необходимо, чтобы при нагреве он испытывал, хотя бы частичную, твердофазовую перекристаллизацию. Применительно к сталям нагрев при закалке обычно ведут до температуры Ас3 (доэвтектоидные стали) и Ас] (заэвтектоидные стали). Если нагрев ведется до температур Ас3 или Аст, то такая закалка называется полной, если до Ас] - неполной.
В зависимости от скорости охлаждения существуют два принципиально различных способа закалки - закалка на ферритно-цементитные смеси и закалка на мартенсит. При охлаждении со скоростью ниже критической, т.е. такой минимальной скорости, которая необходима для образования мартенсита, возникают структуры перлитного типа (перлит, сорбит, троостит, бейнит). Сорбит и троостит отличаются от перлита и друг от друга степенью дисперсности (троостит дисперснее сорбита, а последний - перлита). Чем структура дисперснее, тем выше ее механические свойства.
Охлаждение со скоростью выше критической ведет к превращению аустенита в мартенсит. Суть превращения состоит в перестройке кристаллической решетки аустенита (ГЦК) в решетку феррита (ОЦК). При этом углерод, растворенный в аустените, оказывается полностью в решетке феррита. Таким образом, мартенсит представляет собой пересыщенный твердый раствор углерода в феррите. Кристаллическая решетка мартенсита - тетрагональная (искаженная решетка феррита с увеличенным параметром с).
Если при полной закалке (полном отжиге) охлаждение нагретой заготовки ведут на спокойном воздухе, то такая термическая обработка называется нормализацией.
Большинство легирующих элементов, растворенных в аустените, повышают его временную устойчивость, сдвигая С-образные кривые изотермического превращения аустенита вправо по координатной оси времени. При этом критическая скорость закалки уменьшается. (В сталях мартенситного типа этого уменьшения оказывается достаточно, чтобы уже при нормализации получить мартенситную структуру).
Мартенситное превращение протекает по бездиффузионному, сдвиговому механизму. Отличительными особенностями мартенситного превращения являются бездиффузионность и ориентированность (иглы мартенсита находятся под определенными углами относительно друг друга в соответствии с расположением плоскостей легкого скольжения в аустените).
Мартенситное превращение не захватывает всю аустенитную структуру. Часть аустенита сохраняется в закаленной стали. Такой аустенит называют остаточным. Количество остаточного аустенита определяется режимами термической обработки и зависит от температур начала и конца мартенситного превращения.
Мартенсит - самая твердая структура, образующаяся при термообработке сталей. Чем больше в нем углерода, тем он тверже.
Заэвтектоидные стали, в отличие от доэвтектоидных, подвергают неполной закалке. Это объясняется тем, что избыточная фаза заэвтектоидных сталей (цементит) обладает высокой твердостью, и наличие дисперсных включений цементита повышает износостойкость стали. Нагрев до Аст привел бы к растворению цементита и, кроме того, к укрупнению аустенитного зерна, а, следовательно, к возникновению после закалки структуры крупноигольчатого мартенсита, обладающего пониженными механическими свойствами. Если неполной закалке подвергнуть доэвтектоидную сталь, то избыточная фаза (феррит), имеющая малую твердость, понизит механические свойства закаленного сплава.
Температура начала мартенситного превращения не зависит от скорости охлаждения, но определяется составом сплава. Углерод и большинство легирующих элементов сдвигают точки начала и конца превращения к более низким температурам.
Мартенсит - термодинамически неустойчивая структура. Нагрев, повышая подвижность атомов, приводит к образованию более устойчивых структур (троостит, сорбит, перлит). С повышением температуры снижается твердость и возрастает пластичность сплава.
Термическая обработка, состоящая в нагреве закаленной стали до температуры ниже А1, выдержке и последующем охлаждении с произвольной скоростью, называется отпуском. Чем выше нагрев, тем в большей степени структура приближается к равновесной. Различают три вида отпуска: низкий (t = 150... 250 °С), средний (t = 350... 500 °С) и высокий (t = 500... 680 °С).
Сочетание закалки и высокого отпуска называют улучшением, а стали, предназначенные для такой обработки (среднеуглеродистые стали), - улучшаемыми.
В некоторых случаях нагрев при отпуске заменяют длительной выдержкой при нормальной температуре. Такая обработка называется старением. Если старение проводят с небольшим нагревом, то его называют искусственным.
Обычно при среднем отпуске образуется трооститная структура, при высоком - сорбитная. От одноименных структур закалки троостит и сорбит отпуска отличается тем, что цементитные частицы в них имеют зернистую форму (в структурах закалки - пластинчатую).
Большинство легирующих элементов сдерживают мартенситное превращение, сдвигая его в область более высоких температур.
Следует различать термины "закаливаемость" и "прокаливаемость". Закаливаемость - это способность металла повышать твердость при закалке. Прокаливаемость - это глубина, на которую распространяется закаленная область. При сквозной прокаливаемости свойства материала однородны и достаточно высоки по всему сечению. Количественно прокаливаемость оценивается критическим диаметром, под которым понимают наибольший диаметр прутка, прокаливающегося насквозь (в центре возникает полумартенситная структура, состоящая на 50 % из троостита и на 50 % из мартенсита) в данном охладителе. Чем больше скорость теплоотвода (охлаждения), тем на большую глубину прокаливается изделие. Поэтому критический диаметр при охлаждении в воде больше, чем в масле, и тем более больше, чем на воздухе. Особенно сильно увеличивают прокаливаемость сталей легирующие элементы (кроме кобальта), растворенные в аустените. Критический диаметр зависит от критической скорости закалки. Чем скорость меньше, тем больше диаметр.
В ряде случаев применяют закалку, при которой высокому нагреву подвергают лишь поверхностный слой материала (поверхностная закалка). В результате поверхностной закалки изделие приобретает высокую поверхностную твердость, сердцевина же остается вязкой. Широко применяют закалку с индукционным нагревом токами высокой частоты (ТВЧ). Чем выше частота тока, тем тоньше слой, в котором индуцируются токи, и тем тоньше окажется закаленный слой.
Дата публикования: 2015-11-01; Прочитано: 3122 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
